Pfortaderthrombose: Risikofaktoren, bildgebende Diagnostik, Komplikationen
Autor:
Prim. Univ.-Prof. Dr. Wolfgang Schima, MSc.
Abteilung für Diagnostische und Interventionelle Radiologie
Krankenhaus Göttlicher Heiland, Wien
Krankenhaus Barmherzige Schwestern, Wien
St. Josef Krankenhaus, Wien
E-Mail: wolfgang.schima@khgh.at
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Die Risikofaktoren für eine Pfortaderthrombose (PVT) sind vielfältig, häufig entwickelt sie sich als Folge einer Leberzirrhose. Das Vorliegen einer akuten Dekompensation verdoppelt das Risiko. Zu den typischen Symptomen zählen abdominelle Schmerzen, Diarrhö und Erbrechen, wobei auch eine symptomlose PVT möglich ist.
Keypoints
-
Der Risikofaktor Nr.1 für das Auftreten einer Pfortaderthrombose ist die Leberzirrhose, es gibt aber auch eine Reihe anderer angeborener und erworbener Risikofaktoren (Gerinnungsstörungen, myeloproliferative Erkrankungen, orale Kontrazeptiva, Pankreatitis, Divertikulitis etc.)
-
Bildgebende Diagnostik erfolgt mittels farbcodierter Duplexsonografie, Kontrastmittel-verstärkter CT oder MRT, wobei die CT am besten das Ausmaß der Thrombose und mögliche Komplikationen zeigt.
-
Die gefürchtetste Komplikation einer PVT mit Ausdehnung in die Mesenterialvenen ist die Dünndarmnekrose mit hoher Letalität.
Eine Pfortaderthrombose (PVT) ist definiert als das Auftreten eines Thrombus in der Pfortader oder ihrer Äste mit oder ohne Ausdehnung in die V.mesenterica superior und V.lienalis. Die Diagnose wird entweder mittels farbcodierter Duplexsonografie, Kontrastmittel-verstärkter Multidetektor-Computertomografie (MDCT) oder Magnetresonanztomografie (MRT) gestellt.
Die einer PVT potenziell zugrunde liegenden Risikofaktoren und Erkrankungen sind vielfältig, wobei der Pathomechanismus die Trias Hyperkoagulabilität, portale Hypertension (mit reduziertem Pfortaderfluss) und endotheliale Gefäßschädigung umfasst. Primär ist die Differenzierung der PVT in die (häufige) Zirrhose-assoziierte und die (seltenere) nicht-Zirrhose-assoziierte Form wichtig. Bei Non-Zirrhose-Patienten sollte eine sorgfältige Evaluierung möglicher Ursachen durchgeführt werden, da davon die weitere Therapie abhängt.
Wie häufig ist eine Pfortaderthrombose?
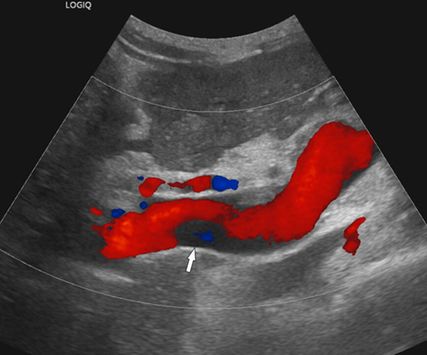
Abb. 1: Die farbcodierte Duplexsonografie zeigt einen wandständigen (nichtokklusiven) Thrombus (Pfeil) in der perfundierten Pfortader
Eine groß angelegte schwedische Autopsiestudie fand eine Prävalenz der PVT von 1%.6 In klinischen Studien wurden deutlich geringere Inzidenzen und Prävalenzen erhoben, 0,7/100000/Jahr (Inzidenz) und 3,7/100000 (Prävalenz).7 Diese um den Faktor 300 niedrigere Prävalenz deutet darauf hin, dass in klinischen Studien die Häufigkeit einer Pfortaderthrombose deutlich unterschätzt wird, weil offenbar eine erhebliche Anzahl klinisch asymptomatisch verläuft.
Bildgebende Diagnostik
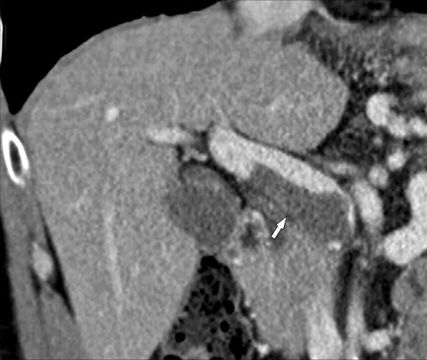
Abb. 2: Die Kontrastmittel-verstärkte MDCT (koronale 3D-Rekonstruktion) kann das Ausmaß einer PVT exakt abbilden: Die Thrombose ist nur im Pfortaderhauptstamm lokalisiert (Pfeil)
Die bildgebende Diagnostik stützt sich auf die farbcodierte Duplexsonografie (Abb. 1), die Kontrastmittel-verstärkte MDCT (Abb. 2) und die MRT, wobei die MDCT die höchste Aussagekraft hinsichtlich Ausdehnung der PVT und Darstellung möglicher Komplikationen hat. Wichtig ist bei der MDCT die Anfertigung von 3D-Rekonstruktionen des MDCT-Datensatzes zur besseren Darstellung der Thromboseausdehnung (Abb. 2), im Vergleich zur ausschließlichen Darstellung auf axialen Bildern.
Klassifikation der Ausdehnung
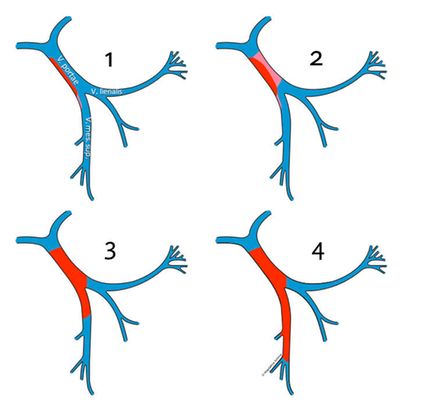
Die Pfortaderthrombose wird nach dem Ausmaß der Pfortaderokklusion und der Ausdehnung der Thrombose in das Splanchnicusgebiet (V.mesenterica superior) entsprechend der Yerdel-Klassifikation in 4 Grade eingeteilt (Abb. 3):8
-
Grad 1: minimale oder partielle Thrombose der Pfortader, mit/ohne minimale Ausdehnung in die V.mes.sup.
-
Grad 2: Thrombose der Pfortader mit Einengung ≥50% oder komplette Thrombose, mit/ohne minimale Ausdehnung in die V.mes.sup.
-
Grad 3: komplette Thrombose der Pfortader und der proximalen V.mes.sup.
-
Grad 4: komplette Thrombose der Pfortader und der proximalen und distalen V.mes.sup.
Ursachen und Risikofaktoren
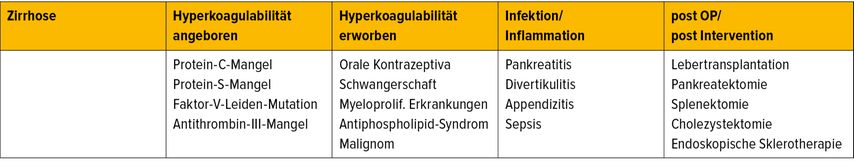
Es sind multiple Ursachen und Risikofaktoren für die Entwicklung einer PVT bekannt, wobei pathophysiologisch die „Virchow-Trias“ die Hautrolle spielt, bestehend aus Hyperkoagulabilität, reduzierter Blutfluss- bzw. Flussgeschwindigkeit in der Pfortader und endothelialen Läsionen des Gefäßes.1 Die wichtigsten Risikofaktoren5 sind in Tabelle 1 aufgelistet.
PVT bei Zirrhose
Die Häufigkeit einer PVT bei Zirrhosepatienten wird in einer rezenten Studie mit ca. 10% angegeben,2 wobei die Angaben in anderen Studien eine große Schwankungsbreite aufweisen (5–26%).3 Das Vorliegen einer akuten Dekompensation verdoppelt das Risiko, eine PVT zu entwickeln (von 5,2% auf 9,4%).9 Ein Zusammenhang zwischen Ursache der Zirrhose und Häufigkeit der PVT konnte bislang nicht verifiziert werden. Ein wesentlicher Risikofaktor ist die portale Hypertension, welche zu einem reduzierten Blutfluss in der Pfortader mit Verringerung der Fließgeschwindigkeit führt. Eine Pfortaderflussgeschwindigkeit von <15cm/s erhöht das Risiko, eine PVT zu entwickeln.
Zirrhose und HCC
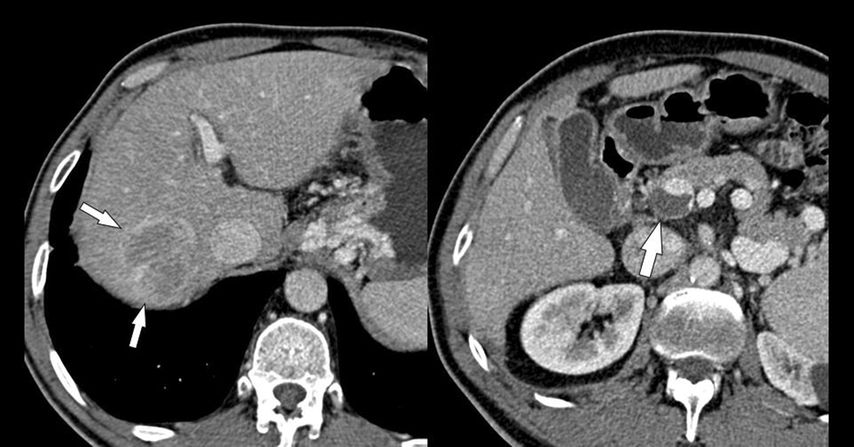
Die Häufigkeit eines hepatozellulären Karzinoms (HCC) ist wesentlich größer bei PVT-positiven als bei PVT-negativen Zirrhosepatienten (28,9% vs. 13,4%), was damit zusammenhängen mag, dass beide eher bei fortgeschrittener Zirrhose auftreten. Es ist essenziell, mittels Bildgebung nachzuweisen, dass der Pfortaderthrombus nicht mit dem HCC in Zusammenhang steht (Abb. 4). Ein HCC bei „blander“ Pfortaderthrombose ist in Abhängigkeit von Tumorstadium und Leberfunktion unter Umständen einer kurativen Behandlung (Resektion, interventionell-radiologische Tumorablation, Transplantation) zugänglich, während ein HCC mit „Tumorthrombus“ eine Kontraindikation für derartige Behandlungen darstellt.
Abb. 4: HCC und PVT: Das HCC im rechten Leberlappen (kleine Pfeile links) hat keinerlei Verbindung zum (blanden) Thrombus im Pfortaderhauptstamm, der kein Kontrastmittel aufnimmt (großer Pfeil)
Zirrhose und „HCC mit Tumorthrombus“
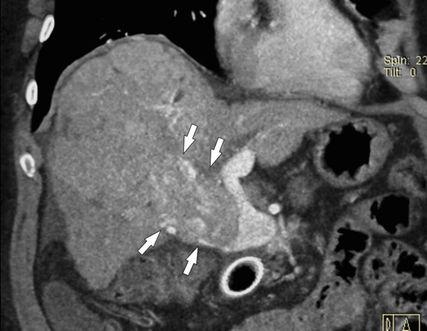
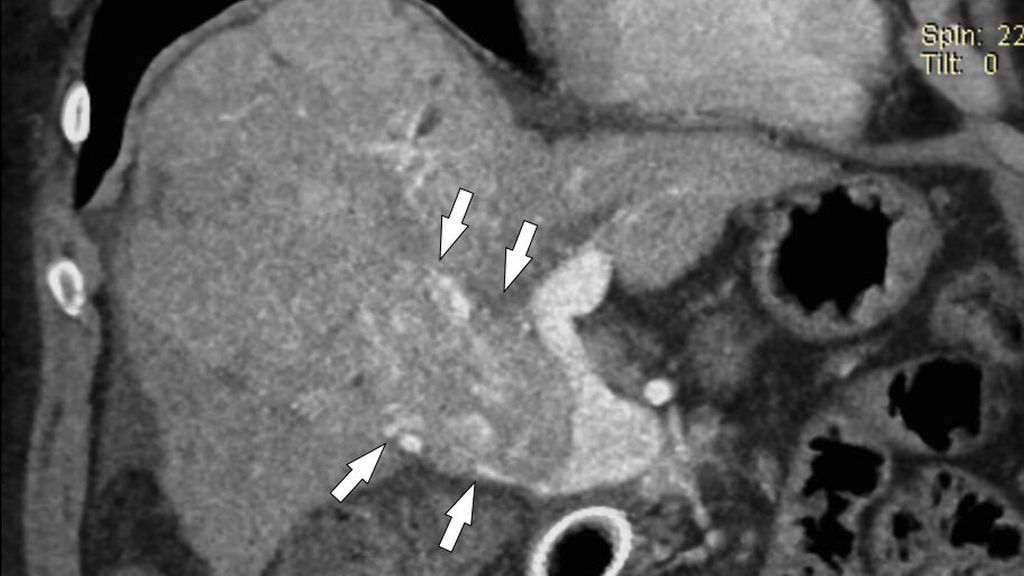
Abb. 5: HCC mit Tumoreinbruch in die Pfortader: Die MDCT (koronale 3D-Rekonstruktion) zeigt den Kontrastmittel-aufnehmenden Tumor, der vom rechten Leberlappen in den rechten Pfortaderast vorwächst und diesen massiv aufweitet (Pfeile)
Die Bezeichnung „HCC mit Tumorthrombus“ ist irreführend und sollte nicht mehr verwendet werden, da es hierbei zu einem direkten Vorwachsen des HCC in die Pfortaderäste (u.U. bis in den Hauptstamm) kommt und nicht zur Bildung eines Thrombus. In der MDCT oder der MRT ist dafür typisch, dass man ein kontinuierliches Vorwachsen des HCC aus dem Parenchym in die Pfortaderäste erkennt. Der intravasale Tumoranteil weitet die Pfortader aus und zeigt ein Kontrastmittelenhancement wie der Tumor (Abb. 5), während ein blander Thrombus typischerweise keine Kontrastmittelaufnahme aufweist (Abb. 5). Der intravasale Tumoranteil muss daher auch wie ein Tumor behandelt werden und nicht wie eine Thrombose. Das American College of Radiology hat deshalb in seiner LI-RADS®-Guideline für die Beurteilung von hepatalen Knoten in der Zirrhose die KategorieLI-RADS TIV („tumor in vein“) geschaffen, um diese besondere Tumorentität von den HCC mit oder ohne PVT klar abzugrenzen.
PVT bei anderen Risikofaktoren
Die Risikofaktoren für eine PVT ohne Leberzirrhose sind mannigfaltig und reichen von angeborenen Koagulopathien (z.B. Protein-S-, Protein-C-Mangel, Faktor-V-Leiden-Mutation, AT-III-Mangel etc.) über erworbene Koagulopathien und prothrombotische Dispositionen (myeloproliferative Erkrankungen, Antiphospholipid-Syndrom, orale Kontrazeptiva oder Malignome etc.) bis zu entzündlichen Erkrankungen im Abdomen (Pankreatitis, Divertikulitis, Cholezystitis, Appendizitis), die entweder aufgrund der lokalen Entzündung (Pankreatitis) oder einer Sepsis zu PVT führen können. Schließlich kann die PVT auch postoperativ/postinterventionell vor allem nach Splenektomie, Pankreasresektion, Lebertransplantation oder endoskopischer Sklerotherapie auftreten.1
Klinische Präsentation und Komplikationen
Die häufigsten Symptome sind abdominelle Schmerzen, Diarrhö und Erbrechen, wobei die PVT auch symptomlos verlaufen kann (und als Zufallsbefund bei einer Bildgebung aus anderen Gründen entdeckt wird). Bei Leberzirrhose ist die klinische Manifestation als Ösophagusvarizenruptur (aufgrund der Erhöhung des Pfortaderdrucks) nicht selten.
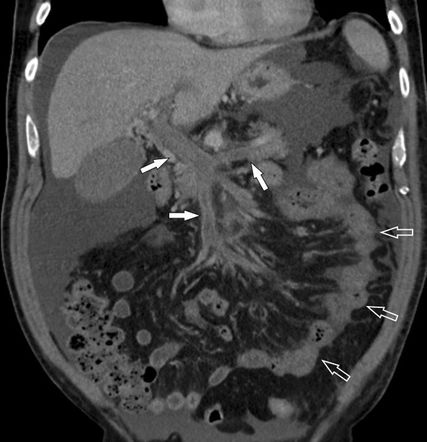
Abb. 6: Pfortader- und Mesenterialvenenthrombose: Die MDCT zeigt die ausgedehnte Thrombose (Pfeile oben) und den ischämischen, wandverdickten Dünndarm (offene Pfeile). In der Laparotomie fand sich eine Dünndarmnekrose
Die am meisten gefürchtete Komplikation bei Ausdehnung der PVT in die Mesenterialvenen ist das Auftreten einer hämorrhagischen Dünndarminfarzierung (Dünndarmnekrose) mit hoher Morbidität und Letalität (Abb. 6). Insgesamt sind bei Verdacht auf das Vorliegen einer Pfortaderthrombose die frühe bildgebende Diagnostik mittels farbcodierter Duplexsonografie und bei inkonklusiver Sonografie eine Kontrastmittel-verstärkte MDCT wichtig für das weitere therapeutische Management.
Literatur:
1 Anton A et al.: The pathophysiology of portal vein thrombosis in cirrhosis: getting deeper into Virchow’s triad. J Clin Med 2022; 11(3): 800 2 Cagin YF et al.: Incidence and clinical presentation of portal vein thrombosis in cirrhotic patients. Hepatobiliary Pancreat Dis Int 2016; 15(5): 499-503 3 Francoz C et al.: Portal vein thrombosis, cirrhosis, and liver transplantation. Hepatol 2012; 57(1): 203-12 4 Intagliata NM et al.: Diagnosis, development, and treatment of portal vein thrombosis in patients with and without cirrhosis. Gastroenterol 2019; 156(6): 1582-99.e1 5 Ogren M et al.: Portal vein thrombosis: prevalence, patient characteristics and lifetime risk: a population study based on 23,796 consecutive autopsies. World J Gastroenterol 2006; 12(13): 2115-9 6 Rajani R et al.: The epidemiology and clinical features of portal vein thrombosis: a multicentre study. Aliment Pharmacol Ther 2010; 32(9): 1154-62 7 Sobhonslidsuk A, Reddy KR: Portal vein thrombosis: a concise review. Am J Gastroenterol 2002; 97(3): 535-41 8 Yerdel MA et al.: Portal vein thrombosis in adults undergoing liver transplantation: risk factors, screening, management, and outcome. Transplantation 2000; 69(9): 1873-81 9 Zhang Y et al.: Prevalence and clinical significance of portal vein thrombosis in patients with cirrhosis and acute decompensation. Clin Gastroenterol Hepatol 2020; 18(11): 2564-72.e1
Das könnte Sie auch interessieren:
HBV-Reaktivierung unter Immunsuppression
Durch rezente Migrationsdynamiken befindet sich auch in Österreich die Prävalenz der Infektion mit dem Hepatitis-B-Virus (HBV) im Steigen. Besonders bei Patient:innen unter ...
OP-Freigabe bei Leberzirrhose
Patient:innen mit Leberzirrhose haben ein erhöhtes Risiko für Komplikationen und eine erhöhte Mortalität – daher muss eine detaillierte präoperative Evaluierung erfolgen. Es stehen ...
Die erste internationale multidisziplinäre MASLD-Leitlinie 2024
Die neue europäische Leitlinie zum Management der mit metabolischer Dysfunktion assoziierten steatotischen Lebererkrankung (MASLD) gibt detaillierte Empfehlungen zu Diagnose, Behandlung ...