Gynäkologische Tumoren
Autor:
Univ.-Prof. Dr. Alexander Reinthaller
Ordensklinikum Linz
Barmherzige Schwestern, Linz
Medizinische Universität Wien
E-Mail: alexander.reinthaller@gmail.com
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Wenn auch beim diesjährigen ASCO keine Studien präsentiert wurden, die die Praxis inder gynäkologischen Onkologie verändern, so brachten doch einige Studien sehr interessante Ergebnisse. Somit haben sie auch das Potenzial, in Zukunft die Praxis zubeeinflussen.
Endometriumkarzinom
Zum Endometriumkarzinom wurden die Langzeitdaten der SIENDO-Studie präsentiert. Diese Studie untersuchte bei Patientinnen mit fortgeschrittenem oder rezidiviertem Endometriumkarzinom den Einsatz von Selinexor, einem XPO1-Inhibitor. XPO1 exportiert wichtige Tumorsuppressorproteine inklusive des p53-Proteins aus dem Nucleus in das Zytoplasma, wodurch es zu einem Funktionsverlust dieser Tumorsuppressorproteine kommt. Im Gegensatz zu gesunden Zellen überexprimieren Tumorzellen XPO1. Dies führt zu einer Inaktivierung zum Beispiel des p53-Proteins durch Proteindegradation und damit zu einer Störung des Zellwachstums.
Selinexor inhibiert XPO1 und den Export von Tumorsuppressorproteinen, inklusive p53, wodurch die Funktion dieser Proteine wiederhergestellt wird. Damit wird die Zellzykluskontrolle reaktiviert und es kommt zum selektiven Zelltod von Tumorzellen, ohne dass gesunde Zellen beeinträchtigt werden.
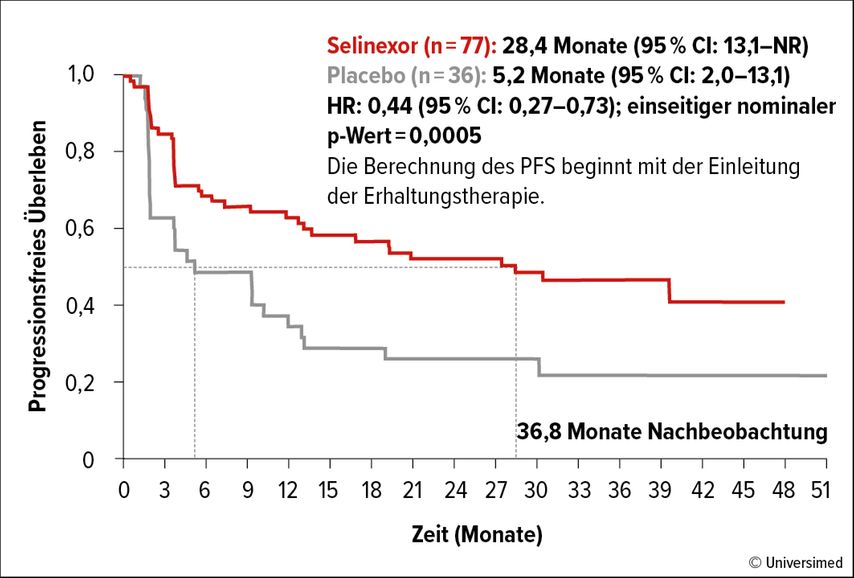
In die randomisierte, placebokontrollierte Studie wurden 263 Patientinnen mit fortgeschrittenem oder rezidiviertem Endometriumkarzinom eingeschlossen. Die Patientinnen konnten bereits eine Operation und/oder Strahlentherapie und auch eine endokrine Therapie erhalten haben. Es musste ein Tumoransprechen auf zumindest vier Zyklen Carboplatin und Taxol gegeben sein. Anschließend wurden die Patientinnen in die Selinexor- oder die Placebo-Gruppe randomisiert. Der primäre Studienendpunkt war das progressionsfreie Überleben (PFS) nach RECIST 1.1. Von besonderem Interesse war die Subgruppenanalyse der p53wt-Patientinnen, da eine Aktivität der Substanz nur bei intaktem p53-Protein zu erwarten ist. In der ersten Präsentation konnte in der „Intention to treat“(ITT)-Population bereits ein PFS-Vorteil für die Selinexor-Gruppe von 1,9 Monaten (HR: 0,705; CI: 0,499–0,996; p=0,024) gezeigt werden. Nun wurden die Langzeitdaten im Hinblick auf die p53wt-Patientinnen präsentiert. Hier zeigte sich ein signifikanter PFS-Vorteil dieser Subgruppe (HR: 0,44; CI: 0,27–0,73; p=0,0005), der sich auch in den molekularen Subgruppenanalysen im Hinblick auf eine „Mismatch repair“(MMR)-Defizienz widerspiegelte (Abb. 1). Beim Gesamtüberleben (OS) fand sich bei noch immaturen Daten in der p53wt-MMRp-Gruppe bereits jetzt bei einer Maturität von 34% ein signifikanter Unterschied zugunsten von Selinexor (HR: 0,48; CI: 0,22–1,07; p<0,03).
Fasst man diese Daten zusammen, so zeigt sich ein deutlicher PFS-Vorteil für die Selinexor-Erhaltungstherapie bei p53wt-Patientinnen, vor allem auch bei den MMRp-Patientinnen, für die bisher nur beschränkte Therapieoptionen zur Verfügung standen. Ermutigende Daten ergeben sich auch aus der ersten Gesamtüberlebensanalyse mit bereits jetzt einem signifikanten Vorteil im OS in der MMRp-Gruppe. Im Vergleich zu den vorangegangenen Daten zeigten sich hinsichtlich Toxizität keine neuen Sicherheitssignale. Die Daten unterstützen eine mögliche Rolle von Selinexor in der Erhaltungstherapie beim fortgeschrittenen/rezidivierten p53wt-Endometriumkarzinom. Derzeit läuft bei dieser Population die Phase-III-Folgestudie ENGOT-en20 mit Selinexor nach Chemotherapie bei p53wt-Patientinnen.
Zervixkarzinom
Zum Thema Zervixkarzinom wurde die Studie GOG-724 präsentiert. Die Phase-III-Studie untersuchte Patientinnen nach radikaler Hysterektomie mit Risikofaktoren (positive Lymphknoten und/oder Parametriuminfiltration und/oder positive Resektionsränder) und adjuvanter, konkomitanter Radiochemotherapie (CCRT) ± Brachytherapie alleine vs. adjuvante Chemotherapie nach CCRT. Insgesamt wurden 212 Patientinnen der FIGO-Stadien IA2, IB oder IIA nach radikaler Hysterektomie randomisiert. Arm 1 erhielt eine CCRT mit wöchentlichem Cisplatin ± Brachytherapie, Arm 2 eine CCRT mit wöchentlichem Cisplatin ± Brachytherapie gefolgt von Carboplatin und Paclitaxel. Es konnte weder im krankheitsfreien Überleben noch im Gesamtüberleben ein Unterschied zwischen den beiden Gruppen gefunden werden. Das Nebenwirkungsprofil in der Gruppe mit adjuvanter Chemotherapie nach CCRT war deutlich schlechter als in der Gruppe mit alleiniger CCRT. So fanden sich Nebenwirkungen der CTCAE-Grade ≥3 in 59% in der Chemotherapiegruppe versus 37% in der Gruppe mit alleiniger Strahlentherapie. Die Daten unterstützen auch die Ergebnisse der OUTBACK-Studie, in der Patientinnen mit lokal fortgeschrittenem Zervixkarzinom eine CCRT als definitive Therapie ± eine adjuvante Chemotherapie erhielten. Auch in dieser Studie, also bei Patienten ohne Operation, zeigte die Gruppe mit adjuvanter Chemotherapie keinen Vorteil.
Die Schlussfolgerungen aus dieser Studie sind demnach, dass die adjuvante Chemotherapie keinen Stellenwert in der Behandlung von Zervixkarzinomen sowohl nach primärer als auch nach adjuvanter CCRT hat.
Ovarialkarzinom
Zum Thema Ovarialkarzinom wurden drei interessante Studien präsentiert. Die CARACO-Studie untersuchte die therapeutische Wertigkeit einer systematischen pelvinen und paraaortalen Lymphadenektomie bei primärer Debulking-OP oder bei „Intervention debulking“-OP nach NACT (Tumorrest <1cm). 450 Patientinnen wurden in die Gruppen Chirurgie plus systematische Lymphadenektomie versus Chirurgie ohne systematische Lymphadenektomie randomisiert. Weder beim PFS noch beim OS (HR: 0,92; CI: 0,72–1,17; p=0,489) konnte zwischen beiden Gruppen ein Unterschied gezeigt werden.
Dies bestätigte die bereits 2017 publizierten Daten der LION-Studie, die die systematische Lymphadenektomie ausschließlich nach optimalem Debulking bei primärer zytoreduktiver Chirurgie untersuchte. In der CARACO-Studie wurde die Randomisierung durch die Publikation der LION-Studie erschwert, sodass die geplante Fallzahl nicht rekrutiert werden konnte. Insgesamt fehlten 29 Events. Auch wenn man diese Events alle zu der Gruppe der Patientinnen ohne Lymphadenektomie dazuzählte, war noch immer kein Unterschied im PFS und OS nachweisbar. Die Nebenwirkungen waren im Hinblick auf die Zahl der Bluttransfusionen, Blutverlust, Reinterventionen und Verletzungen der ableitenden Harnwege in der Gruppe mit Lymphadenektomie signifikant höher.
Somit kann man als Schlussfolgerung festhalten, dass nach optimalem Tumordebulking sowohl bei primärer Zytoreduktion wie auch beim „intervention debulking“ eine systematische Lymphadenektomie keinen Vorteil und damit auch keinen Stellenwert mehr hat.
Die zweite Phase-III-Studie, ENGOT-ov34, untersuchte Atezolizumab plus Bevacizumab plus Monochemotherapie beim fortgeschrittenen platinresistenten Rezidiv oder auch beim platinsensitiven Rezidiv, wenn es sich um das dritte Rezidiv handelte. Die Patientinnen wurden in zwei Gruppen randomisiert: Chemotherapie (PLD oder Paclitaxel) plus Bevacizumab plus Placebo versus Chemotherapie plus Bevacizumab plus Atezolizumab. Insgesamt wurden 550 Patientinnen randomisiert. Die primären Endpunkte waren PFS und OS. Es konnte kein Unterschied zwischen beiden Gruppen im Hinblick auf das PFS (HR: 0,87; CI: 0,73–1,04; p=0,12) und OS gezeigt werden. Diese Ergebnisse entsprechen den bislang publizierten Daten, wobei Checkpoint-Inhibitoren plus Bevacizumab oder auch plus PARPI bislang keinen Effekt gezeigt haben. Lediglich in der DUO-O-Studie, in der eine Triplekombination (CPI + BEV + Olaparib) zum Einsatz kam, zeigte sich für diese Kombination ein gewisser Vorteil.
Die dritte Phase-III-Studie war die SCORES-Studie, in der der VEGF-Antikörper Suvemcitug beim platinresistenten Ovarialkarzinom untersucht wurde. Es erfolgte eine 2:1-Randomisierung von 421 Patientinnen in den experimentellen Arm Suvemcitug plus Chemotherapie (Paclitaxel, PLD, Topotecan) versus den Kontrollarm Placebo plus Chemotherapie. Der primäre Endpunkt war das zentral bestimmte PFS. Sekundärer Endpunkt war unter anderem das OS. Beim PFS zeigte sich ein signifikanter Vorteil für Suvemcitug (HR: 0,60; CI: 0,53–0,60; p<0,0001). Beim OS konnte bei noch immaturen Daten bislang kein signifikanter Unterschied gezeigt werden. Die Daten bestätigen die in vorangegangenen Studien gezeigte Wirkung von Bevacizumab beim fortgeschrittenen Ovarialkarzinom, besonders auch beim platinresistenten Ovarialkarzinom (AURELIA-Studie).
Chemosensitivitätstestung
Eine weitere sehr interessante Studie untersuchte einen Chemosensitivitätstest mittels eines diagnostischen Krebsstammzell-Assays (ChemoID), um das Ansprechen auf die geplante Chemotherapie vorherzusagen. Genaue Details zum Test wurden aufgrund der kommerziellen Natur des Tests nicht bekannt gegeben.
Die Studie untersuchte 81 Patientinnen mit „high-grade“-serösem platinresistentem Ovarialkarzinom. Die Randomisierung erfolgte in einen Kontrollarm, in dem die Chemotherapie durch den behandelten Arzt festgelegt wurde, und in einen experimentellen Arm, in dem die Chemotherapie durch den ChemoID bestimmt wurde. Die Chemosensitivitätstestung erfolgte gegen alle in dieser Situation üblichen Chemotherapeutika (insgesamt 13 Mono- oder auch Kombinationschemotherapien). Der primäre Endpunkt war die Gesamtansprechrate. Sekundäre Endpunkte waren PFS und die Dauer des Ansprechens. Während in der Kontrollgruppe nur ein ausgesprochen geringes Ansprechen auf die vom Prüfarzt gewählte Chemotherapie erzielt werden konnte, zeigten die Patientinnen, bei denen der Sensitivitätstest durchgeführt wurde, ein signifikant höheres Ansprechen. So fand sich in der ChemoID-Gruppe bei 55% der Patientinnen ein Tumoransprechen, verglichen mit 5% in der Prüfarzt-Gruppe (p<0,0001). Die Dauer der Response war acht Monate in der ChemoID-Gruppe versus 5,5 Monate in der Prüfarzt-Gruppe (p<0,0001). Das mediane PFS in der ChemoID-Gruppe war elf Monate versus drei Monate in der Prüfarzt-Gruppe. Die „Clinical benefit“-Rate war 85% versus 24% (p<0,0001). Insgesamt zeigte diese Studie also eine beachtliche Verbesserung der Chemotherapie-Effektivität und des PFS bei platinresistentem Ovarialkarzinom nach Anwendung des ChemoID-Tests.
Literatur:
beim Verfasser
Das könnte Sie auch interessieren:
Adjuvantes Osimertinib reduziert ZNS-Rezidive bei EGFR-mutierter Erkrankung
Etwa 30% der Patienten mit nicht kleinzelligem Lungenkarzinom (NSCLC) präsentieren sich mit resezierbarer Erkrankung und werden einer kurativen Operation unterzogen. Viele Patienten ...
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
Aktualisierte Ergebnisse für Blinatumomab bei neu diagnostizierten Patienten
Die Ergebnisse der D-ALBA-Studie bestätigen die Chemotherapie-freie Induktions- und Konsolidierungsstrategie bei erwachsenen Patienten mit Ph+ ALL. Mit einer 3-jährigen ...