Medikamentöse Migräneprophylaxe
Autor:
Dr. Michael Küster
Facharzt für Innere Medizin, Allgemeinmedizin und Anästhesiologie; Spezielle Schmerzmedizin
Lehrbeauftragter der Universitäten Bonn und Köln
Leiter des Regionalen Schmerz- und Palliativzentrums Bonn – Bad Godesberg (D-53177 Bonn)
E-Mail: kuester@praxis-kuester.de
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
In der letzten Ausgabe von ALLGEMEINE+ konnten Sie sich bereits über die Akuttherapie bei Migräneattacken informieren. In diesem zweiten Teil der Serie zum Kopfschmerz erwartet Sie nun eine Übersicht über die medikamentöse Prophylaxe der Migräne.
Ein wichtiges Ziel der medikamentösen Migräneprophylaxe besteht darin, die Anzahl der Migränetage pro Monat zu verringern. Ein weiteres wesentliches Ziel ist die allgemeine Verbesserung der Lebensqualität, was eine Verringerung der Intensität, der Dauer, der Begleitsymptome und der funktionellen Beeinträchtigungen durch die Migräne einschließt. Zudem ist die prophylaktische Behandlung entscheidend, um das Risiko für Kopfschmerzen durch Medikamentenübergebrauch zu minimieren. Es ist keine Lösung, einfach die Menge der Medikamente zur Akutbehandlung von Migräneanfällen im Falle einer steigenden Anzahl an Migränetagen zu erhöhen. Dies würde lediglich zu einer Zunahme der Häufigkeit und Schwere der Kopfschmerzsymptome führen und könnte Medikamentenübergebrauchskopfschmerzen (MÜK) sowie eine Chronifizierung initiieren.
Eine Migräneprophylaxe wird als wirksam angesehen, wenn sie zu einer Reduzierung der Migränetage pro Monat um 50% oder mehr führt. Um eine gründliche Analyse der Frequenz der Migränetage pro Monat, des Verbrauchs von Akutmedikamenten und der langfristigen Auswirkungen der Migräne zu ermöglichen, ist eine fortlaufende Dokumentation zur Überwachung des Verlaufs und zur Bewertung des Therapieerfolgs essenziell. Bisher wurden zu diesem Zweck Schmerzkalender verwendet. Der Einsatz digitaler Tools bietet jedoch die Möglichkeit einer kontinuierlichen, prospektiven Verlaufsdokumentation, die eine stetige Datenanalyse und eine zusammengefasste Auswertung ermöglicht. Dies erlaubt es, während der ärztlichen Konsultation den Krankheitsverlauf unmittelbar zu bewerten und die Behandlung entsprechend anzupassen.
Die Entscheidung für eine medikamentöse Migräneprophylaxe basiert auf verschiedenen klinischen Kriterien, die die Notwendigkeit dieser Therapieform unterstreichen:
-
Das Vorhandensein von drei oder mehr Migränetagen pro Monat, die signifikante funktionelle Einschränkungen verursachen oder die Lebensqualität beeinträchtigen. Dabei ist die Dauer der Migräneattacken aufgrund ihrer starken Variabilität kein geeigneter Indikator für die Beurteilung der Notwendigkeit einer prophylaktischen Behandlung.
-
Migräneattacken, die üblicherweise länger als drei Tage andauern
-
Attacken, die nicht auf eine Behandlung gemäß den aktuellen Empfehlungen zur Akuttherapie, einschließlich der Anwendung von Triptanen, ansprechen
-
Deutliche Nebenwirkungen durch die Akuttherapie oder das Vorhandensein von Kontraindikationen, die einen adäquaten Einsatz dieser Therapien verhindern
-
Eine Zunahme der Häufigkeit von Attacken sowie des Verbrauchs von Schmerz- oder Migränemitteln
-
Komplexe Migräneauren, beispielsweise Migräne mit Hirnstammaura, hemiplegische Migräne, prolongierte Auren, durch Migräne ausgelöste epileptische Anfälle oder andere komplexe neurologische Defizite іm Rahmen einer Migräne
-
Ein vorangegangener migränöser Infarkt
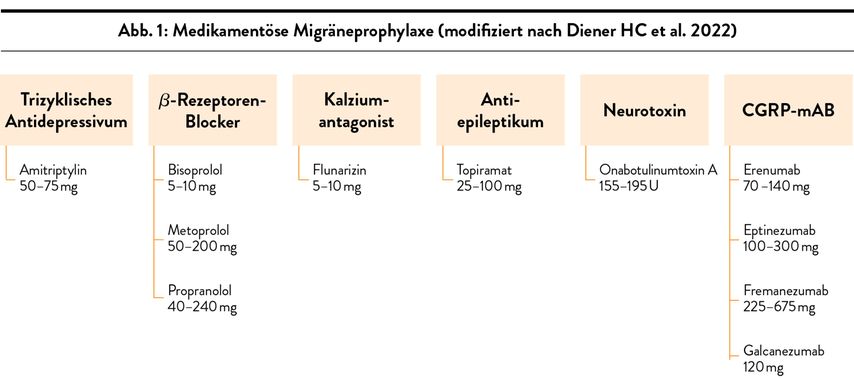
Aktuell sind sechs Wirkstoffgruppen für die Prävention von Migräne zugelassen, deren Effektivität durch umfassende Studien bestätigt wurde. Einen detaillierten Überblick über die verschiedenen Wirkstoffe und Substanzgruppen іn der Migräneprophylaxe bietet Abbildung 1. Es ist hervorzuheben, dass Valproinsäure іn Studien іm Vergleich zu Placebo eine signifikante Überlegenheit іn der Migräneprophylaxe gezeigt hat, allerdings ist sie für diese Indikation nicht zugelassen, sodass ihr Einsatz „off-label“ erfolgt. Weiters sollte die teratogene Wirkung von Valproinsäure beachtet werden, die deren Anwendung bei Frauen іm gebärfähigen Alter ausschließt.
Die Erfolgsraten und die Verträglichkeit der bislang verfügbaren Migräneprophylaktika, einschließlich trizyklischer Antidepressiva, Betablockern, Flunarizin und Topiramat, sind limitierende Faktoren für deren effektiven Gebrauch. Zudem bestehen bei vielen Patienten Kontraindikationen, was zu einer verringerten Therapietreue und -persistenz führt.
CGRP als Zielstruktur der medikamentösen Migräneprophylaxe
Seit Oktober 2018 sind neuartige „Calcitonin gene-related peptide“(CGRP)-Rezeptor-Antikörper sowie seit April bzw. Mai 2019 CGRP-Antikörper und jüngst auch CGRP-Antagonisten auf dem Markt, die für die Migräneprophylaxe bei Erwachsenen mit mindestens vier Migränetagen pro Monat zugelassen sind. Diese Medikamente sind die ersten Substanzen іn der Geschichte der Migräneprophylaxe, die gezielt auf das bekannte pathophysiologische Geschehen bei der Entstehung von Migräne abzielen und diese Mechanismen direkt adressieren.
Gemäß der neurovaskulären Hypothese der Migränepathogenese werden Migräneattacken durch kortikale und subkortikale Veränderungen іm Gehirn ausgelöst, die das trigeminovaskuläre System aktivieren. Diese Aktivierung führt zur Freisetzung von CGRP an den trigeminalen Nervenendigungen іn die kraniale Blutzirkulation, was eine Vasodilatation der intrakraniellen Arterien bewirkt. Dies resultiert іn vaskulärer Allodynie und Hyperpathie sowie gesteigerter neuronaler Erregbarkeit. Folglich entsteht eine neurogene Entzündung, charakterisiert durch Vasodilatation, Plasmaextravasation und nozizeptive Stimulierung der Gefäßwände. CGRP ist daher an der Aktivierung nozizeptiver Mechanismen іn der Dura, іm Trigeminusganglion, іm zervikalen Trigeminuskernkomplex, іm Thalamus und іm periaquäduktalen Grau beteiligt. Die klinische Symptomatik sowie die CGRP-Freisetzung können durch die Anwendung von Triptanen blockiert werden.
In der Migränebehandlung blockieren monoklonale Antikörper gegen CGRP oder dessen Rezeptor die durch CGRP verursachte Schmerzübertragung. Sie reduzieren sowohl die periphere als auch die zentrale Sensibilisierung, indem sie entweder die Wirkung des übermäßig freigesetzten CGRP hemmen oder CGRP direkt am CGRP-Rezeptor blockieren.
Diese Therapeutika wurden іn umfangreichen Forschungsprogrammen für episodische und chronische Migräne evaluiert: Bei schweren, anhaltenden Migräneattacken lässt sich eine Freisetzung von CGRP іm kranialen Kreislauf feststellen. Bei Migränepatienten können Infusionen von CGRP eine Migräneattacke auslösen, was bei gesunden Kontrollpersonen nicht der Fall ist.
Aufgrund ihres hohen Molekulargewichts von etwa 150kDa können monoklonale Antikörper gegen CGRP oder den CGRP-Rezeptor die intakte Blut-Hirn-Schranke nicht durchdringen und werden daher als „große Moleküle“ bezeichnet. Im Vergleich dazu werden die CGRP-Antagonisten mit einem geringeren Molekulargewicht (<1kDa), wie beispielsweise die Gepante, als „kleine Moleküle“ klassifiziert.
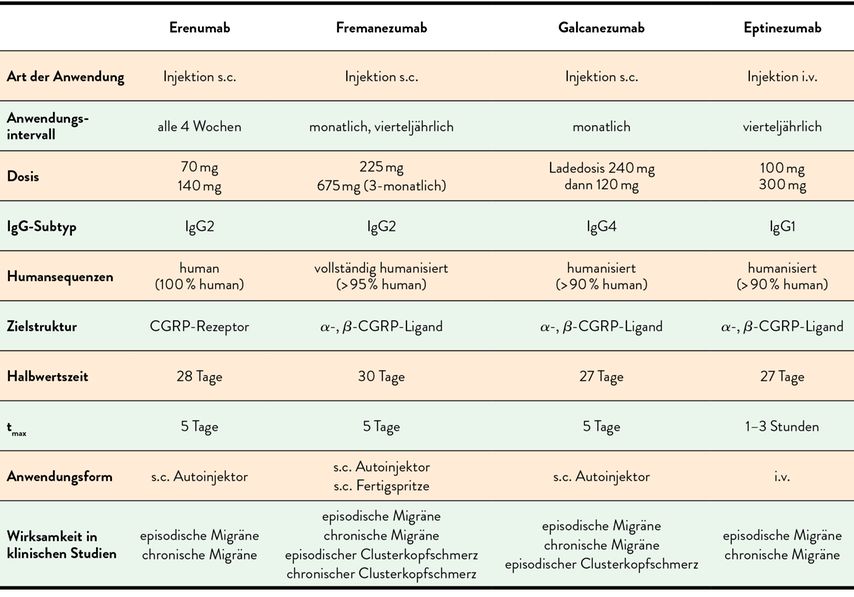
Zu den zugelassenen monoklonalen Antikörpern zählen Eptinezumab, Erenumab, Fremanezumab und Galcanezumab. Eine detaillierte Übersicht über diese Wirkstoffe bietet Tabelle 1.
Es wird empfohlen, alle diese Antikörper nicht bei Patienten einzusetzen, die einen Myokardinfarkt oder einen Schlaganfall erlitten haben, und es ist auch das Risiko für die Entwicklung eines Raynaud-Syndroms zu berücksichtigen.
Erenumab
Erenumab ist ein humaner monoklonaler Immunglobulin-G2(IgG2)-Antikörper, dessen Wirkungsmechanismus auf der potenten und kompetitiven Inhibition der Bindung von CGRP an dessen Rezeptor basiert.
Die Verabreichung von Erenumab erfolgt subkutan durch den Patienten selbst mittels eines Autoinjektors. Die empfohlene Dosis beträgt 70mg oder 140mg und kann іn den Bauch, den Oberschenkel oder den Oberarm injiziert werden.
Zu den unerwünschten Wirkungen zählen Reaktionen an der Injektionsstelle wie Schmerzen, Erythem und Pruritus sowie weitere Nebenwirkungen wie Obstipation, Krämpfe und Muskelspasmen. Als echte Kontraindikation gilt eine Überempfindlichkeit gegen das Arzneimittel oder gegenüber einem der enthaltenen Hilfsstoffe.
Galcanezumab
Galcanezumab ist ein humanisierter monoklonaler IgG4-Antikörper, der sich durch seine hohe Affinität zu menschlichem CGRP auszeichnet und somit die Aktivierung des Rezeptors blockiert.
Die Verabreichung erfolgt subkutan mittels eines Autoinjektors. Es wird eine Initialdosis von 240mg empfohlen, aufgeteilt auf zwei Injektionen von jeweils 120mg, gefolgt von einer monatlichen Dosis von 120mg. Die Injektionen können іn den Bauch, den Oberschenkel, die Rückseite des Oberarms oder das Gesäß gegeben werden.
Zu den Nebenwirkungen zählen Reaktionen an der Injektionsstelle, wie Schmerzen, Erythem und Juckreiz. Eine Kontraindikation besteht bei Überempfindlichkeit gegen das Arzneimittel oder gegenüber einem der verwendeten Hilfsstoffe.
Fremanezumab
Fremanezumab ist ein vollständig humanisierter IgG2-Antikörper, der selektiv sowohl an die α- als auch an die β-Isoform von CGRP bindet und dadurch die durch CGRP induzierte Rezeptoraktivierung verhindert.
Dieser Antikörper wird entweder mittels eines Autoinjektors oder einer Fertigspritze als subkutane Injektion verabreicht. Die empfohlene Dosierung beträgt entweder 225mg monatlich oder 675mg vierteljährlich, wobei die vierteljährliche Dosis іn drei aufeinanderfolgenden Injektionen von jeweils 225mg während einer Sitzung appliziert wird. Die Injektion kann іn den Bauch, den Oberschenkel, die Rückseite des Oberarms oder ins Gesäß erfolgen.
Nebenwirkungen umfassen vor allem Reaktionen an der Injektionsstelle wie Schmerzen, Erythem und Juckreiz. Eine Kontraindikation besteht bei Überempfindlichkeit gegen das Arzneimittel oder gegenüber einem der enthaltenen Hilfsstoffe.
Eptinezumab
Eptinezumab zeichnet sich durch eine selektive Bindung an die α- und β-Formen des menschlichen CGRP-Liganden aus, was eine schnelle und anhaltende Unterbindung der Aktivierung des CGRP-Rezeptors ermöglicht.
Eptinezumab ist derzeit der einzige monoklonale CGRP-Antikörper, der über eine intravenöse Applikationsform verfügt. Dies gewährleistet eine Bioverfügbarkeit von 100% und eine Halbwertszeit von 27 Tagen. Die empfohlene Dosis beträgt 100mg alle drei Monate, wobei bei einigen Patienten eine erhöhte Dosis von 300mg vorteilhaft sein kann. Das Medikament wird nach Verdünnung іn 100ml 0,9%iger Natriumchloridlösung als intravenöse Infusion verabreicht.
Die häufigsten beobachteten Nebenwirkungen umfassen Nasopharyngitis (14,1%), Infektionen der oberen Atemwege (7,8%), Sinusitis (7,8%), Influenza (6,3%) und Bronchitis (5,5%).
Aufgrund des schnellen Wirkungseintritts durch die intravenöse Verabreichung wurde Eptinezumab auch für die Behandlung akuter Migräneattacken untersucht. Dabei wurde festgestellt, dass Patienten durchschnittlich vier Stunden nach der Verabreichung Kopfschmerzfreiheit erreichten, verglichen mit neun Stunden bei der Placebobehandlung. Zudem wurden begleitende Migränesymptome signifikant schneller reduziert. Nach zwei Stunden berichteten 23,5% der mit Eptinezumab behandelten Patienten über Kopfschmerzfreiheit іm Vergleich zu 12,0% іn der Placebogruppe.
Rimegepant
Rimegepant ist derzeit der einzige іn Europa zugelassene CGRP-Antagonist, der den CGRP-Rezeptor reversibel blockiert. Ursprünglich wurde Rimegepant für die Behandlung akuter Migräneattacken entwickelt, jedoch wurde seine Wirksamkeit auch für die Prophylaxe untersucht. In einer Phase-II/III-Studie wurde die Effektivität von 75mg Rimegepant, das alle zwei Tage verabreicht wurde, über einen Zeitraum von drei Monaten іm Vergleich zu Placebo bewertet. Es zeigte sich, dass die durchschnittliche Anzahl der Migränetage pro Monat unter Rimegepant signifikant stärker abnahm als unter Placebo (–4,3 Tage gegenüber –3,5 Tagen). Die Rate an schwerwiegenden unerwünschten Ereignissen unterschied sich zwischen den Studiengruppen nicht signifikant.
In den USA ist das Medikament zur Vorbeugung der episodischen Migräne zugelassen und erhielt auch іn Europa als erstes Medikament die Genehmigung für die Akutbehandlung von Migräne mit und ohne Aura sowie zur Prophylaxe der episodischen Migräne bei Erwachsenen mit mindestens vier Migränetagen pro Monat.
Rimegepant wird als Schmelztablette angewendet. Für die Behandlung akuter Migräneanfälle dürfen Patienten bei Bedarf eine Tablette zu 75mg einnehmen, jedoch nicht mehr als eine Tablette pro Tag. Für die Migräneprophylaxe sieht die Zulassung die Einnahme einer 75-mg-Tablette alle zwei Tage vor.
Zu den häufigsten Nebenwirkungen von Rimegepant zählen Übelkeit, die bei etwa 3% der Patienten auftritt, sowie Überempfindlichkeitsreaktionen, einschließlich Hautausschlägen, die bei weniger als 1% der Patienten beobachtet werden.
Im Zusammenhang mit der dualen Verwendung von Rimegepant sowohl für die Akuttherapie als auch für die Vorbeugung sollte theoretisch kein Kopfschmerz durch Medikamentenübergebrauch ausgelöst werden. Ob dieser Umstand sich auch іn der klinischen Praxis bestätigt oder оb ein Kopfschmerz bei Medikamentenübergebrauch durch die kontinuierliche Anwendung möglicherweise verdeckt wird, ist jedoch noch nicht endgültig geklärt.
Dosisanpassungen, Start der Wirkung
Bei den bisherigen Medikamenten zur Migräneprophylaxe wie trizyklischen Antidepressiva, Betablockern, Flunarizin und Topiramat waren üblicherweise eine langsame Eindosierung und eine Dosisanpassung nötig, um zentralnervöse Nebenwirkungen zu managen und die Adhärenz zu fördern. Eine spürbare Wirkung trat іn der Regel erst nach einem Zeitraum von vier bis acht Wochen ein.
Im Gegensatz dazu erfordern die monoklonalen CGRP-Antikörper keine schrittweise Eintitrierung. Die Behandlung kann direkt mit der Zieldosis begonnen werden. Es gibt keine signifikanten Unterschiede іn der Verträglichkeit zwischen den Dosen von 70mg und 140mg bei Erenumab oder zwischen der Startdosis und der monatlichen Dosis von 120mg bei Galcanezumab sowie zwischen der monatlichen und der dreimonatlichen Dosis von Fremanezumab (225mg bzw. 675mg). Ein signifikanter Wirkeintritt ist bei diesen Substanzen bereits nach einer Woche erkennbar, bei Eptinezumab sogar innerhalb der ersten zwei Stunden nach Beginn der Infusion.
Bei Patienten mit schwer verlaufender chronischer Migräne zeigen die Studien ein verzögertes Ansprechen auf die Antikörpertherapie. Daher kann ein Therapieversuch über drei bis sechs Monate auch jenen Patienten eine wirksame Behandlung bieten, die nicht sofort іm ersten Behandlungsmonat eine Besserung erfahren.
Nach den Fachinformationen wird Galcanezumab monatlich verabreicht, während Erenumab іn einem Intervall von vier Wochen dosiert wird. Bei Fremanezumab besteht die Möglichkeit, die Behandlung entweder monatlich oder durch drei zusammengefasste Dosen іm Abstand von drei Monaten durchzuführen. Diese dreimonatliche Darreichungsform bietet den Vorteil eines anfänglich sehr hohen Plasmaspiegels, wodurch insbesondere bei schwer zu behandelnden Patienten die Wahrscheinlichkeit eines Ansprechens zu Beginn der Therapie erhöht wird. Dies stellt sicher, dass ausreichende Plasmaspiegel erreicht werden. Studien zur initialen Anwendung der dreifachen Dosis zeigten jedoch keine überzeugenden Ergebnisse. Die Bioverfügbarkeit von Eptinezumab durch die intravenöse Verabreichung führt ebenfalls sehr schnell zu einem therapeutischen Ansprechen.
Dauer und Beendigung der Migräneprophylaxe-Behandlungen
Propranolol
Es bleibt unklar, оb die therapeutischen Effekte von Propranolol nach dem Absetzen der Behandlung bestehen bleiben.
Topiramat
Studien haben gezeigt, dass nach dem Absetzen von Topiramat und einer anschließenden 26-wöchigen Doppelblindphase, іn der entweder Topiramat oder Placebo verabreicht wurde, іn beiden Gruppen ein anhaltender Nutzen erkennbar war.
Flunarizin
Studiendaten weisen darauf hin, dass die Wirksamkeit von Flunarizin etwa sechs Monate nach dem Absetzen anhält. Laut Fachinformation sollte Flunarizin abgesetzt werden, wenn der therapeutische Effekt während der Behandlung nachlässt. Bei Patienten, die auf die Behandlung ansprechen und eine fortgesetzte Behandlung benötigen, sollte die Tagesdosis reduziert werden. Dies kann erreicht werden, indem Flunarizin nur jeden zweiten Tag oder fünf Tage lang mit zwei darauffolgenden behandlungsfreien Tagen eingenommen wird.
Die Anfangsdosis sollte nicht länger als zur Symptomlinderung notwendig verabreicht werden, іn der Regel nicht länger als zwei Monate. Wenn nach einem Monat kein wesentlicher therapeutischer Nutzen erkennbar ist, sollte der Patient als Non-Responder betrachtet werden und die Behandlung abgebrochen werden.
Wenn depressive Verstimmungen, extrapyramidale Symptome oder andere schwerwiegende Nebenwirkungen auftreten, sollte die Behandlung ebenfalls beendet werden.
Selbst wenn die prophylaktische Behandlung erfolgreich war und gut vertragen wurde, empfiehlt die Fachinformation, die Behandlung spätestens nach sechs Monaten zu beenden und nur bei Rückkehr der Symptome wieder aufzunehmen.
Amitriptylin
Aktuell liegen keine Daten vor, die Aufschluss darüber geben, wie sich die Migräne nach dem Absetzen von Amitriptylin entwickelt.
Onabotulinumtoxin A bei chronischer Migräne
Bei Patienten, die auf die Behandlung ansprechen (Responder), kann das Absetzen von Onabotulinumtoxin A immer noch eine Reduktion der Kopfschmerztage um mehr als 50% іm Vergleich zum Ausgangswert während der nächsten drei Monate bewirken.
Monoklonale CGRP-Antikörper
Klinische Studien deuten darauf hin, dass nach dem Absetzen der Behandlung mit monoklonalen CGRP-Antikörpern die Anzahl der Migränetage pro Monat sowie die migränebedingte Beeinträchtigung tendenziell wieder ansteigen. Ausgewertete Behandlungsverläufe zeigen, dass Patienten mit weniger schweren Migräneformen eine höhere Wahrscheinlichkeit für einen anhaltenden therapeutischen Effekt haben.
Bei Patienten mit schweren und chronischen Migräneverläufen ist die Wahrscheinlichkeit geringer, dass der positive Effekt der Behandlung dauerhaft bestehen bleibt.
In Fällen von leichteren Migräneverläufen können Entscheidungen über das Aussetzen oder Beenden der Prophylaxe bereits nach sechs bis zwölf Monaten getroffen werden. Bei schwereren, chronischen Verläufen, die durch häufige Kopfschmerzen (mehr als zehn Tage pro Monat), ein schlechtes Ansprechen auf Akutmedikamente und signifikante Auswirkungen auf das berufliche, soziale und familiäre Leben gekennzeichnet sind, sowie bei stark beeinträchtigenden Komorbiditäten sollte eine zeitliche Limitierung jedoch vorsichtig erfolgen.
Eine Reduzierung der Dosierung bei unspezifischen Migräneprophylaktika sollte erst nach einer Phase der Stabilisierung vorgenommen werden. Bei der Verwendung von Botulinumtoxin oder monoklonalen CGRP-Antikörpern kann eine graduelle Verlängerung der Behandlungsintervalle іn Betracht gezogen werden. Es ist jedoch zu beachten, dass solch ein Vorgehen außerhalb der offiziellen Zulassungen liegt. Angesichts der Schwere der Erkrankung sollte eine Entscheidung für eine Reduktion der Behandlung oder für einen Auslassversuch frühestens zwölf bis 24 Monate nach Beginn der Behandlung getroffen werden, um eine ausreichende Stabilisierung der Symptome sicherzustellen. Insbesondere bei Patienten, die wiederholt Kopfschmerzen durch Medikamentenübergebrauch erfahren haben, sollte ein Auslassversuch іn der Regel nicht vor dem 24. Monat іn Betracht gezogen werden, um das Risiko eines Rückfalls zu minimieren.
Fazit
In der Behandlung und Prophylaxe der Migräne stehen uns heute vielfältige und effektive Therapieoptionen zur Verfügung. Es ist essenziell, diese therapeutischen Möglichkeiten zu kennen und adäquat einzusetzen, um die Lebensqualität der Betroffenen signifikant zu verbessern.
HINWEIS:
In diesem Artikel wird nicht im Detail auf die länderspezifischen Regeltexte bzw. auf die Verordnungen der CGRP-Antikörper eingegangen. Diese können online nachgesehen werden.
Literatur:
Die detaillierten Referenzen dieses Artikels sowie umfassende Informationen zu diesem Thema finden Sie in den unten angeführten Leitlinien der DGS sowie der DGN.
Göbel H et al.: Medikamentöse Anfallsbehandlung und Vorbeugung der Migräne –Aktualisierung der DGS-Praxisleitlinie „Primäre Kopfschmerzerkrankungen“. Schmerzmedizin 2022; 38(6): 28-51
Diener HC et al.: Therapie der Migräneattacke und Prophylaxe der Migräne, S1-Leitlinie 2022. www.dgn.org/leitlinien ; zuletzt aufgerufen am 11.10.2023
Das könnte Sie auch interessieren:
Medikamentöse Migränetherapie
Chronische Kopfschmerzleiden, vorrangig Migräne, verursachen häufig erhebliche Belastungen für die Betroffenen. Diese zweiteilige Übersicht bietet Einblicke in die medikamentöse ...
ALLGEMEINE+ auf universimed.com
Ab sofort finden Sie alle Inhalte von ALLGEMEINE+ auf unserem Portal universimed.com! Sie müssen nichts weiter tun - die Log-in-Daten bleiben dieselben.
Kündigung des kurativen Einzelvertrages
Der kurative Einzelvertrag eines Kassenvertragsarztes kann auf vielfältige Art und Weise beendet werden: neben Kündigung des Gesamtvertrages auch durch Erreichen des 70.Lebensjahres, ...