Welche Rolle spielt das Mikrobiom?
Autorinnen:
PD Dr.med. Verena Bossung, MHBA, IBCLC
Dr.med. Franziska Krähenmann
Klinik für Geburtshilfe
Universitätsspital Zürich
E-Mail: verena.bossung@usz.ch
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Die Mastitis ist eine entzündliche Erkrankung der Milchdrüse, häufig durch bakterielle Infektionen bedingt. Das Brustmilchmikrobiom beeinflusst die Pathogenese massgeblich, da Dysbiosen die Kolonisation pathogener Keime begünstigen. Präventions- und Therapieoptionen umfassen Probiotika und gezielte antibiotische Strategien.
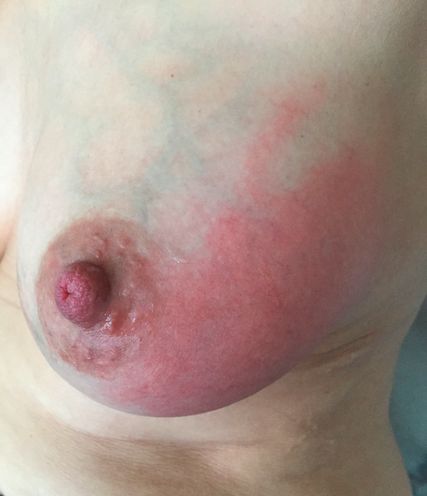
Abb. 1: Symptome einer Mastitis umfassen u.a. Schmerzen, Rötung oder Überwärmung der Brust
Eine Laktationsmastitis ist eine häufige Komplikation in der Stillzeit und führt nicht selten sogar zum vorzeitigen Abstillen. Bis zu einem Viertel aller stillenden Frauen sind von Mastitissymptomen betroffen. Am häufigsten tritt eine Mastitis in den ersten vier bis sechs Wochen nach Stillbeginn auf.1 Sie ist gekennzeichnet von ein- oder beidseitigen Lokalsymptomen der Brust wie Schmerzen, Rötung oder Überwärmung (Abb. 1) und ist bei fortgeschrittenen Formen mit systemischen Symptomen wie Fieber, Grippegefühl, Gliederschmerzen oder Kopfschmerzen kombiniert. Das Protokoll Nummer 36 der Academy of Breastfeeding Medicine (ABM) spricht von einem Mastitisspektrum.2 Das Spektrum umfasst die Begriffe Milchstau, subakute Mastitis, inflammatorische Mastitis, infektiöse Mastitis, Abszess und Phlegmone. Entsprechend gibt es frühe Mastitisformen, die selbstlimitierend sind, und auf der anderen Seite schwere Verläufe, welche eine stationäre Behandlung mit intravenöser antibiotischer Therapie notwendig machen. Eine bakterielle Laktationsmastitis wird durch das gleiche Spektrum an Bakterien verursacht, welche auch zum physiologischen Brustmilchmikrobiom (BMM) gehören. Insbesondere die Bakteriengattungen (Genera) Staphylococcus wie Staphylococcus aureus und Staphylococcus epidermidis oder Streptococcus sind Haupterreger. Daher kann es nicht die Anwesenheit dieser Bakterien allein sein, die eine Mastitis verursacht. Vielmehr entstehen Erkrankungen des Mastitisspektrums durch ein Zusammenspiel mehrerer Risikofaktoren aufseiten der Frau («host»), des Mikrobioms oder durch äussere Einflüsse. Das Mastitisspektrum folgt in seiner Entstehung häufig einer gewissen Reihenfolge. Bevor diese näher beschrieben wird, soll auf die Grundlagen des BMM näher eingegangen werden.
Das Brustmilchmikrobiom
Als Mikrobiota wird die Gesamtheit aller Mikroorganismen (Bakterien, Viren, Pilze und Co.) in einer Umgebung bzw. Körperregion bezeichnet. Das Mikrobiom ist das gesamte Habitat einer Körperregion, also die Mikrobiota inklusive ihrer Gene, Stoffwechselprodukte und Umweltbedingungen. Viele Schleimhäute und Körperoberflächen haben ihr eigenes charakteristisches Mikrobiom, wie etwa das Darmmikrobiom. Es ist wichtig zu verstehen, dass aktuell der Grossteil des menschlichen Mikrobioms nicht kultivierbar ist. Hierfür sind molekulargenetische Methoden erforderlich, die weitestgehend noch keine Rolle in der klinischen Routinediagnostik spielen. In den in der Klinik üblichen mikrobiologischen Kulturen, z.B. aus einem Muttermilchabstrich, wird nur ein kleiner Teil des gesamten Mikrobioms abgebildet.
Zum BMM gehören Bakterien, Viren, Hefen und Pilze sowie Protozoen (Urtierchen) und Archaea (einzellige Mikroorganismen ohne Zellkern). Auch wenn es individuelle Unterschiede im Aufbau des BMM gibt, werden bestimmte Mikroorganismen immer wieder nachgewiesen. Eine grosse Metaanalyse konnte mehr als 800 Spezies in Muttermilchproben sowie Brustbiopsien nachweisen.3 Zu den häufigsten gehörten Staphylococcus aureus, Staphylococcus epidermidis,Streptococcus agalactiae,Cutibacterium acnes, Enterococcus faecalis,Bifidobacterium breve, Escherichia coli,Streptococcus sanguinis, Lactobacillus gasseri und Salmonella enterica. Per Bakterienkultur konnten nur 24% der Bakterien in Biopsien und 38% in Muttermilch nachgewiesen werden, mit molekularen Methoden dagegen 85% in Biopsien und 88% in Muttermilch. Dies zeigt, dass die Kombination beider Methoden für eine umfassende Diagnostik am besten geeignet ist. In einer anderen Arbeit, die das BMM in Proben aus elf Ländern weltweit untersuchte, waren die Genera Staphylococcus und Streptococcus in ca. 98% der Muttermilchproben vorhanden.4 Die Genera Propionibacterium, Bifidobacterium, Veillonella, Rothia und Lactobacillus werden häufig als Bestandteil des BMM berichtet. Zudem gehören Corynebacterium, Ralstonia, Acinetobacter, Acidovorax, Pseudomonas, Bacteroides, Clostridium, Escherichia/Shigella, Gemella und Enterococcus zu den Bakterien, die dem BMM zugeschrieben werden, wobei das sogenannte «Kernmikrobiom» der Muttermilch unterschiedlich definiert wird.5
Die meisten Viren des BMM (95%) zählen zu den Bakteriophagen, also Viren, welche Bakterien infizieren. Ihre Anzahl im BMM ist insbesondere in den ersten Lebenstagen hoch. Ein Befall mit einem Bakteriophagen kann entweder den Tod des Bakteriums bedeuten oder die Viren integrieren ihre Gene in das Bakteriengenom, sodass dieses sich verändert und neue Funktionen erlangt. Die Bakteriophagen werden häufig gemeinsam mit den entsprechenden Bakterien von der Mutter auf das gestillte Kind übertragen und können im kindlichen Darm nachgewiesen werden. Dazu zählen Myoviridae, Siphoviridae und Podoviridae. Zu den Viren des BMM, welche menschliche Zellen befallen (eukaryote Viren), gehören etwa Herpesviridae, Poxviridae,Mimiviridae und Iridoviridae. Für das Zytomegalievirus, das zu den Herpesviren gehört, ist seit Langem bekannt, dass es als Bestandteil des BMM auf das Neugeborene übertragen werden kann.6
Zu den Hefen und Pilzen des BMM (Mykobiom) zählen Malassezia, Davidiella, Ascomycota,Candida und Saccharomyces. Über das Stillen können diese den kindlichen Darm besiedeln. Auch das Vorkommen von Protozoen in Muttermilch wird in der Literatur berichtet, z.B. Toxoplasma gondii und Giardia intestinalis, es bleibt aber unklar, wie weit verbreitet ihr Vorkommen im BMM ist. Archaea sind nicht kultivierbar und konnten bereits in Muttermilch nachgewiesen werden. Beim Menschen findet man sie ansonsten im Darm, in der Mundhöhle oder der Vagina. Sie sind keine Krankheitserreger. Ihre Rolle im BMM und im kindlichen Darm ist heute noch unklar.5
Woher stammt das Brustmilchmikrobiom?
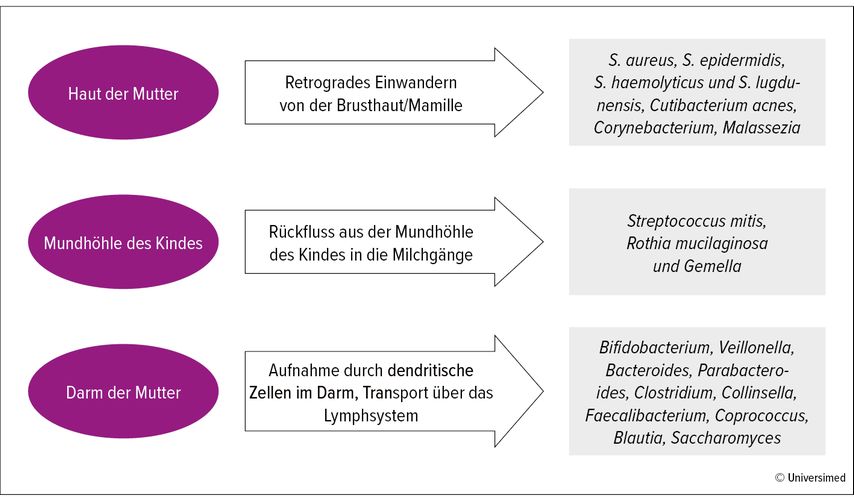
Aktuelle Untersuchungen legen nahe, dass es drei Hauptquellen für das BMM gibt (Abb. 2). Es wird davon ausgegangen, dass Mikroorganismen der Brusthaut bzw. der Mamille retrograd in die Milchgänge und das Brustgewebe gelangen. Das BMM enthält viele Mikroorganismen des Hautmikrobioms, darunter viele Bakterien der Gattungen Staphylococcus, wie Staphylococcus aureus, Staphylococcus epidermidis, Staphylococcus hominis, Staphylococcus haemolyticus und Staphylococcus lugdunensis. Auch Cutibacterium acnes und Bakterien der Gattung Corynebacterium werden häufig im BMM gefunden. Der Pilz Malassezia ist zudem Bestandteil des Hautmykobioms und auch im BMM zu finden. Zudem besteht während des Stillens ein enger Kontakt zwischen der kindlichen Mundhöhle und dem dortigen Mikrobiom und der Brustdrüse. Es ist bekannt, dass es während des Stillens auch zu einem Rückfluss von Milch aus dem Mund in die Milchgänge kommt. Typische Mikroorganismen der Mundhöhle werden regelmässig im BMM nachgewiesen, wie z.B. Streptococcus salivarius, Streptococcus mitis,Rothia mucilaginosa und Gemella spp. Natürlich ist es auch umgekehrt so, dass das BMM die kindliche Mundhöhle besiedelt. Zusätzlich wird ein enteromammärer Übertragungsweg vermutet, bei dem dendritische Zellen des Immunsystems im mütterlichen Darm lebendige Bakterien aufnehmen und diese über das lymphatische System bis ins Brustgewebe gelangen. So sind typische Darmbakterien, aber auch Hefen und Pilze Bestandteil des BMM. Hierzu zählen die Anaerobier der Gattungen Bifidobacterium, Veillonella,Bacteroides,Parabacteroides,Clostridium, Collinsella, Faecalibacterium, Coprococcus und Blautia sowie der Pilz Saccharomyces. Warum nur manche Bakterien diesen Weg nehmen, andere dagegen selten bis nie im Brustgewebe nachgewiesen werden, ist bis heute unklar. Die Besiedelung der Brustdrüse scheint auch ausserhalb der Stillzeit stattzufinden. In Gewebeproben von Frauen, die nicht stillen oder sogar noch nie schwanger waren, wurden Mikroorganismen nachgewiesen, allerdings in geringer Zahl. Auch das Kolostrum von Schwangeren vor der Geburt hat bereits ein Mikrobiom. Mit dem Stillbeginn und dem Kontakt zur kindlichen Mundhöhle sowie der regelmässigen Entleerung von Milch aus der Brust verändert sich das Mikrobiom. Trotzdem wird die Frage diskutiert, ob die Mikroorganismen des BMM das Brustgewebe tatsächlich kolonisieren, also bewohnen, oder ob sie nicht vielmehr aus den verschiedenen oben genannten Quellen stammen und wie Touristen auf der Durchreise sind.5,7,8
Risikofaktoren für eine Mastitis
Wie gezeigt wurde, sind Mikroorganismen während der Stillzeit ein normaler Bestandteil der Brustdrüse. Allerdings ist im Fall einer Mastitis die Gesamtzahl an Bakterien in der Muttermilch deutlich erhöht und die Diversität erniedrigt. Im Prinzip kommt es zu einer Dysbiose, bei der wenige Bakterien die anderen überwuchern. Man geht davon aus, dass die Dysbiose gemeinsam mit einer Hyperlaktation bzw. einem Milchstau ursächlich für eine Mastitis ist.2 Zudem ist wichtig zu wissen, dass Bakterien unterschiedliche Eigenschaften tragen können, die sie gefährlicher bzw. infektiöser für den Menschen machen, wie z.B. ihre Fähigkeit zur Bildung bestimmter Proteine, die sie resistenter gegen das Immunsystem machen, ihre Haftungsfähigkeit oder auch Antibiotikaresistenzen. Ein Staphylococcus aureus ist also z.B. nicht gleich einem anderen Staphylococcus aureus. Solche Virulenzfaktoren können die Entstehung einer Mastitis begünstigen und ihre Behandlung erschweren. Zu den äusserlichen Faktoren, die das Mikrobiom beeinflussen, gehört z.B. die Ernährung der Frau, da ein Teil des BMM aus dem Darm stammt. Eine Dysbiose oder gar Infektion des mütterlichen Darms, der kindlichen Mundhöhle oder der mütterlichen Haut kann eine Mastitis begünstigen, da diese – wie oben gezeigt – die Quellen des BMM sind. Auch Antibiotika, aber auch Probiotika beeinflussen das Brustmilchmikrobiom und damit das Risiko für eine Mastitis. Stress, Schlafmangel, Eisenmangel und ein geschwächtes Immunsystem sind ebenfalls relevante mütterliche Faktoren. Wunde Mamillen werden häufig als Risikofaktor angesehen bzw. mit Mastitis assoziiert, sie begünstigen zumindest Inflammation und den Eintritt von Bakterien der Haut und der Mundhöhle. Fremdoberflächen wie Milchpumpen oder Stillhütchen sind häufig mit Mikroorganismen besiedelt und stellen eine potenzielle Infektionsquelle dar, zudem fördert der Einsatz von Milchpumpen eine Hyperlaktation.
Das Mastitisspektrum
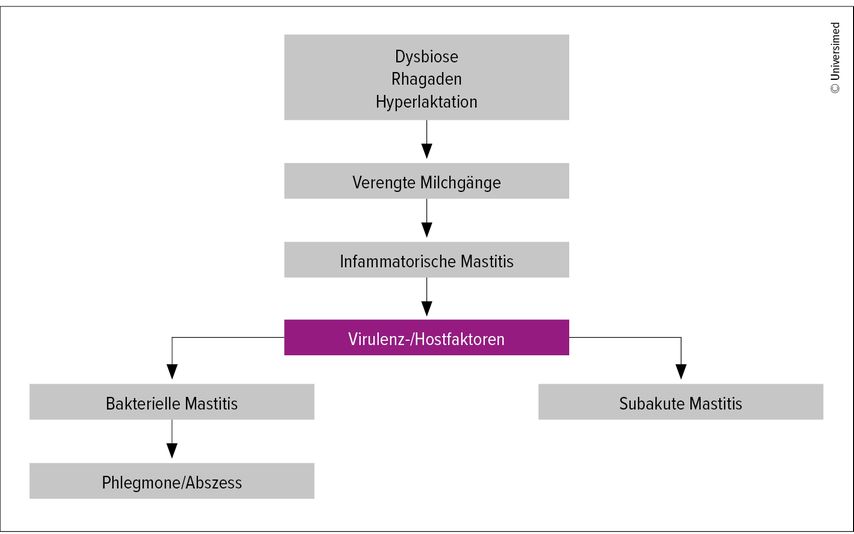
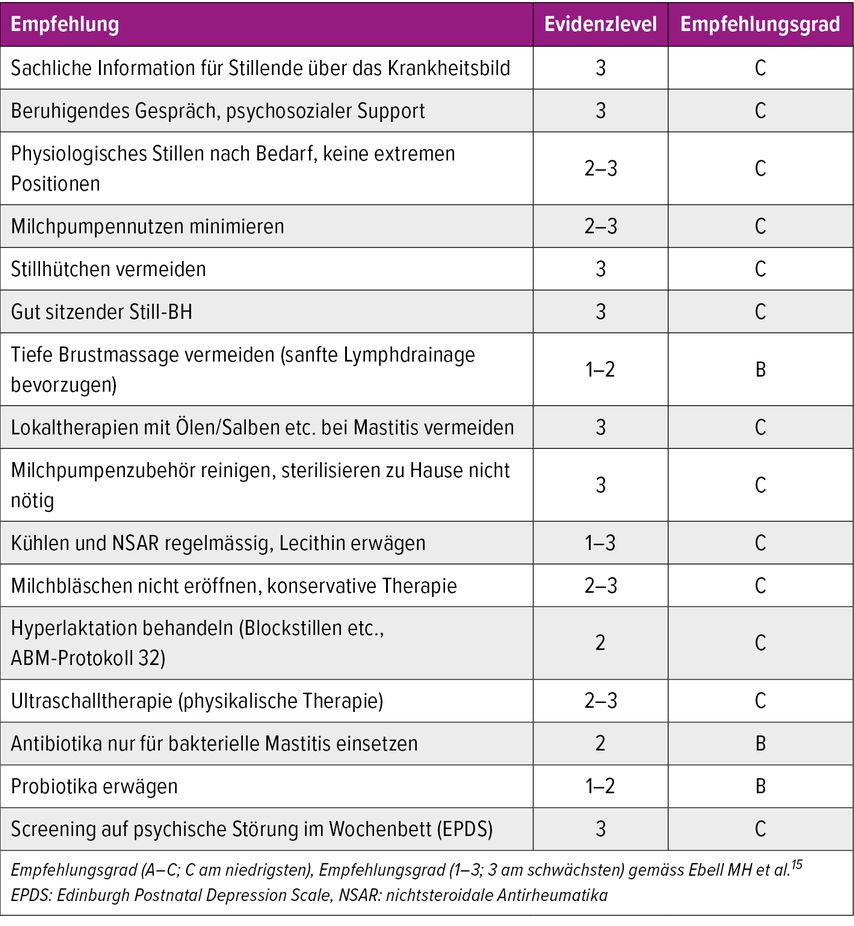
Ein lokaler Milchstau steht häufig am Anfang des Mastitisspektrums. Dieser führt zu einer mangelhaften Milchentleerung und nachfolgender Schwellung. Die Schwellung hat ein lokales Ödem zur Folge, das andere Milchgänge komprimiert und die Milchstase verstärkt. Es besteht zunächst eine Inflammation in den Milchgängen, also eine lokale Entzündungsreaktion mit Einwandern von Entzündungszellen. Ein bestehendes Überangebot an Milch im Sinne einer Hyperlaktation verstärkt die Stauungssymptomatik. Es bestehen nun verengte Milchgänge mit immer mehr enthaltenen Mikroorganismen und Entzündungszellen. Wenn dieser Milchstau nicht gelöst wird, kann es schliesslich zur inflammatorischen Mastitis kommen, bei der die Entzündungsreaktion sich auf das Gewebe um die Milchgänge herum ausweitet. Die nächste Stufe ist die bakterielle Mastitis mit Einwandern der Mikroorganismen in das umgebende Gewebe. Schliesslich kann ein Abszess oder sogar eine Fasziitis entstehen. Abhängig von Virulenzfaktoren des Erregers oder Hostfaktoren der Stillenden kann statt einer akuten Mastitis auch eine subakute Form entstehen (Abb. 3). Für alle Formen des Mastitisspektrums werden laut ABM die gleichen Basistherapien empfohlen (Tab. 1). Je nach Stufe kommen spezifische Therapien hinzu.2
Abb. 3: Das Mastitisspektrum modifiziert nach ABM-Protokoll 36(modifiziert nach Mitchell KB et al.)2
Milchstau («ductal narrowing»)
Bei einem Milchstau besteht eine lokal begrenzte Verengung von Milchgängen mit Dysbiose und Inflammation. Die Schwellung bedingt eine beeinträchtigte lokale Blut- und Lymphzirkulation. Klinisch imponieren eine lokale Schwellung und Rötung, die schmerzhaft sein kann. Es bestehen keine systemischen Symptome. Eine Therapie mit lokaler Kühlung, oralen nichtsteroidalen Antirheumatika (NSAR, z.B. Ibuprofen), regelmässiger physiologischer Brustentleerung und einer Überprüfung der Stilltechnik ist indiziert. Extreme Stillpositionen sowie ein forciertes Entleeren der Brust mit der Milchpumpe sind nicht sinnvoll. Das Verstärken einer Hyperlaktation sollte unbedingt vermieden werden. Es gelten die spektrumweiten Therapieempfehlungen gemäss Tabelle 1.2,9
Inflammatorische Mastitis
Diese Form der Brustdrüsenentzündung entsteht durch das schwellungsbedingte Einwandern von Entzündungszellen ins Gewebe. Häufig bestehen bereits Allgemeinsymptome wie Fieber und Krankheitsgefühl, die auch ohne eine bakterielle Mastitis möglich sind. Die Therapie setzt sich wie beim Milchstau aus lokaler Kühlung, regelmässiger Einnahme von oralen NSAR (Ibuprofen), physiologischer Brustentleerung und einer Überprüfung der Stilltechnik zusammen. Eine manuelle Lymphdrainage kann hilfreich sein. Nach 24 Stunden sollte eine erneute professionelle klinische Beurteilung erfolgen. Eine Abgrenzung zwischen inflammatorischer und bakterieller Mastitis ist klinisch kaum möglich. Daher sollte bei voranschreitenden Symptomen mit einer antibiotischen Therapie begonnen werden.
Bakterielle Mastitis
Beim Fortschreiten der Erkrankung kommt es zu einer starken Vermehrung eines Bakteriums zulasten des diversen physiologischen BMM und zum Einwandern dieser Bakterienspezies ins Brustgewebe. In einer grossen Untersuchung von Milchproben bei Laktationsmastitis wurde Staphylococcus epidermidis in knapp 92% der Proben nachgewiesen, Staphylococcus aureus bei knapp 30%. Die Gattungen Streptococcus (70,2%) und Corynebacterium(16,6%) waren ebenfalls häufig. Candida wurde hingegen nur in 0,5% der Proben gefunden und spielt bei der akuten Mastitis keine Hauptrolle.10 Klinisch imponieren neben Lokalsymptomen nun ein ausgeprägtes Krankheitsgefühl, Fieber und Kopfschmerzen. Es ist zusätzlich zu den allgemeinen Massnahmen wie in Tabelle 1 angeführteine antibiotische Therapie indiziert. Empfohlen werden Staphylokokkenpenicilline (Flucloxacillin) bzw. Cephalosporine der ersten oder zweiten Generation (Cefazolin, Cefuroxim). Bei Allergie gegen Cephalosporine kann Clindamycin eingesetzt werden oder auch Trimethoprim/Sulfamethoxazol (das Zweite allerdings nur bei reifgeborenen Säuglingen, die mindestens einen Monat alt sind). Die letzten beiden eignen sich auch bei Frauen mit Risikofakoren für eine MRSA-Infektion (Methicillin-resistenter Staphylococcus aureus). Eine bakterielle Mastitis ist nicht ansteckend und in der Regel kann weitergestillt werden. Bei schweren klinischen Verläufen muss auf Breitbandantibiotika wie z.B. Piperacillin-Tazobactam, Ceftriaxon oder sogar Vancomycin zurückgegriffen werden. Wichtig ist es, die wirksame antibiotische Therapie ausreichend lange durchzuführen. Empfohlen werden 10 bis 14 Tage.
Die Diagnose einer bakteriellen Mastitis ist klinisch zu stellen. In der Regel erfolgt zudem eine Laboruntersuchung der Entzündungswerte im Blut, wobei auch diese nicht hilfreich ist bei der Abgrenzung zu anderen Stufen des Mastitisspektrums, da Leukozyten und CRP unspezifische Inflammationsmarker sind. Bei schweren Verläufen sollten Blutkulturen abgenommen werden. Ein Ultraschall der Brust dient dem Ausschluss einer Abszedierung. Bei rezidivierenden Verläufen, Ausbleiben einer klinischen Besserung trotz antibiotischer Therapie oder bei Allergien gegen Antibiotika kann eine Muttermilchkultur hilfreich sein. Hierzu wird die Brust mit Wasser sanft gereinigt. Ein paar Milchtropfen werden verworfen. Nun erfolgen die manuelle Expression von Milch in das sterile Medium und eine rasche Weiterverarbeitung, da die zellulären Bestandteile der Milch die Keime auf dem Weg ins Labor abbauen können. Häufig finden sich in der Muttermilchkultur zahlreiche Mikroorganismen und die Interpretation kann Probleme bereiten. Daher ist eine Kultur sicher nicht bei jeder Erkrankung des Mastitisspektrums zielführend und sollte individuell eingesetzt werden.
Ein ambulantes Management sollte bei der Mastitis wann immer möglich angestrebt werden. Eine Separation von Mutter und Kind(ern) ist zu vermeiden, um das Weiterstillen zu ermöglichen. Wenn eine stationäre Aufnahme indiziert ist, sollten Mutter und Kind(er) gemeinsam aufgenommen werden. Physiologisches Stillen zur regelmässigen Brustentleerung ist wichtig für den Heilungsprozess. Eine Hyperlaktation ist zu vermeiden, da sie die Mastitis aggraviert. Daher ist der Einsatz von Milchpumpen bei Mastitis kritisch zu sehen.
Phlegmone, Abszess
Staphylokokken und Streptokokken gehören zu den Bakterien, die eine stark pyogene Wirkung haben. Daher kann sich eine bakterielle Mastitis in eitrigen Prozessen fortsetzen. Es sind die Phlegmone und der Abszess zu unterscheiden. Bei einer Phlegmone handelt es sich um eine diffuse eitrige Entzündung im Bindegewebe bedingt durch eine bakterielle Infektion. Hier gibt es keine klare Wand oder Kapsel und sie kann sich daher schnell ausbreiten. Ein Abszess ist dagegen eine klar begrenzte Gewebseinschmelzung durch bakterielle Toxine begrenzt durch eine Abszessmembran bzw. Bindegewebskapsel. Beide fallen klinisch durch eine lokalisierte tastbare Induration auf und können im Ultraschall bestätigt werden. Im Falle eines Abszesses ist eine Entlastung indiziert. Dies ist durch Punktion oder Drainage möglich. Beides sollte unter Ultraschallkontrolle erfolgen. Abszesspunktionen müssen in der Regel mehrfach erfolgen, um eine komplette Sanierung zu ermöglichen. Dafür sind sie im ambulanten Setting einfach durchzuführen und führen oft zum Erfolg. Für die Punktion empfehlen sich die Anwendung eines Lokalanästhesie-Pflasters oder eine lokale Infiltration und eine dicke Nadel zum Abpunktieren, da der Inhalt oft zäh fliesst. Auch eine Abszesseröffnung kann ambulant und unter Lokalanästhesie erfolgen, wenn dieser nicht zu tief liegt. Nach Stichinzision und Spülung sollte eine Drainage (z.B. Penrose, Gummilasche) eingelegt und mit einem Faden fixiert werden. Diese kann in der Regel nach drei bis sieben Tagen entfernt werden.11 Bei tiefer liegenden Abszessen muss die Drainage im Operationssaal unter Narkose erfolgen. Bei Drainagen oder Punktionen sollte eine mikrobiologische Kultur aus dem Abszessinhalt angelegt werden. In der Regel werden Antibiotika für 1–14 Tage gegeben. Bei lokalisierten Abszessen ohne relevante systemische Symptome (kein Fieber, kein Krankheitsgefühl) reicht mitunter die lokale Punktion bzw. Drainage.
Subakute Mastitis und Soor
Bei der subakuten Mastitis (SAM) wird heute eine chronische Verengung der Milchgänge in Kombination mit einer Dysbiose des BMM als Ätiologie angesehen.2,9 Es kommt wie bei der akuten Mastitis zu einer Vermehrung von pathogenen Bakterien, die im Normalzustand auch Teil des BMM sein können, aber nun proliferieren und die typische Symptomatik auslösen. Dies geht zulasten der Diversität (Vielfältigkeit) des BMM. Infrage kommen z.B. Koagulase-negative Staphylokokken (wie etwa Staphylococcus epidermidis) und Viridans-Streptokokken (wie etwa Streptococcus salivarius). Da sie nicht die gleichen Virulenzfaktoren aufweisen, wie z.B. Staphylococcus aureus, verläuft das Krankheitsbild anders, in diesem Fall subakut. Typische Symptome umfassen brennende Schmerzen in der Brust beim Stillen, die anhalten können und zum Teil in Achsel und Rücken ausstrahlen, Milchbläschen, rezidivierende Verhärtungen oder Rötungen, zum Teil in Kombination mit Hyperlaktation. Allgemeinsymptome sind untypisch. Ob auch Soor eine solche subakute Symptomatik auslösen kann, ist umstritten. Sicher ist dies deutlich seltener, als es eine Zeit lang angenommen wurde. Grundsätzlich erscheint es jedoch denkbar, dass ein Teil der SAM-Fälle auf dem Boden einer Dysbiose auch durch Candida bedingt sein können, insbesondere, wenn sich beim Kind (Windelsoor, Mundsoor) oder im Bereich der Haut der Mutter andere klinische Hinweise auf eine Mykose finden. Auch bei der SAM kann ein Therapieversuch mit Ibuprofen, Probiotika und ggf. auch Wärme nach dem Stillen erfolgen (insbesondere bei Tendenz zu Vasospasmen). Wenn andere Ursachen ausgeschlossen sind und die allgemeinen Therapieempfehlungen inkl. Optimierung des Stillmanagements wie in Tabelle 1 angeführt nicht geholfen haben, kann eine Therapie mit Antibiotika erfolgen, hier erscheinen bei SAM Makrolide günstig (z.B. Clarithromycin 2x500mg tgl., 10–14 Tage). Aufgrund der chronischen Natur der Schmerzen sollte vor Beginn der Therapie eine Milchkultur angelegt werden, welche allerdings nicht immer hilfreich ist. Bei klinisch hartem Verdacht auf Soor, bzw. Nachweis in der Milchkultur, kann eine lokale Therapie der Brust erfolgen (z.B. Miconazol, Clotrimazol oder Ketoconazol als Creme, jeweils nach dem Stillen für 14 Tage). Gleichzeitig sollte beim Säugling eine Therapie des Mund- und/oder Windelsoors in Rücksprache mit dem Kinderarzt/der Kinderärztin erfolgen. Wenn die Lokaltherapie der Brust zu keiner Symptommilderung führt, kann eine systemische Therapie mit Fluconazol oral für 2 Wochen erfolgen (am ersten Tag 200mg, dann 100mg/d). Dies sollte nur bei kulturell nachgewiesenem Soor bzw. eindeutiger Klinik erfolgen.
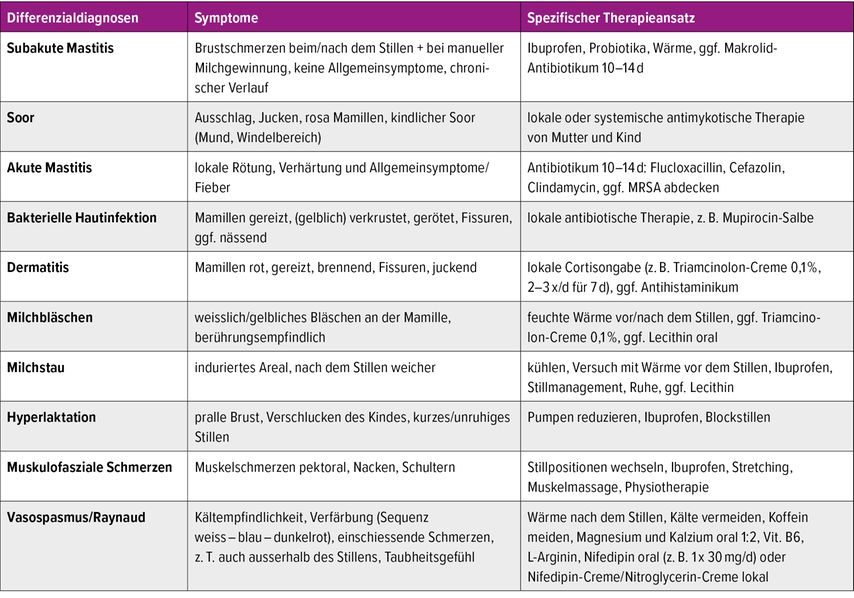
Brustschmerzen sind ein häufiges Symptom in der Stillzeit. Hier kommt neben Erkrankungen des Mastitisspektrums eine ganze Reihe an Differenzialdiagnosen infrage. Tabelle 2 bietet eine orientierende Übersicht. Die Frauen sind oft stark belastet. Neben der Abklärung somatischer Ursachen ist auch an die strukturierte Abfrage von Symptomen einer Wochenbettdepression zu denken. Hierfür sind kurze, standardisierte Fragebögen online und in vielen Sprachen erhältlich, z.B. die Edinburgh-Postnatal-Depression-Skala.Bei Auffälligkeiten sollte an Fachpersonen für Psychotherapie verwiesen werden.
Tab. 2: Überblick über Differenzialdiagnosen bei Brustschmerzen in der Stillzeit (modifiziert nach Lawrence RA et al.)9
Probiotika
Durch den enteromammären Weg gelangen Mikroorganismen aus dem Darm in die Brustdrüse und werden Teil des BMM (Abb. 3). Dies macht man sich auch beim Einsatz oral eingenommener Probiotika zunutze. In einer kleinen Studie mit 20 Frauen mit Laktationsmastitis erhielt die Hälfte täglich ein Probiotikum mit Lactobacillus salivarius CECT5713 und Lactobacillus gasseri CECT5714 versus Placebo. Nach 30 Tagen hatten die Frauen der Probiotikagruppe eine geringere Zahl an S. aureus im BMM und bei 6 von 10 Frauen konnten die verabreichten Lactobacilli im BMM nachgewiesen werden.12 In einer zweiten Studie wurde L. salivarius PS2 stillenden Frauen prophylaktisch verabreicht. Die Mastitisrate in der Probiotikagruppe konnte halbiert werden (25% versus 57%).13 In einer prospektiv-randomisierten Doppelblindstudie erhielten Frauen zwischen der 35. SSW und zwölf Wochen postpartal L. salivarius PS2 oder Placebo. Die Rate an Mastitis während des Studienzeitraums war in der Studiengruppe 58% niedriger (14% versus 6%). Allerdings war die Studie durch die Pharmaindustrie finanziert, welche entsprechende Produkte selbst vermarktet.14 Dies zeigt, dass oral verabreichte Probiotika das Potenzial zur Prophylaxe und Therapie einer Laktationsmastitis haben. Aufgrund des Einflusses des mütterlichen Hautmikrobioms wären auch Probiotika denkbar, welche über die Haut appliziert werden. Es sind weitere unabhängige klinische Studien mit gut abgestimmten Probiotika notwendig.
Zusammenfassung
Muttermilch enthält ein Mikrobiom aus Bakterien, Viren, Hefen und Pilzen sowie Protozoen und Archaea. Ein Grossteil des menschlichen Mikrobioms ist nicht kultivierbar und kann daher nur mit Methoden der Molekulargenetik nachgewiesen werden. Als Ursprung der Mikroorganismen in Muttermilch werden die mütterliche Haut, die kindliche Mundhöhle und der mütterliche Darm angesehen. Das Brustmilchmikrobiom wird durch mütterliche Ernährung, Adipositas, Begleiterkrankungen, Umweltfaktoren und Medikamente beeinflusst. Hier spielen insbesondere Antibiotika während Schwangerschaft, Geburt und in der Neugeborenenzeit eine wichtige Rolle. Die Mastitisformen werden heute als Spektrum ähnlicher Genese angesehen. Ursächlich sind verengte Milchgänge in Kombination mit einer Dysbiose des Brustmilchmikrobioms. Nicht selten besteht eine Hyperlaktation. Die Bakterien, welche eine Mastitis auslösen, gehören häufig zum physiologischen Brustmilchmikrobiom, es kommt jedoch zu einem Überwiegen eines oder weniger Mikroorganismen und damit zu einer Störung des natürlichen Gleichgewichts. Je nach Virulenzfaktoren der Erreger und Abwehrfaktoren der Stillenden entstehen in der Folge die verschiedenen Krankheitsbilder des Mastitisspektrums. Antibiotika und Antimykotika sollten nur bei hochgradigem klinischem Verdacht oder sogar Erregernachweis zum Einsatz kommen, da sie das Mikrobiom nachhaltig stören. Probiotika können bei gezieltem Einsatz in der Prävention und Therapie des Mastitisspektrums hilfreich sein.
Literatur:
1 Wilson E et al.: Incidence of and risk factors for lactational mastitis: a systematic review. J Hum Lact 2020; 36(4): 673 2 Mitchell KB et al.: Academy of Breastfeeding Medicine Clinical Protocol #36: The mastitis spectrum, revised 2022. Breastfeed Med 2022; 17(5): 360-7 3 Togo A et al.: Repertoire of human breast and milk microbiota: a systematic review. Future Microbiol 2019; 14(7): 623-41 4 Lackey KA et al.: What’s normal? Microbiomes in human milk and infant feces are related to each other but vary geographically: the INSPIRE study. Front Nutr 2019; 6: 5 Stinson LF et al.: The human milk microbiome: who, what, when, where, why, and how? Nutr Rev 2021; 79(5): 529-43 6 Pannaraj PS et al.: Shared and distinct features of human milk and infant stool viromes. Front Microbiol 2018; 9: 1162 7 Xu R et al.: Residents or tourists: Is the lactating mammary gland colonized by residential microbiota? Microorganisms 2024; 12(5): 1009 8 Dombrowska-Pali A et al.: Human milk microbiome—a review of scientific reports. Nutrients 2024; 16(10): 1420 9 Lawrence RA, Lawrence RM: Breastfeeding: aGuide for the Medical Profession. 9th ed. Elsevier 2021 10 Mediano P et al.: Microbial diversity in milk of women with mastitis: potential role of coagulase-negative staphylococci, viridans group streptococci, and corynebacteria. J Hum Lact 2017; 33(2): 309-18 11 Kornfeld H et al.: Management of infected galactocele and breast implant with uninterrupted breastfeeding. Plast Reconstr Surg Glob Open 2021; 9(11): e3943 12 Jiménez E et al.: Oral administration of Lactobacillus strains isolated from breast milk as an alternative for the treatment of infectious mastitis during lactation. Appl Environ Microbiol 2008; 74(15): 4650-5 13 Fernández L et al.: Prevention of infectious mastitis by oral administration of Lactobacillus salivarius PS2 during late pregnancy. Clin Infect Dis 2016; 62(5): 568-73 14 Jiménez E et al.: Ligilactobacillus salivarius PS2 supplementation during pregnancy and lactation prevents mastitis: a randomised controlled trial. Microorganisms 2021; 9(9): 1933 15 Ebell MH et al.: Strength of recommendation taxonomy (SORT): a patient-centered approach to grading evidence in the medical literature. J Am Board Fam Pract 2004; 17(1): 59-67
Das könnte Sie auch interessieren:
ERAS: Was wissen und machen wir in Österreich?
Im September 2024 fand in der Nähe von Málaga in Spanien der 10. Weltkongress der Internationalen Gesellschaft für „Enhanced Recovery After Surgery“ (ERAS) statt. Im Rahmen des ...
Morbus Paget der Vulva
Nach Definition der WHO stellt der Morbus Paget der Vulva eine intraepitheliale Neoplasie und obligate Präkanzerose dar, die von pluripotenten Stammzellen der interfollikulären Epidermis ...
„Eine Kombination könnte eine personalisierte und prädiktive Medizin ermöglichen“
Wir müssen uns eingestehen, dass auch in der heutigen Medizin manche Vorgehensweisen als unmodern und geradezu primitiv anzusehen sind. Dies gilt auch für Vorsorge und Früherkennung von ...