Bessere Diagnostik, geringerer Antibiotikagebrauch
Bericht:
Reno Barth
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Wenn es um die Unterscheidung zwischen viralen und bakteriellen Infektionen der unteren Atemwege geht, zeigt die klinische Diagnostik eine geradezu katastrophale Sensitivität. Die Folge ist häufige antibiotische Übertherapie. Biomarker im ambulanten Setting und molekulare Diagnostik im Krankenhaus verbessern die Ergebnisse und führen zu reduziertem Antibiotikagebrauch ohne Nachteile für die Patienten.
Um eine sinnvolle antibiotische Therapie einer Infektionskrankheit sicherzustellen, ist auf mehrere Parameter zu achten, so Univ.-Prof. Dr. Daiana Stolz von der Universität Freiburg im Rahmen der „ERS Satellites“. Es sollte eine korrekte Diagnose vorliegen, es sollte ein Antibiotikum mit einem schmalen Wirkspektrum gewählt und über eine möglichst kurze Zeit eingesetzt werden. Dabei ist auf die lokale Verbreitung von Resistenzen zu achten. Wo immer möglich sollte durch rechtzeitige Impfung der Bedarf an einem Antibiotikum von vornherein vermieden werden. Es gelte eine einfache Regel: Je mehr Antibiotika verwendet werden, desto mehr Resistenzen wird man bekommen.
Daten aus verschiedenen europäischen Ländern zeigen sehr unterschiedliche Verschreibungspraktiken und letztlich auch sehr unterschiedliche Resistenzmuster, die mit den Verschreibungen im jeweiligen Land korrelieren. Insbesondere die Resistenzraten von Pneumokokken gegen Penicillin sind in Ländern mit hohem Antibiotikagebrauch hoch.1
Konventionelle Mikrobiologie ist langsam und unzuverlässig
Ein erster Schritt wäre die korrekte Unterscheidung zwischen viralen und bakteriellen Infektionen. Diese sei allerdings in der Theorie oft einfacher als im klinischen Alltag, so Stolz, was häufig zu Antibiotikaeinsatz auf Verdacht führe. Das ist nicht besonders sinnvoll, wie Studiendaten zeigen: In einer Untersuchung mit mehr als 2000 erwachsenen Patienten mit Husten und Verdacht auf eine Infektion der unteren Atemwege reduzierte der empirische Einsatz von Amoxicillin weder Schwere noch Dauer der Symptome signifikant. Dafür waren in der Antibiotikagruppe unerwünschte Wirkungen wie Ausschlag, Durchfall und Übelkeit häufiger. Diese Ergebnisse waren unabhängig vom Patientenalter.2
Im Gegensatz dazu führt eine ätiologische Diagnose einer Infektion der unteren Atemwege, gefolgt von einer gezielten, am jeweiligen Pathogen ausgerichteten Therapie zu deutlichen Reduktionen von Morbidität und Mortalität – insbesondere wenn es sich um eine bakterielle Infektion handelt und die antibiotische Therapie innerhalb weniger Stunden begonnen werden kann. Stolz: „Wenn wir wissen, was wir behandeln, bekommen wir viel bessere Ergebnisse.“ Allerdings gilt auch hier: In der Praxis stellen sich die Dinge oft weit komplexer dar als in der Theorie. Denn die konventionelle Mikrobiologie ist ein zweifelhafter Goldstandard in der Diagnostik mit teilweise sehr geringer Sensitivität. Zudem benötigen Untersuchungen auf Kulturbasis bis zu 72 Stunden und zusätzlich noch Tests auf Antibiotikaresistenzen. Stolz: „Während wir auf die Ergebnisse der Bakteriologie warten, wissen wir nicht, was wir mit dem Patienten machen sollen. In diesen Situationen wird dann sehr freizügig mit Antibiotika behandelt.“ Bei bereits unter antibiotischer Therapie stehenden Patienten ist der Erregernachweis noch schwieriger. Man dürfe in diesem Zusammenhang auch nicht übersehen, dass virale Infektionen der Atemwege sehr schwerwiegend verlaufen und sowohl die oberen als auch die unteren Atemwege betreffen können, so Stolz. Virale Infektionen zeigen dabei eine deutliche saisonale Häufung mit typischen, wiederkehrenden Mustern. Dies trifft nicht nur auf die bekannten Influenzawellen, sondern auch auf eine Vielzahl anderer Viren wie Rhinoviren, Coronaviren und RSV zu. Stolz weist allerdings darauf hin, dass Jahr um Jahr zu Zeiten vermehrter viraler Infektionen auch der Antibiotikaverbrauch ansteigt. Dies sei sogar in Ländern mit sehr restriktivem Antibiotikaeinsatz wie zum Beispiel den Niederlanden zu beobachten.
Eine in den USA durchgeführte Studie mit erwachsenen Patienten, die wegen Pneumonie hospitalisiert werden mussten, fand bei weniger als 40% überhaupt einen Erreger. Wurde ein Erreger gefunden, so war es in der Mehrzahl der Fälle ein Virus. Lediglich 14% der Kohorte zeigten eine nachgewiesene bakterielle Infektion.3
Unterscheidung zwischen viralen und bakteriellen Infektionen
Ein besonderes Problem stellen Koinfektionen dar. Eine Studie, die mit mehr als 1000 immunkomprimierten Patienten mit Atemwegsinfektion, die sich einer Bronchoskopie unterzogen, durchgeführt wurde, fand bei rund 10% sowohl virale als auch bakterielle Erreger. Darunter waren RSV und Adenoviren mit der höchsten Mortalität assoziiert. Auch kombinierte virale und bakterielle Infektionen erhöhten die Sterblichkeit, während bei rein bakteriellen Infektionen die Mortalität niedriger war.4
Stolz betont, dass Viren auch im Zusammenhang mit COPD-Exazerbationen nicht unterschätzt werden dürfen und in rund einem Drittel der Fälle nachgewiesen werden können.5 Alle diese Daten sind allerdings nicht geeignet, die Entscheidung für oder gegen Antibiotika im konkreten Fall zu erleichtern, sondern erhöhen allenfalls die Verwirrung, so Stolz.
Wird versucht, eine bakterielle Pneumonie rein anhand klinischer Zeichen zu diagnostizieren, so gelangt man zu wenig verlässlichen Ergebnissen. Eine Studie aus dem Jahr 2006 zeigte für dieses Vorgehen einen positiven Prädiktionswert von lediglich 14%. Der negative Prädiktionswert ist mit 90% deutlich besser, was letztlich bedeutet, dass zwar wenige bakterielle Pneumonien unerkannt bleiben, dass gleichzeitig jedoch viel zu viele Patienten, die kein Antibiotikum benötigen, eines erhalten.6 Zusätzliche Informationen liefert die Bildgebung. Womit ebenfalls nicht alle Probleme gelöst sind. Stolz verweist auf eine vor rund zehn Jahren an Intensivstationen durchgeführte Studie, die lediglich geringe Übereinstimmung zwischen Röntgen und CT zeigt, wobei das Röntgen in einem hohen Prozentsatz zu falschen Diagnosen führte.7
Biomarker erweisen sich im klinischen Alltag als hilfreich
Mehrere Studien zeigen, dass sich der Antibiotikagebrauch durch den Einsatz der Biomarker C-reaktives Protein (CRP) und Procalcitonin signifikant senken lässt. In einer niederländischen Arbeit, die in allgemeinmedizinischen Praxen durchgeführt wurde, reduzierten sowohl der Einsatz von CRP als auch ein Training für verbesserte anamnestische Kommunikation die Menge der verschriebenen Antibiotika. Wurden CRP und Schulung kombiniert, sank der Antibiotikagebrauch um fast 80% –ohne dass es dadurch zu schlechteren klinischen Outcomes kam.8
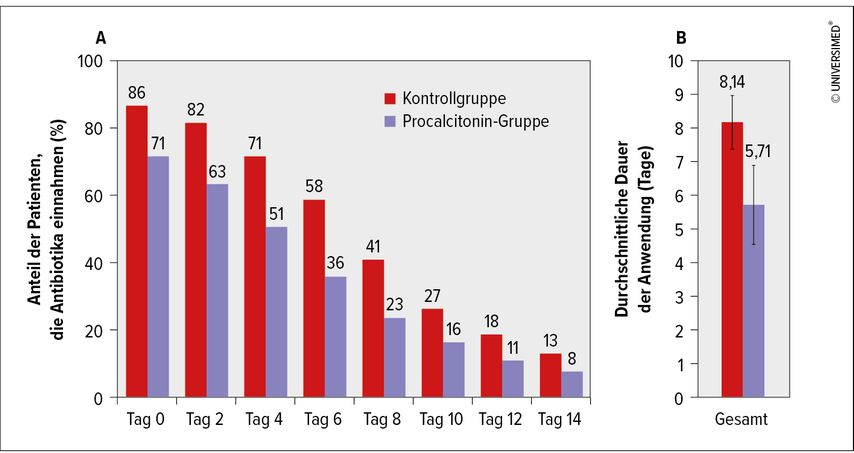
Für den Einsatz von Procalcitonin konnten in zahlreichen Studien Senkungen des Antibiotikabedarfs zwischen 20% und fast 80% gezeigt werden, ohne dass es dadurch zu einem Anstieg der Mortalität gekommen wäre. Eine Metaanalyse von 26 Studien in 12 Ländern mit mehr als 6000 Patienten zeigte in den Procalcitonin-Gruppen im Mittel eine Reduktion der Antibiotikaexposition um 2,4 Tage (Abb. 1).9
Abb. 1: Der Einsatz von Procalcitonin als Biomarker senkt den Antibiotikabedarf bei Patienten mit Atemwegsinfektionen (modifiziert nach Schuetz P et al. 2018)9
Nicht perfekt, aber besser: Erregernachweis mit PCR
Im Krankenhausbereich werden mittlerweile auch Forderungen nach vermehrtem Einsatz von PCR zum genetischen Erregernachweis erhoben. So zum Beispiel in der aktuellen Leitlinie von ERS/ESICM/ESCMID/ALAT für das Management ambulant erworbener Pneumonien.
Wann immer möglich soll mit Sputum oder endotrachealen Aspiraten aus den unteren Lungenabschnitten mittels PCR befundet werden, sofern der Einsatz von Nichtstandard-Antibiotika angedacht wird. Diese Empfehlung hat sehr niedrige Evidenzqualität und auch Stolz betont, dass es zu diesem Vorgehen wenig Studiendaten gibt.10 Eine der verfügbaren Arbeiten verglich Multiplex-PCR mit konventioneller Diagnostik (Kultur) – jeweils aus der bronchoalveolären Lavage (BAL) – und fand zu jedem Zeitpunkt höhere Diagnoseraten mit der PCR.11 Stolz: „Die Sensitivität war mit etwas über 30% noch immer sehr schlecht – aber immerhin besser als im konventionellen Arm, in dem 22% erreicht wurden.“ Auch wurden Unterschiede zwischen den Keimen mit einer höheren Sensitivität bei gramnegativen Bakterien gefunden.
Die Frage sei also: „Hilft das in der Klinik?“ Die Antwort ist offen. In einer prospektiven Beobachtungsstudie mit 605 Fällen zeigte sich, dass der Einsatz der PCR zwar zur Detektion von 50% mehr Bakterien führte, dass die klinischen Konsequenzen jedoch minimal waren und sich die beiden Gruppen hinsichtlich der gewählten Therapien sowie hinsichtlich der Dauer der Krankenhausaufenthalte nicht signifikant unterschieden.12
In der Folge wurde zu dieser Fragestellung die randomisierte, prospektive Studie Flagship II durchgeführt, die eine deutliche Reduktion unnotwendiger Antbiotikatherapien um 45% zeigte. Die Chancen, ohne Antibiotikum auszukommen, wurden damit um mehr als den Faktor 3 erhöht, die mittlere Dauer antibiotischer Therapien reduzierte sich um mehr als 20%.13 Entscheidend war, so Stolz, dass esdabei klare Anweisungen für die Behandler gab, welche Maßnahmen in welcher Situation zu setzen sind. Stolz: „Das zeigt, dass molekulare Diagnostik den Antibiotikagebrauch senken kann, wenn man den Klinikern genaue Leitlinien gibt.“ Vergleichbares wurde auch in einem intensivmedizinischen Setting gezeigt.14
Quelle:
ERS Satellites 2024: Session „Infection“, online am 5. März 2024
Literatur:
1 Goossens H et al.: Lancet 2005;365(9459): 579-87 2 Little P et al.: Lancet Infect Dis 2013; 13(2): 123-9 3 Jain S et al.: N Engl J Med 2015; 373(5): 415-27 4 Jahn K et al.: Eur J Intern Med 2024; 120: 52-61 5 Stolz D et al.: Eur Respir J 2019; 54(4): 1900407 6 Hopstaken RM et al.: Fam Pract 2006; 23(5): 512-9 7 Self WH et al.: Am J Emerg Med 2013; 31(2): 401-5 8 Cals JWL et al.: Br Med J 2009; 5: 338-74 9 Schuetz P et al.: Lancet 2018; 18(1): 95-107 10 Martin-Loeches I et al.: Intensive Care Med 2023; 49(6): 615-632 11 Affolter K et al.: Chest 2018; 154(3): 722-5 12 Salina A et al.: ERJ Open Res 2022; 8(2): 00595-2021 13 Darie AM et al.: Lancet Respir Med 2022; 10(9): 877-87 14 Poole S et al.: J Infect 2022; 85(6): 625-33
Das könnte Sie auch interessieren:
Therapie der obstruktiven Schlafapnoe – eine interdisziplinäre Herausforderung
Die obstruktive Schlafapnoe (OSA) ist mit einem erhöhten kardiovaskulären Risiko belastet. Outcome-Studien für die CPAP-Therapie zeigten jedoch nicht die erwarteten Therapieerfolge. Dies ...
Allergie: wie es beginnt
Allergien sind multifaktorielle Erkrankungen, die in jedem Lebensalter, vornehmlich aber in den ersten Lebensdekaden auftreten. Auch Asthma bronchiale ist eine heterogene, ...