Sarkoidose: die Fortschritte der letzten 20 Jahre
Autor*innen:
PD Dr. Anne-Marie Kirsten
Prof. Dr. Detlef Kirsten
Hamburger Lungenpraxis
Hamburg
OÄ Dr. Elvin Atug
Klinik für PneumologieAsklepios-Klinik Harburg
Hamburg
Korrespondierender Autor:
Prof. Dr. Detlef Kirsten
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Die Sarkoidose ist ein heterogenes, ätiologisch ungeklärtes multisystemisches Syndrom. Seit Jahrzehnten spricht man deshalb vom „Chamäleon“ der inneren Medizin oder nach dem Sarkoidoseexperten D.G. James vom „Eisbergcharakter der Sarkoidose“. In den letzten zwei Jahrzehnten hat sich vordergründig betrachtet an diesen Einschätzungen wenig geändert. Die Begründung hierfür ist sicher die weiter ungeklärte Ursache der Erkrankung. Doch im Detail ergibt sich ein anderes erfreulicheres Bild. Auf jedem der genannten Teilgebiete der Sarkoidoseforschung hat sich viel getan.
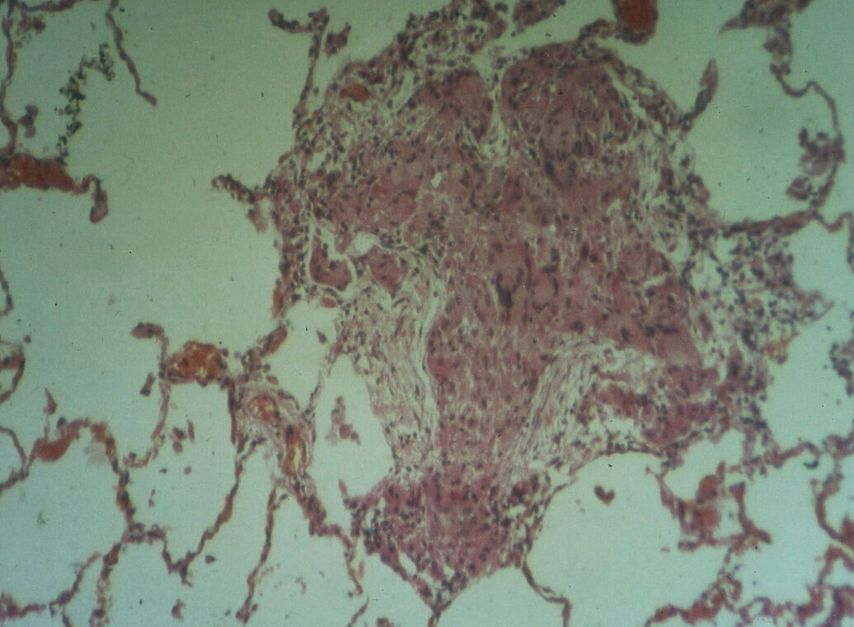
Im Zentrum des wissenschaftlichen Interesses steht weiterhin das epitheloidzellige Granulom, die bedeutendste immunologische Leistung des erkrankten Organismus, um seine Integrität zu wahren (Abb.1). Aus der Vielzahl der potenziellen Sarkoidose verursachenden Agenzien haben in der aktuellen Forschung Mycobacteriumtuberculosis und Propionibacteriumacnes die größte Bedeutung.
Immunologie und Genetik
Ein internationaler Forschungsschwerpunkt der letzten Jahrzehnte sind die BAL-Zellen mit ihren unterschiedlichen Zytokinmustern. In den letzten Jahren wurde besonders die Funktionsweise regulatorischer T-Zellen bei den verschiedenen Aktivitätsformen der Sarkoidose erforscht. Die gute Prognose der akuten Sarkoidose scheint auf gut funktionierenden regulatorischen T-Zellen zu beruhen. BAL-Studien zeigten bei aktiver Sarkoidose eine vermehrte Zahl an T-Helfer-Lymphozyten. In den letzten Jahren wurde geklärt, dass die Th1-Helferzellen sich zu Th17.1 differenzieren können, die wiederum ein Hauptproduzent von IFN-gamma sind. Eine vermehrte Th17.1-Produktion ihrerseits ist verbunden mit einem Verlust an regulatorischen T-Zellen und dadurch bedingter Dysbalance mit unterschiedlicher Aktivität von Th1, Th2 sowie Makrophagenprodukten der körpereigenen Abwehr.
Das erste Sarkoidosegen wurde von deutschen Forschern im Jahr 2005 auf Chromosom 6 identifiziert. Ein einziger veränderter Gen-Buchstabe im Eiweiß BTNL2 vermindert die Signalfunktion für ein eindringendes Agens, führt zur Entzündung und erhöht so das Risiko für das Krankheitsbild Sarkoidose um 60%. Von der weiteren immunologischen Forschung wird die Lösung des Sarkoidoserätsels erwartet.
Bronchologische Diagnostik
Angesichts der Bedeutung einer histologisch abgesicherten Sarkoidosediagnose ist neben der Haut und den peripheren Lymphknoten die Lunge im Fokus der bioptischen Untersuchungen. Bei schwer zugänglichen extrapulmonalen Herden versucht man so zur histologischen Bestätigung zu kommen, um die Diagnose abzusichern.
Seit ca. 20 Jahren werden zur Diagnostik der Sarkoidose kaum noch Organbiopsien oder eine Mediastinoskopie durchgeführt. Auch die Zahl der transbronchialen Lungenbiopsien ist deutlich zurückgegangen. Die EBUS-transbronchiale Nadelbiopsie (EBUS-TBNA) hat sich in den letzten Jahren als zuverlässige Methode zur Sicherung der Diagnose aus mediastinalen und hilären Lymphknoten entwickelt und hat die bronchialen Schleimhautbiopsien wie auch meist die transbronchialen Lungenbiopsien abgelöst.
Die neuen Bildverfahren ersetzen oft eine Biopsie (PET, MRT bei Neuro- bzw. Herzsarkoidose) oder zeigen dem Anwender der bioptischen Methoden den zielgenauen Weg.
Für die diffusen, differenzialdiagnostisch oft schwer einzuordnenden pulmonalen Herdsetzungen scheint sich in den letzten fünf Jahren die transbronchiale Kryobiopsie mit dem Erhalt größerer Zellverbände einen festen Platz in der Diagnostik zu erobern. Offene Lungenbiopsien sind im Gegensatz zum vergangenen Jahrhundert bei Sarkoidoseverdacht eine Rarität geworden.
Bildgebung
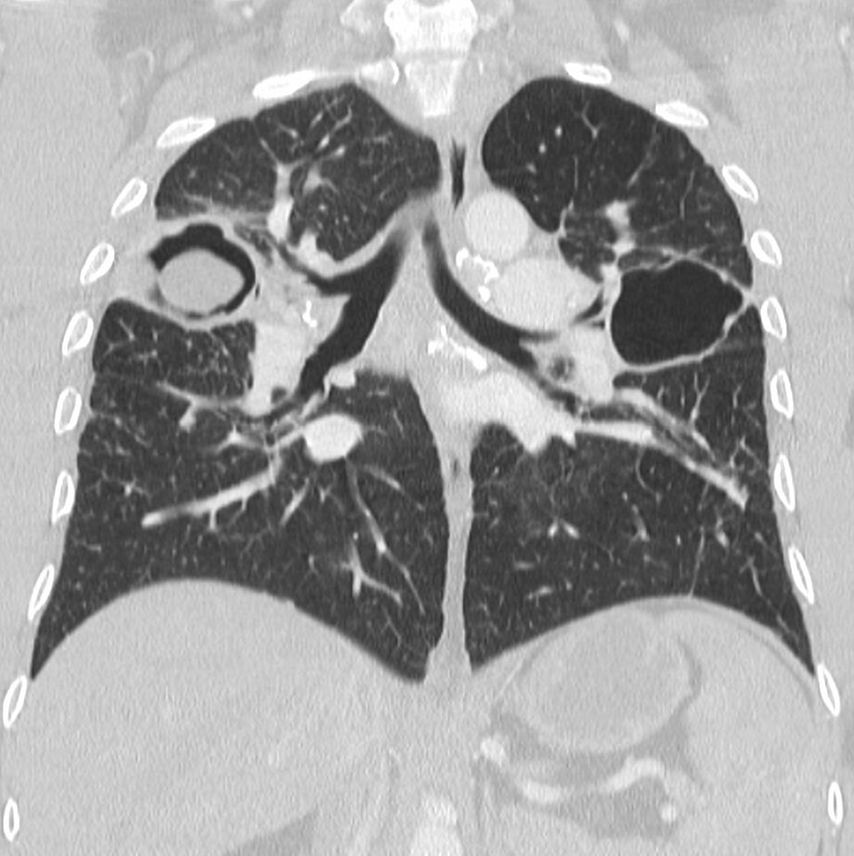
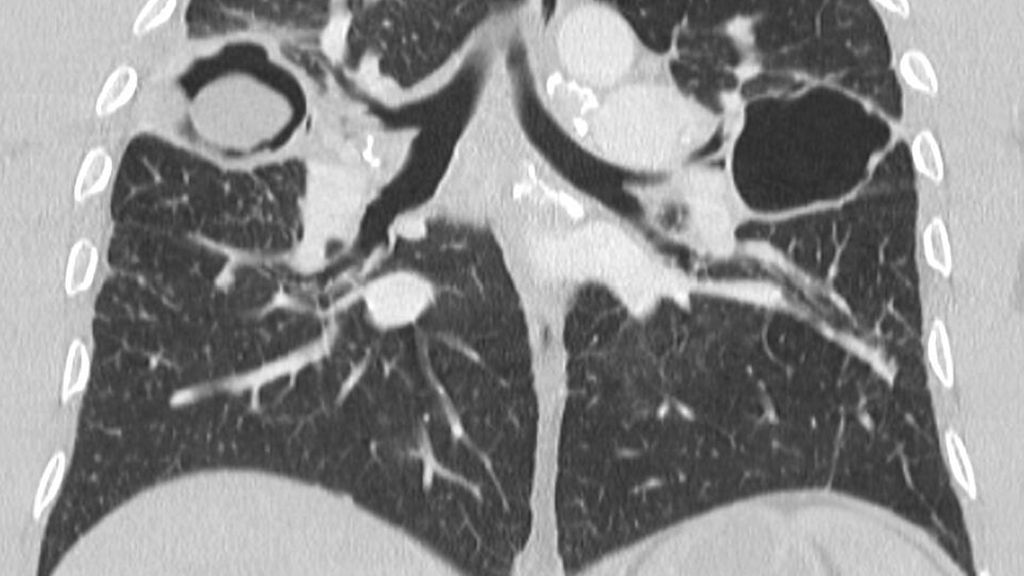
Aus klinischer Sicht sind die größten Fortschritte bei den verschiedenen Bildgebungsmethoden zu nennen. Insbesondere die zunehmende Anwendung hochauflösender Computertomogramme (HRCT, Abb. 2) hat zu wesentlichen neuen Erkenntnissen geführt. Das betrifft genau genommen nur ca. 20% aller Patienten. Bei diesen Patienten ist die frühe Kenntnis von Fibrosierungsvorgängen besonders wertvoll.
Abb. 2: Thorax-CT mit chronischer Lungensarkoidose und beidseitigen Aspergillomen und Kaverne links
Bei der Mehrzahl der Patienten mit Lungensarkoidose reicht zur Diagnostik weiterhin eine Thorax-Übersichtsaufnahme in zwei Ebenen aus. Die Einteilung in Röntgen-Typen oder Stadien wird weiterhin nur anhand der Thorax-Übersichtsaufnahmen durchgeführt! Unseres Erachtens wird derzeit die Computertomografie (CT) zu häufig bei der Primärdiagnostik eingesetzt. Nur bei 20% bis max. 30% aller Patienten führt eine CT zu besseren Ergebnissen mit früher Kenntnis von strukturellen Änderungen und Komplikationen.
Indikationen zur HRCT bei Sarkoidose sind zum Beispiel:
-
Verdacht auf eine Sarkoidose bei unauffälligem Röntgen-Thoraxbild (bis zu 10% der Fälle!)
-
atypische klinische und radiologische Befunde
-
Verdacht auf Superinfektion oder Pneumonie bei bekannter Sarkoidose
-
Verdacht auf Malignität
-
begleitende Komorbidität wie COPD
-
Verdacht auf Komplikationen wie Aspergillom
-
Verdacht auf fibrotische Veränderungen
Der Gebrauch von HRCT-Aktivitäts-Scores hat sich nicht durchgesetzt, wohl auch wegen des Fehlens kompetenter Pulmo-Radiologen.
Nuklearmedizinische Untersuchungen bei Sarkoidose wurden lange Zeit mit Ga67 durchgeführt. Die hohe Strahlenbelastung ließ ihre Anwendung nur in Studien und bei differenzialdiagnostischen Problemen zu.
Eine sensitivere Methode stellt heute die F-18-Fluorodeoxyglucose-Positronen-Emissions-Tomografie (FDG-PET) dar. Mithilfe des dabei durchgeführten Ganzkörperszintigramms können auch versteckte stoffwechselaktive Granulome dargestellt werden. Die Studien mit FDG-PET der vergangenen Jahre zeigten erneut den systematischen Charakter der Erkrankung. Naturgemäß speichern die meisten Granulome bei Röntgen-Typen I und II der Lungensarkoidose. Wertvoll ist die FDG-PET-Untersuchung besonders bei extrapulmonalen Sarkoidosen wie Herz- und Hirnbefall.
Ein Verfahren ohne Röntgenstrahlen ist die Magnetresonanztomografie (MRT), die auch zur Untersuchung des Lungenparenchyms eingesetzt werden kann. Diese hat sich bezüglich der Lungensarkoidose bisher nicht durchgesetzt, wohl aber beispielsweise bei der kardialen Sarkoidose, da hierdurch eine exakte Darstellung des befallenen Myokards dargestellt werden kann. Die MRT eignet sich so auch zur Verlaufsbeobachtung derartig komplizierter verlaufender extrapulmonaler Sarkoidosen. Seit in den letzten 10 Jahren die MRT und FDG-PET-Methoden bei der Sarkoidose vermehrt angewendet wurden, konnte in vielen Fällen das wahre Ausmaß jedes Granulombefalls erkannt werden. Das gilt im Besonderen für die Beteiligung der Knochen und der Muskulatur, beides Sarkoidosemanifestationen, die ohne diese Methoden eher selten diagnostiziert werden.
Nicht unerwähnt bleiben soll die transthorakale Sonografie in der Hand ausgewiesener Experten. Mit hochauflösendem Ultraschall und/oder Farbdoppler gelingt es, mediastinale Lymphome darzustellen und im Verlauf zu kontrollieren.
Diagnostik extrapulmonaler Sarkoidosen
Die Diagnostik extrapulmonaler Sarkoidosen ist (mit Ausnahme der Hautsarkoidose) wegen ihrer Seltenheit weiterhin ein Problem. Hier sind differenzialdiagnostisches Denken und die klinische Erfahrung von besonderer Bedeutung. Bei der Therapie derartiger Sarkoidoseformen gilt ebenfalls die oben gemachte Einschränkung zur Therapienotwendigkeit nur bei Symptomen oder Funktionsverlust. Ausnahmen hiervon sind Herz- und Hirnbefall, die eine unbedingte Therapie erfordern. Art und Dauer der Behandlung sollten von einem Expertenteam, zum Beispiel im Rahmen eines multidisziplinären Boards, diskutiert werden.
Wegen der besonderen Brisanz der Herzsarkoidose und wegen des jahrzehntelangen Interesses der Autoren an dieser Problematik soll die Zusammenarbeit von Kardiologen und Pneumologen bei dieser Spielart der Sarkoidose betont werden. In Deutschland ist 2020 ein Konsensus-Papier beider Fachgesellschaften zu diesem Thema publiziert worden. Eine aktuelle Kasuistik soll diesen Sachverhalt unterstreichen:
Fallbericht: junge Patientin mit einem AV-Block III° bei kardialer Sarkoidose
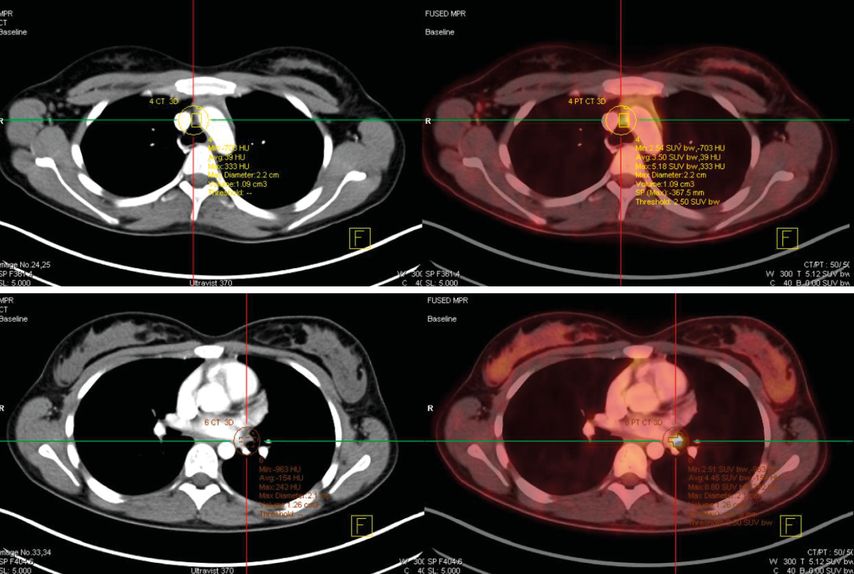
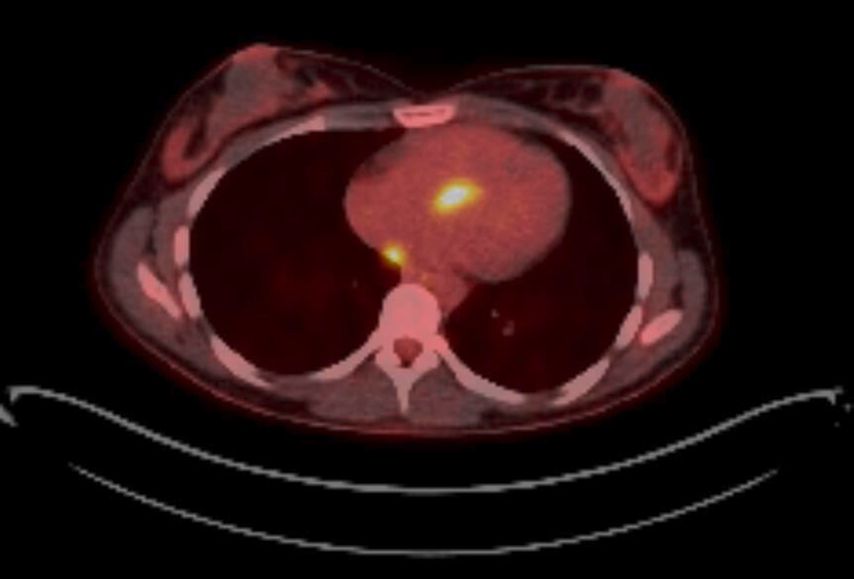
Eine 20-jährige Patientin wird in Begleitung des Rettungsdienstes aus der Hausarztpraxis mit orthostatischem Schwindel und Belastungsluftnot in die Klinik eingewiesen. Es bestehen keine Vorerkrankungen und es werden keine Medikamente eingenommen. Die Patientin gab an, in den letzten Tagen sich körperlich nicht mehr belasten zu können, sonst sei sie regelhaft sportlich sehr aktiv. Elektrokardiografisch konnte bei Aufnahme ein AV-Block 3. Grades nachgewiesen werden, sodass die umgehende Monitorüberwachung und stationäre Aufnahme erfolgte. Die weitere diagnostische Abklärung konnte ursächlich hierfür den Nachweis einer kardialen Sarkoidose bekräftigen. Die ergänzend neben dem Herz-MRT durchgeführte PET-CT-Untersuchung konnte eine hohe FDG-Aufnahme im Bereich des basalen interventrikulären Septums zeigen als morphologisches Korrelat des AV-Blockes (Abb. 3 und Abb. 4).
Abb. 3: PET-CT mit Nachweis einer FDG-Speicherung von kleinen mediastinalen und linkshilären Lymphknoten (mit freundlicher Genehmigung von Prof. Gross-Fengels, MVZ Nuklearmedizin Hamburg-Harburg)
Abb. 4: PET-CT mit Nachweis einer hohen FDG-Speicherung im Bereichdes basalen intraventrikulären Septums (mit freundlicher Genehmigung von Prof. Gross-Fengels, MVZ Nuklearmedizin Hamburg-Harburg)
Die EBUS-gestützte Punktion von kleinen, im PET-CT positiven mediastinalen Lymphknoten konnte histologisch den Nachweis von nicht nekrotisierenden Epitheloidzellgranulomen sichern. Nach Einleitung einer Prednisolontherapie kam es sehr rasch zu einem Rückgang der höhergradigen AV-Blockierungen. In den darauffolgenden sehr engmaschigen LZ-EKG-Kontrollen konnten keine AV-Blockierungen mehr aufgezeichnet werden, die klinische Beschwerdesymptomatik war vollständig rückläufig. In diesem speziellen Fall wurde aufgrund des Alters der Patientin und der raschen Regredienz der AV-Blockierung von einer Schrittmacherversorgung zunächst abgesehen.
Therapie der Sarkoidose
Die Heterogenität des Krankheitsbildes Sarkoidose sowie ihre Seltenheit verhindern bislang große Therapiestudien. Deshalb kommt es weiterhin auf die Darstellung des Einzelfalls an, der in seiner individuellen Besonderheit eine klinische Wertung erfahren muss.
Die entscheidende Voraussetzung zur Therapie ergibt sich allein durch ihre klinische Symptomatik mit Einschränkung der Lebensqualität. Bei einer Erkrankung mit einer hohen spontanen Remissionsrate ist eine solche Vorgehensweise zwingend und hat sich unter den Experten durchgesetzt. Weiterhin ist die Therapie mit Glukokortikoiden die Therapie der Wahl bei allen Formen der Sarkoidose.
Die verwendeten Dosierungen der Glukokortikoide haben sich in den letzten Jahren geändert. Die Anfangsdosis liegt jetzt bei 20–30mg/d. Die Gesamtbehandlungsdauer wird mit 6–12 Monaten angegeben, im Einzelfall länger. Die Leitlinien empfehlen eine Therapie mit Immunsuppressiva („second line“), wenn durch die Behandlung mit Steroiden keine Symptomlinderung erzielt werden kann oder diese zu unerwünschten starken Nebenwirkungen geführt hat. Heutzutage wird dabei Methotrexat der Vorzug vor Azathioprin gegeben, was unseres Erachtens an der selten sorgfältig beachteten Lebertoxizität liegt. Falls auch hier eine Wirkung ausbleibt, sollte Infliximab zusätzlich gegeben werden.
Darüber hinaus gibt es in der Hand von Experten eine Reihe weiterer Off-Label- Therapie-Optionen wie Adalimumab, Rituximab, JAK-Inhibitoren als sogenannte „third line therapy“. Bei der kardialen Sarkoidose sollte bei entsprechender Konstellation frühzeitig an den Einsatz von Herzschrittmachern und/oder Defibrillatoren gedacht werden. Hier ist die enge Zusammenarbeit von Kardiologen und Pneumologen wichtig!
Die Therapie-Leitlinie der European Respiratory Society und der European Lung Foundation zur Sarkoidose wurde kürzlich in einer Fachzeitschrift publiziert (Baughman RP et al.: Eur Respir J 2021; doi: 10.1183/13993003.04079-2020).
Rehabilitation bei Sarkoidose
Zur Rehabilitation von Sarkoidosepatienten gibt es nur sparsame Mitteilungen. Das Gros der Betroffenen benötigt zunächst sicher nur eine sorgfältige Diagnostik und ggf. Therapie, aber eine gute Betreuung, um frühzeitige pathologische und psychologischeoder auch therapieinduzierte Veränderungen zu erfassen.
Eine erste systematische Untersuchung zur Rehabilitation, die PROKASARE-Studie, wurde 2019 in Deutschland durchgeführt und zeigte kurz- und mittelfristige positive Resultate bei vielen untersuchten Items, beispielsweise bei Fatigue, der Lebensqualität sowie der körperlichen Fitness. Ein besonderes Augenmerk wurde auf die Trainingstherapie mit Ausdauerbelastungen und Verbesserung der Muskelkraft gelegt. Da die meisten Betroffenen sich im mittleren Lebensalter befinden, ist ein positiver Effekt auf die Arbeit und Erwerbstätigkeit durch eine kompetente Rehabilitation von großer Bedeutung.
Fazit
Seit über 150 Jahren beschäftigt die Sarkoidose die medizinische Welt. Sie hat in dieser Zeit wenig von ihrer Faszination verloren. Unser Verständnis für ihre Verursachung, ihren genetischen Hintergrund, die zugrunde liegenden Pathomechanismen und ihre klinische Präsentation sind gewachsen. Die Erkenntnis, dass die Sarkoidose nicht selten einen komplizierten und im Einzelfall prognostisch ungünstigen Verlauf nehmen kann, hat sich durchgesetzt. Die letzten 20 Jahre waren besonders geprägt von einer außerordentlich innovativen Bildgebung und verbesserten pharmakologischen Interventionen mit der Einführung von „Second“- und „Third line“-Therapien bei refraktären Krankheitsverläufen.
Wegen der Beschränkung des Artikels auf die Entwicklungen der letzten beiden Jahrzehnte ist es den Autoren wichtig zu betonen, dass es weiterhin bei der Betreuung von Sarkoidosepatienten einer subtilen Anamneseerhebung und sehr sorgfältiger klinischer Untersuchung bedarf. Schon beim Erstkontakt kann dadurch der richtige diagnostische Weg festgelegt und vielfältige zeitraubende und kostenintensive Spezialdiagnostik vermieden werden. Eine gute fachärztliche Betreuung, nicht selten von mehreren Fachdisziplinen gemeinsam, ist bei komplizierten Verläufen notwendig. Eine Rehabilitation mit körperlichem Training und Erlernen von krankheitsspezifischen Strategien zur Bewältigung der individuellen Probleme stellt eine nützliche zusätzliche Option dar.
Literatur:
Literatur bei den Verfasser*innen
Das könnte Sie auch interessieren:
Therapie der obstruktiven Schlafapnoe – eine interdisziplinäre Herausforderung
Die obstruktive Schlafapnoe (OSA) ist mit einem erhöhten kardiovaskulären Risiko belastet. Outcome-Studien für die CPAP-Therapie zeigten jedoch nicht die erwarteten Therapieerfolge. Dies ...
Allergie: wie es beginnt
Allergien sind multifaktorielle Erkrankungen, die in jedem Lebensalter, vornehmlich aber in den ersten Lebensdekaden auftreten. Auch Asthma bronchiale ist eine heterogene, ...