Praktische Dosierungsanpassungen in Schwangerschaft und Stillzeit
Autorinnen:
Andrea Burch, MSc1,3
Verena Gotta, PhD2
1Schweizerische Akademie für Perinatale Pharmakologie (SAPP), Zürich
2Universitäts-Kinderspital beider Basel, UKBB
Pädiatrische Pharmakologie & Pharmakometrie
3Spitalapotheke Universitätsspital Zürich
E-Mail: andrea.burch@usz.ch
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Während der Schwangerschaft wie auch postpartal kann es zu signifikanten pharmakokinetischen Änderungen kommen. Das optimale Vorgehen hinsichtlich der Dosisanpassung ist jedoch klinisch nur für wenige Substanzen untersucht, was in Beispielen beleuchtet wird. Pharmakometrische Computermodelle werden in Zukunft mehr und mehr die Formulierung von Dosierungsempfehlungen auf Basis von minimalinvasiven klinischen oder virtuellen Studien unterstützen.
Keypoints
-
Oft werden bei Schwangeren niedrigere Plasmaspiegel von Arzneimitteln im Vergleich zu Nichtschwangeren beobachtet, was das Risiko für Wirkungsabschwächung oder verkürzte Wirkzeiten birgt.
-
Dies erfordert ein enges Monitoring und/oder möglicherweise eine Anpassung der Dosis respektive des Dosisintervalls während der Schwangerschaft (zum Erhalt der gewünschten Wirkung) sowie postpartal (zur Prävention von dosisabhängigen unerwünschten Wirkungen).
-
In der Nutzen-Risiko-Abwägung bezüglich Dosisänderung ist auch das ungeborene beziehungsweise gestillte Kind zu berücksichtigen.
-
Pharmakometrische Modelle erlauben es, Vorhersagen von Kinetikänderungen und deren Variabilität in Schwangerschaft und Stillzeit quantitativ zu formulieren, selbst wenn noch wenige oder keine klinischen Daten dazu vorliegen.
Pharmakokinetische Änderungen in Schwangerschaft und Stillzeit
Physiologische Adaptationen während einer Schwangerschaft und postpartal passieren bei der Mutter, aber auch beim Kind respektive Ungeborenen.1–3Weitere Ausführungen hierzu finden Sie im Beitrag «Pharmakotherapie bei der Frau, bei Schwangeren und Stillenden – mehr als eine Genderfrage» .
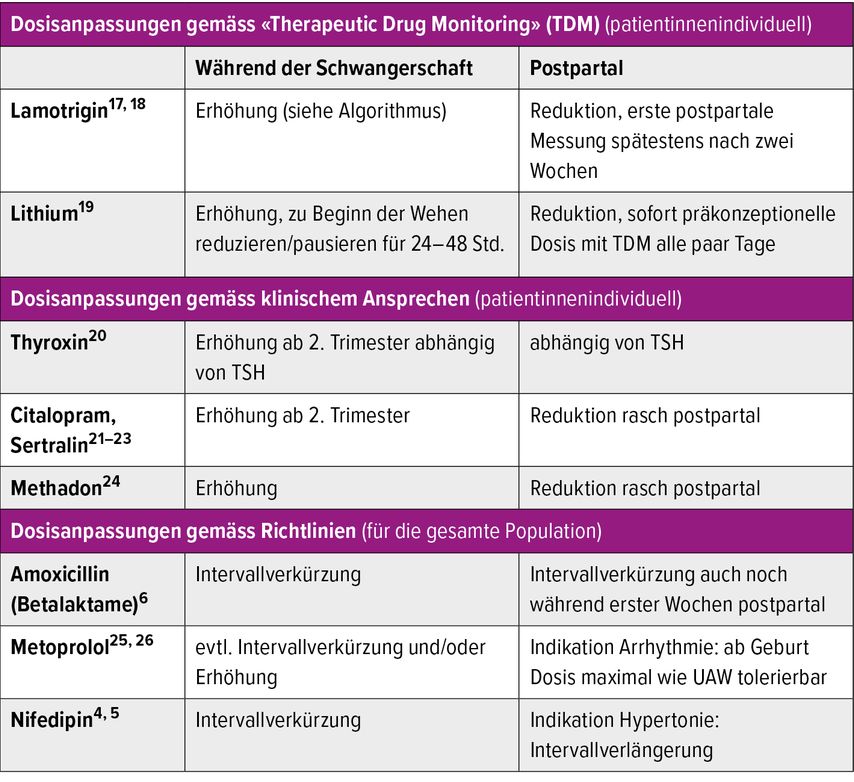
Da sich entsprechend die Frage nach Dosisanpassungen während und nach der Schwangerschaft stellt, werden im Folgenden zunächst klinische Beispiele zur mütterlichen Dosisanpassung illustriert (Tab. 1), gefolgt von einer Diskussion zur Nutzen-Risiko-Abwägung und Forschungsentwicklung mittels Pharmakometrie.
Tab. 1: Beispiel von Dosisanpassungen gemäss «Therapeutic Drug Monitoring» (TDM), klinischem Ansprechen oder gemäss Richtlinien. TSH = Thyroidea stimulierendes Hormon
Ansätze zur mütterlichen Dosisanpassung
Schwangerschaftsbedingte Medikation – Beispiel Nifedipin
Bei Indikation einer antihypertensiven Therapie mit Nifedipin in der Schwangerschaft ist zu beachten, dass die Clearance über CYP3A4 in der Schwangerschaft erhöht ist, was mit einer verkürzten Eliminationszeit von Nifedipin einhergeht.4,5 Dies kann zu Wirkverlusten im Lauf des Tages führen. Dem kann entgegengewirkt werden, indem das Dosierungsintervall verkürzt wird. Die so erreichten konstanteren Arzneimittelspiegel und stabileren Blutdruckwerte werden auch mit einer besseren Verträglichkeit assoziiert, insbesondere beim Einsatz als Tokolytikum bei grundsätzlich normotonen Frauen, welche stärker unter Kopfschmerzen aufgrund von Nifedipin-assoziierten Blutdruckschwankungen leiden.
Schwangerschaftsunabhängige Medikation – Beispiel Penicillin G bzw. Betalaktame
Betalaktamantibiotika erreichen ihre maximale Wirksamkeit bei möglichst konstanten Plasmakonzentrationen über der minimalen Hemmkonzentration (MHK) des zu eradizierenden Pathogens. Aufgrund des erhöhten Verteilungsvolumens wie auch der erhöhten renalen Clearance von Penicillinen in der Schwangerschaft soll Penicillin G zur Behandlung von Streptokokken-B-positiven Frauen unter Geburt in einem verkürzten Intervall verabreicht werden, um effektive Wirkspiegel zu erreichen.6,7
Vorbestehende mütterliche Therapie – Beispiel Lamotrigin
Plasmakonzentrationen des Antiepileptikums Lamotrigin sinken im zweiten und dritten Trimenon bei gleichbleibender Dosierung nachweislich ab.8 Dies ist insofern relevant, als ein Konzentrationsabfall um mehr als 35% ein Prädiktor für eine erhöhte Anfallsfrequenz ist.9 Postpartal wiederum steigen die Plasmakonzentrationen an. Dies kann bei unterlassener Dosierungsanpassung zu Überdosierungssymptomen führen. Eine individuell ander Patientin orientierte Dosisanpassung entsprechend der Plasmakonzentrationsmessung («Therapeutic Drug Monitoring», TDM) wird daher empfohlen.
Mütterliche Therapie mit Relevanz für das ungeborene Kind – Beispiel antiretrovirale Therapie
In den letzten Jahren gab es mehrere Untersuchungen, welche einen Abfall der Arzneimittelexposition im Plasma bei Schwangeren unter antiretroviraler Therapie mit Darunavir, Elvitegravir und dem Booster Cobicistat beschrieben haben, insbesondere im zweiten und dritten Trimenon.10,11 Dies wird durch einen erhöhten hepatischen Metabolismus über Cytochrom-P450-Enzyme begründet. Die reduzierte Exposition erhöht theoretisch das Risiko für ein Therapieversagen mütterlicherseits, aber auch das Risiko für eine Mutter-Kind-Übertragung.12,13 Aktuell gibt es jedoch noch keine tatsächlichen Fallberichte dazu, und der adäquate Ansatz zur Dosisanpassung bleibt unklar.
Nutzen-Risiko-Abwägung für das Kind
Ob und in welcher Dosierung eine medikamentöse Therapie in und nach der Schwangerschaft am besten erfolgen soll, ist eine Nutzen-Risiko-Abwägung für Mutter und Kind, unter Berücksichtigung von bekannten und unbekannten Risiken während Schwangerschaft und Stillzeit. Ideal ist ein prospektives Management ab Kinderwunsch respektive bei Beginn der Therapie in der Schwangerschaft. Beispielsweise muss in der Schwangerschaft unter einer antidepressiven Therapie mit Citalopram das Risiko für einen Wirkverlust gegen das Risiko für Anpassungsstörungen des Neugeborenen nach Geburt abgewogen werden. Postpartal kommt es zu physiologischen Änderungen bei Mutter und Kind, die bei Beurteilung der Stillkompatibilität nebst dem Übergang der Arzneimittel in die Muttermilch zu berücksichtigen sind. Beispielsweise sinken beim gestillten Säugling gemessene Citalopram-Plasmakonzentrationen innerhalb der ersten zwei Lebensmonate bei konstanter Citalopram-Milchkonzentration um mehr als den Faktor 20 ab,14 unter anderem durch eine stetig steigende Eliminationskapazität des Säuglings.
Pharmakometrische Dosierungsempfehlung bei mangelnden Daten
Idealerweise liegen den Dosierungsempfehlungen in Schwangerschaft und Stillzeit klinische Daten zur Dosis-Expositions-Beziehung (Pharmakokinetik), Wirksamkeit und Sicherheit zugrunde. Solche Daten für Mutter und Kind zu erheben ist in der Praxis jedoch oft nicht oder nur schwer möglich. Während Daten zur Sicherheit im Rahmen der Teratovigilanz bereits möglichst systematisch erfasst werden, fehlen häufig Daten zur Pharmakokinetik und zur davon abhängigen Wirksamkeit.
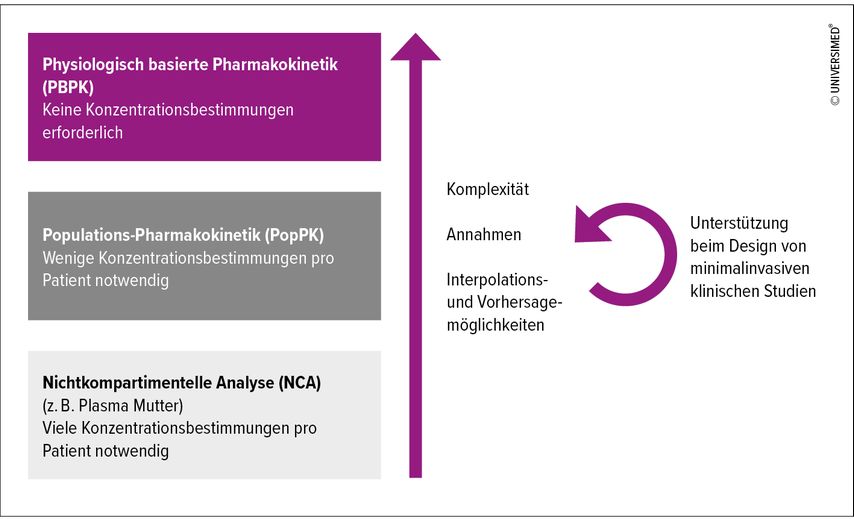
Sogenannte pharmakometrische Ansätze unterstützen hier die quantitative Vorhersage von Kinetikänderungen während Schwangerschaft und Stillzeit unter Verwendung einer möglichst minimalen Anzahl von klinisch-invasiven Messungen der Arzneimittelkonzentration bei Mutter und Kind (Abb. 1): Im Vergleich zur klassischen nichtkompartimentellen Analyse, die viele Konzentrationsbestimmungen pro Patient erfordert, kommt die Analyse mittels Populationspharmakokinetik mit wenigen Konzentrationsbestimmungen pro Patient aus. Zusätzlich können relevante Informationen zur inter- und intraindividuellen Variabilität sowie zu physiologischen Vorgängen gewonnen werden.15 Komplexe Modelle der physiologisch basierten Pharmakokinetik erlauben ausserdem Vorhersagen allein aufgrund von bekannten «systemspezifischen» physiologischen Parametern in der Schwangerschaft oder beim Säugling (z.B. Herzzeitvolumen und Organperfusion, glomeruläre Filtrationsrate, hepatische Enzymaktivität) im Zusammenspiel mit bekannten «wirkstoffspezifischen» Eigenschaften (z.B. physiko-chemische Eigenschaften, Affinität zu bestimmten Enzymen).16 Die Zahl der Arzneimittel, die mittels Pharmakometrie charakterisiert werden, steigt stetig. Dies unterstützt die Formulierung von Dosierungsansätzen und das Design von weiteren klinischen Studien zur Evaluation von physiologischbasierten Vorhersagen.
Abb. 1: Pharmakometrische Ansätze zur Vorhersage und Quantifizierung von Kinetikänderungen während und nach der Schwangerschaft beziehungsweise Stillzeit (adaptiert und modifiziert nach van Hasselt JG et al.).27Durch Integration von bekannten physiologischen und arzneimittelspezifischen Parametern (Annahmen) in Modelle steigender Komplexität lässt sich die Notwendigkeit von invasiven klinischen Messungen (z.B. Plasmakonzentrationsbestimmung) reduzieren und eine Erwartung der Arzneimittelexposition in verschiedenen Verteilungsräumen (z.B. Plasma, Fetus, Milch, Neugeborenes) formulieren, welche durch minimalinvasive klinische Studien evaluiert werden können
Literatur:
1 Ito S: Mother and Child: Medication use in pregnancy and lactation. Clin Pharmacol Ther 2016; 100(1): 8-11 2 Constantine MM: Physiologic and pharmacokinetic changes in pregnancy. Front Pharmacol 2014; 5:65 3 Palahniuk RJ et al. Pregnancy decreases the requirement for inhaled anesthetic agents. Anesthesiology 1974;41:82-3 4 ter Laak MA et al.: Pharmacokinetics of nifedipine slow-release during sustained tocolysis. Int J Clin Pharmacol Ther 2015; 53(1): 84-91 5 Silberschmidt A-L et al.: Nifedipine concentration in maternal and umbilical cord blood after nifedipine gastrointestinal therapeutic system for tocolysis. BJOG 2008; 115(4): 480-5 6 Andrew MA et al.: Amoxicillin pharmacokinetics in pregnant women: modeling and simulations of dosage strategies. Clin Pharmacol Ther 2007; 81(4): 547-56 7 Johnson JR et al. Optimal dosing of penicillin G in the third trimester of pregnancy for prophylaxis against group B Streptococcus. Am J Obstet Gynecol 2001;185:850-3 8 Franco V et al.: Changes in lamotrigine pharmacokinetics during pregnancy and the puerperium. Ther Drug Monit 2008; 30(4): 544-7 9 Pennell PB et al.: Lamotrigine in pregnancy: clearance, therapeutic drug monitoring, and seizure frequency. Neurology 2008; 70(22Pt2): 2130-6 10 Momper JD et al.: Elvitegravir/cobicistat pharmacokinetics in pregnant and postpartum women with HIV. AIDS 2018; 32(17): 2507-16 11 Momper JD et al.: Pharmacokinetics of darunavir and cobicistat in pregnant and postpartum women with HIV. AIDS 2021; 35(8): 1191-9 12 Swissmedic: DHPC – Genvoya® (Elvitegravir/Cobicistat/Emtricitabin/Tenofoviralafenamid)/Stribild®(Elvitegravir/Cobicistat/Emtricitabin/Tenofovirdisoproxil)/Tybost® (Cobicistat). Verfügbar unter https://www.swissmedic.ch/swissmedic/de/home/humanarzneimittel/marktueberwachung/health-professional-communication--hpc-/dhpc_evgcobi_pregnancy.html ; zuletzt aufgerufen am 14.22024 13 Swissmedic: DHPC – Prezista® (Darunavir). Verfügbar unter https://www.swissmedic.ch/swissmedic/de/home/humanarzneimittel/marktueberwachung/health-professional-communication--hpc-/dhpc-prezista_darunavir.html ; zuletzt aufgerufen am 14.2.2023 14 Heikkinen T et al.: Citalopram in pregnancy and lactation. Clin Pharmacol Ther 2002; 72(2): 184-91 15 Gotta V et al.: [Understanding and reducing the risk of adverse drug reactions in pediatric patients]. Ther Umsch 2015; 72(11-12): 679-86 16 Dallmann A et al.: Physiologically based pharmacokinetic modeling in pregnancy: a systematic review of published models. Clin Pharmacol Ther 2018; 104(6): 1110-24 17 EURAP Study Group: Seizure control and treatment in pregnancy: observations from the EURAP epilepsy pregnancy registry. Neurology 2006; 66(3): 354-60 18 Sabers A: Algorithm for lamotrigine dose adjustment before, during, and after pregnancy. Acta Neurol Scand 2012;126:e1-4 19 Wesseloo R et al.: Lithium dosing strategies during pregnancy and the postpartum period. Br J Psychiatry 2017;211:31-6 20 Soldin OP et al.: Therapeutic drug monitoring during pregnancy and lactation: thyroid function assessment in pregnancy-challenges and solutions Ther Drug Monit 2010;32:265-8 21 O’Brien L et al.: Changes in antidepressant metabolism in pregnancy evidenced by metabolic ratios in hair: a novel approach. Forensic Sci Int 2010;196:93-6 22 Freeman MP at al.: Pharmacokinetics of sertraline across pregnancy and postpartum. J Clin Psychopharmacol 2008;28:646-53 23 Sit DK et al.: Changes in antidepressant metabolism and dosing across pregnancy and early postpartum J Clin Psychiatry 2008;69:652-8 24 Ke AB et al.: Expansion of a PBPK model to predict disposition in pregnant women of drugs cleared via multiple CYP enzymes, including CYP2B6, CYP2C9 and CYP2C19 Br J Clin Pharmacol 2014;77:554-70 25 Roston TM et al.: Caring for the pregnant woman with an inherited arrhythmia syndrome. Heart Rhythm 2020; 17(2): 341-8 26 Haas DM, D’Alton M: Pharmacogenetics and other reasons why drugs can fail in pregnancy: higher dose or different drug? Obstet Gynecol 2012; 120(5): 1176-9 27 van Hasselt JGC et al.: The status of pharmacometrics in pregnancy: highlights from the 3(rd) American conference on pharmacometrics. Br J Clin Pharmacol 2012; 74(6): 932-9
Das könnte Sie auch interessieren:
Pharmakotherapie bei der Frau, bei Schwangeren und Stillenden
Die Gabe von Medikamenten bei Frauen, insbesondere bei Schwangeren und Stillenden, erfordert eine sorgfältige Überlegung und Abwägung, da sie nicht nur die Gesundheit der Frau, sondern ...
«Fire Drill» im Kreisssaal
Ein sorgfältig durchgeführter «Fire Drill» kann Leben retten und stellt sicher, dass alle Beteiligten auf den Ernstfall vorbereitet sind. Die Einführung eines «Fire Drill» im Kreisssaal ...
Verbesserung der Ästhetik ohne onkologische Kompromisse
In der Brustchirurgie existiert eine Vielzahl an unterschiedlich komplexen onkoplastischen Operationstechniken mit verschiedenen Klassifikationen. Die kritische Selektion der Patient: ...