Endometriose: Was sollte die Hausärzteschaft wissen?
Autor:innen:
Dr. med. Isabel Ihnenfeld Arcienega
Dr. med. Daniel Passweg
Frauenklinik
Stadtspital Triemli
Zürich
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Endometriose ist häufig und wenn man als Internist:in Frauen zwischen Menarche und Menopause betreut, finden sich darunter Endometriosepatientinnen. Die Endometriose hat eine wichtige Bedeutung, da sie Frauen in ihrer produktiven und reproduktiven Lebensphase betrifft und sie stark einschränken kann, was die Erkennung und Betreuung der Krankheit noch wichtiger macht.
Keypoints
-
Endometriose ist eine chronische, entzündliche, hormonabhängige Krankheit, die bis zur Menopause in ihren verschiedenen Facetten begleitet werden muss. Medikamentöse und chirurgische Therapien können gegeneinander abgewogen und der Situation und den Präferenzen der Patientin angepasst und/oder kombiniert werden.26
-
Wenn man katameniale Schmerzsymptome bei jüngeren Frauen ernst nimmt, ist die Verdachtsdiagnose «Endometriose» mehr als naheliegend. Die Diagnostik ist einfach und beinhaltet zwingend als Erstes einen gynäkologischen Status mit Vaginalsonografie.
-
Medikamentöse Therapien der Endometriose und der «essenziellen» Dysmenorrhö sind über Strecken deckungsgleich (KOK, POP) und können darum probatorisch ohne gesicherte Diagnose eingesetzt werden.
Die Endometriose wird histologisch definiert: Endometriumgewebe, sowohl Epithel wie auch Stroma, siedelt sich ausserhalb des Uteruskavums an und proliferiert. Die Endometriose ist eine chronisch rezidivierende Krankheit, die zu Entzündung, Fibrose und Schmerzen im kleinen Becken führt. Östrogene fördern das Wachstum von endometriotischen Ansiedelungen. Somit ist die Endometriose hormonabhängig und beschränkt sich auf die Geschlechtsreife; in der Menopause verliert sie ihre Bedeutung. Die Endometriose kann in der Regel nicht geheilt werden, unsere Aufgabe ist es vielmehr, die Endometriosepatientinnen therapeutisch zu begleiten.
Die Lebensentwürfe haben sich in der industrialisierten Welt über die letzten 100 Jahre geändert: Die Geburt des ersten Kindes wird mindestens ins 3. Lebensjahrzehnt verschoben; die Anzahl der Kinder pro Frau hat sich reduziert und zusammen mit den kürzeren Stillphasen führt dies dazu, dass sich die Anzahl Menstruationen auf ein Frauenleben berechnet in den letzten 100 Jahren verzehnfacht hat. Die physiologische Amenorrhö durch repetitive Schwangerschaften und lange Stillperioden findet nicht mehr statt und die Endometriose kann sich besser entwickeln.
Zur Unterdrückung der Endometriose war die Entwicklung der Antibabypille durch Carl Djerassi und Gregory Pincus vorteilhaft. Die zunehmende Kritik und Pillenmüdigkeit der letzten Jahre wiederum gab der Endometriose mehr Raum.1 Die Amenorrhö durch eine langfristige Einnahme eines kombinierten oralen Antikonzeptivums (KOK) im Langzyklus (LZ) ist eigentlich wesentlich physiologischer als die berechneten 400 Menstruationen, die eine moderne Frau durchmacht.
Inzidenz
In einer nicht selektierten Population dürfte die Endometriosehäufigkeit bei wenigen Prozent liegen, bei nicht symptomatischen Frauen ist die Inzidenz nicht bekannt. In Risikopopulationen mit chronischen Unterbauchschmerzen und/oder Infertilität liegt sie hingegen im zweistelligen Prozentbereich (40–60%).
Morbidität, Symptome
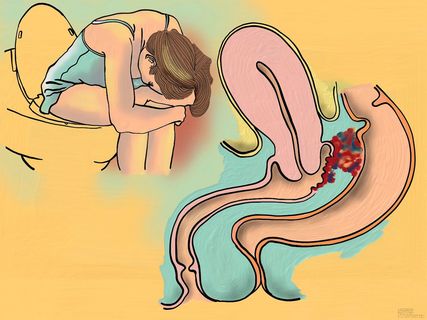
Abb. 1: Katameniale Dyschezie und Dyspareunie bei Endometriosebefall des Rektums und des rektovaginalen Septums
Die Anamnese ist wie so häufig zentral und im hohen Masse diagnostisch.2 Die Endometriose verursacht in erster Linie Schmerzen und in zweiter Linie Infertilität. Die Schmerzen sind typischerweise zyklisch und mit der Menstruation assoziiert. Die «4 D» der Endometriose muss man abfragen: Dysmenorrhö, Dysurie, die Dyschezie (Schmerzen bei der Defäkation) und Dyspareunie, wobei die Dysmenorrhö das Leitsymptom ist (Abb. 1).
Die Infertilität ist neben den Schmerzen das zweite zentrale Symptom der Endometriose. Die Ursachen für eine endometriosebedingte Sterilität sind vielfältig: Verwachsungen im kleinen Becken, verschlossene Tuben, eine verschlechterte ovarielle Reserve, das chronisch-entzündliche Milieu im kleinen Becken oder die Adenomyose des Uterus, die häufig gemeinsam mit einer Endometriose vorkommt. Dadurch wird die Implantation erschwert und es können Aborte getriggert werden (Abb. 2 und 3).
Untersuchung
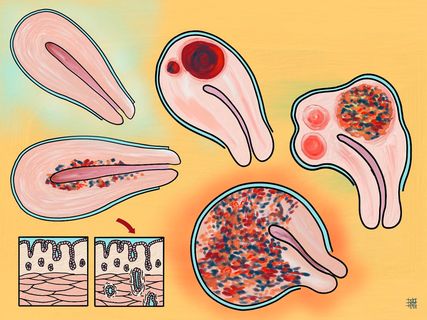
Abb. 3: Die Adenomyose (Endometriose des Myometriums) verursacht eine ausgeprägte Dysmenorrhö und Blutungsstörungen, reduziert aber auch die Implantationsrate und erhöht die Abortrate. Das Bild zeigt die verschiedenen Ausprägungsgrade der Adenomyose
Die klinische Beurteilung beinhaltet eine gynäkologische Untersuchung. Dabei soll ein Einbruch ins hintere Scheidengewölbe erkannt oder ausgeschlossen werden. Ebenso ist eine bimanuelle und rektale digitale Untersuchung in Steinschnittlage nötig, um einen parametranen Befall («deep endometriosis», DE) oder eine ovarielle Endometriose zu ertasten.
Der vaginale Ultraschall ist zentral in der Diagnostik und ist hochsensitiv im Erkennen von ovariellen und tiefen Endometriosen. Die Sonopalpation (Auslösen von Schmerzen?) ist ebenso wichtig wie die Beurteilung der Verschieblichkeit von Organen (Ovarien) und Schichten gegeneinander («sliding sign»). Wurde eine tiefe oder eine ovarielle Endometriose diagnostiziert, ist ein zusätzlicher abdominaler Ultraschall zur Beurteilung der Nieren zum Erkennen oder zum Ausschluss einer Hydronephrose obligat.
Das MRI kann den klinischen und sonografischen Befund gegenlesen und hilft bei der präoperativen Planung, ist aber nur in ausgewählten Fällen, wie beispielweise zum Erkennen eines Befalls der sakralen Spinalnerven, des multifokalen intestinalen Befalls oder einer Zwerchfell-Endometriose, die entscheidende Untersuchung.
Bis vor Kurzem war die Laparoskopie mit Visualisierung der Endometriose und histologischer Sicherung der diagnostische Goldstandard.3 Heute stützt man sich bei der Diagnose auf Anamnese, klinische und vaginalsonografische Befundung und stellt die Indikation zur Laparoskopie nur aus therapeutischen Überlegungen.4 Die rein diagnostische Laparoskopie verschwindet aus den Leitlinien.
Ein moderat erhöhtes CA-125 in der Labordiagnostik ist Ausdruck des chronisch-entzündlichen Beckenperitoneums, ist aber als diagnostisches Element zu unspezifisch. Ein Speicheltest, basierend auf mikroRNA (miRNA), eröffnet seit Kurzem neue Möglichkeiten. Bei Patientinnen mit vorbekannter Endometriose konnte man mithilfe von «next-generation sequencing» (NGS) und künstlicher Intelligenz eine Kombination von 109 miRNA im Speichel definieren. Durch mathematische Optimierung erhält man eine hohe Trennschärfe zwischen der miRNA-Signatur der Patientinnen mit und ohne Endometriose und damit einen Labortest mit sehr hoher diagnostischer Sicherheit. Der Test macht Sinn, wenn eine Patientin an endometriosetypischen Symptomen leidet, aber weder in der klinischen Untersuchung noch im Vaginalultraschall endometriosetypische Befunde erhoben werden können. Bei Patientinnen ohne eindeutige Diagnose, die keine probatorische endokrine Therapie beginnen wollen, bietet sich der Speicheltest als Alternative zur diagnostischen Laparoskopie an. Als reiner Screeningtest ist der Speicheltest nicht nur viel zu teuer (>700.– Fr.), sondern verliert auch an Spezifizität und Sensibilität, da er für ein Schmerzkollektiv entwickelt wurde, in dem die Endometrioseinzidenz naturgemäss sehr hoch ist. Ob der Test ausschliesslich die aktive Endometriose anzeigt oder auch deren genetische Prädisposition, ob er auch die Adenomyose erkennt, ob er als Marker im Verlauf eingesetzt und die Therapie damit überwacht werden kann, wissen wir nicht.5,6
Grundprinzipien der Therapie
Die Endometriose wird medikamentös und/oder chirurgisch behandelt. Voraussetzung jeder Therapie ist die klare Definition des individuellen therapeutischen Ziels: Geht es um die Behandlung von Schmerzen, die aktuelle Erfüllung des Kinderwunsches, die Schmerzbehandlung unter Berücksichtigung eines zukünftigen Kinderwunsches oder ist die Familienplanung abgeschlossen? Nur wenn diese Fragen geklärt sind, lässt sich auch eine langfristige therapeutische Strategie festlegen.
Medikamentöse Therapie, hormonelle Therapie
Da die Endometriose eine hormonabhängige Krankheit ist, besteht die medikamentöse Behandlung immer in einer endokrinen Therapie, die, solange sie eingenommen wird, die Fertilität einschränkt. Andere spezifisch gegen die Endometriose gerichtete Medikamente gibt es nicht. Das therapeutische Ziel der endokrinen Therapie ist die Induktion einer langfristigen Blutungsfreiheit durch die Downregulation der Hypothalamus-Hypophysen-Achse.
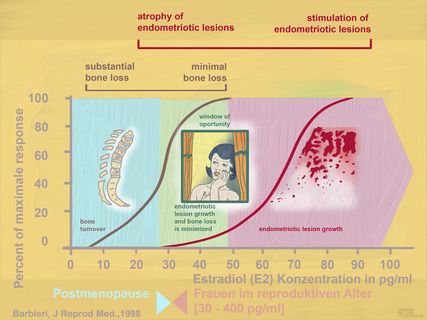
Abb. 4: Endokrine Therapie der Endometriose. Ziel ist ein Serum-Estradiol-Spiegel zwischen 20 und 50pg/ml (= therapeutisches Fenster, «window of opportunity»)
Ausschlaggebend ist das Ausmass der Senkung des Estradiolspiegels (E2) im Serum durch die endokrine Therapie: Senkt man den E2-Spiegel unter 20pg/ml, induziert man zusätzlich klimakterische Beschwerden und eine Reduktion der Knochendichte. Bleibt der E2-Spiegel über 50pg/ml, können Endometrioseherde weiter stimuliert werden. Das interessante therapeutische Fenster («window of opportunity») liegt zwischen 20 und 50pg/ml, in welchem weder Osteoporose induziert noch Endometrioseherde stimuliert werden (Abb. 4).7
Für die Behandlung der Endometriose können orale Gestagene, implantierte Gestagene, Gestagene in intrauterinen «devices» (IUD), kombinierte orale Kontrazeptiva (KOK), GnRH-Analoga und GnRH-Antagonisten eingesetzt werden. Alle endokrinen Therapien sind wirksam, unterscheiden sich aber in den Nebenwirkungen. Um eine hohe therapeutische Adhärenz zu erreichen, ist es zentral, die endokrine Therapie zu begleiten und bei Bedarf anzupassen.
Gestagene
Gestagene reduzieren den Östrogenspiegel über die Hypothalamus-Hypophyen-Achse und wirken auf die Endometrioseherde auch direkt regressiv, antientzündlich, antiangiogenetisch, antineurogenetisch und apoptotisch und reduzieren so die endometriosebedingten Schmerzen. Dienogest (Visanne®) 2mg/d ist für die Endometriosebehandlung zugelassen und Therapeutikum der ersten Wahl. Auch die Langzeitanwendung wird durch Studien breit abgestützt.8 Dienogest führt bei der erwachsenen Frau im Gegensatz zu GnRH-Analoga nicht zur Verminderung der Knochendichte9 und wirkt anders als die KOK nicht thrombogen. Der Einsatz von Dienogest als Antikonzeptivum in der Monotherapie ist «off-label», allerdings entspricht die Dosis von 2mg Dienogest einer doppelten Ovulationshemmdosis und bietet damit in der Langzeitanwendung eine mindestens so hohe Sicherheit wie die Klassiker mit 0,075mg Desogestrel (Cerazette®) oder 4mg Drospirenon (Slinda®). Reine Gestagenpräparate («progesteron-only pills», POP) werden subjektiv gerade von Jugendlichen allerdings häufig mässig gut toleriert. Blutungsstörungen, Brustspannen, Akne, Gewichtszunahme und depressive Stimmungslage gehören zum möglichen Nebenwirkungsprofil.
Levonorgestrel-IUD (z.B. Mirena®) zielen konzeptionell auf einen maximal hohen intrauterinen, aber umgekehrt einen möglichst niedrigen systemischen Gestagenspiegel. Im Off-Label-Use kann man die Levonorgestrel-IUD als Schmerztherapeutikum einsetzen und sie sind logischerweise gerade bei Adenomyose günstig. Bei einer tiefen oder ovariellen Endometriose dürfte der geringe systemische Gestageneffekt nicht ausreichen, um die Krankheit zu kontrollieren.10
KOK (kombinierte orale Kontrazeptiva)
KOK sind als Endometriosetherapeutika «off-label», aber dennoch sehr effektiv in der Behandlung der Dysmenorrhö.11 Subjektiv werden die KOK gut toleriert, sind den jungen Patientinnen vertraut, im Gegensatz zu Dienogest auch offiziell ein Antikonzeptivum, verbessern die jugendliche Haut, haben aber anders als die POP relevante Kontraindikationen und sollen bei Thrombophilie, Adipositas, Nikotinabusus oder Migräne mit neurologischen Ausfällen nicht verwendet werden.12 Zu bevorzugen sind KOK mit Dienogest als Gestagenkomponente (z.B. Valette®). Die Einnahme von KOK im Langzyklus ohne monatliche Pause und damit ohne monatliche Blutung ist in der Endometriosebehandlung logischer.13 Es gibt Hinweise, dass das Ethinylestradiol der KOK den Gestageneffekt konterkariert, sodass das Fortschreiten einer Endometriose nicht suffizient verhindert wird.14
GnRH-Analoga
Die GnRH-Analoga führen zu einer Downregulation der hypophysären Rezeptoren und zu einem hypoöstrogenen Zustand und reduzieren die endometriosebedingten Schmerzen effektiv: Folgen sind allerdings auch klimakterische Beschwerden und eine Verminderung der Knochendichte. Ohne Add-back-Therapie muss man die Injektionen auf ein halbes Jahr beschränken. Heute sind die GnRH-Analoga, obwohl für die Endometriosebehandlung zugelassen, deshalb Zweitlinienmedikamente. Als Add-back eignen sich Östrogene (oral oder transdermal), kombinierte Östrogen-Gestagen-Präparate oder Tibolon (Livial®). Der gewünschte Effekt der GnRH-Analoga auf die endometriosebedingten Schmerzen wird durch die Add-back-Therapeutika nicht gemindert.15
GnRH-Antagonisten
Der oral verabreichbare GnRH-Antagonist Relugolix ist unter anderem in den USA für die Endometriosebehandlung zugelassen. Der therapeutische Effekt ist wie auch die Nebenwirkungen dosisabhängig. Zum Teil wird Relugolix 40mg als fixe Kombination mit Estradiol und Norethisteronacetat als Add-back angeboten (Ryeqo®).16 Wie die GnRH-Analoga sind die GnRH-Antagonisten Zweitlinientherapeutika.
Chirurgische Therapie
Das Konzept der Endometriose als hauptsächlich chirurgisch zu behandelnde Krankheit wird zunehmend verlassen und weicht dem Bild einer chronisch-entzündlichen Krankheit, die bis zur Menopause in ihren verschiedenen Facetten begleitet werden muss. Operieren will man möglichst nur einmalig zum richtigen Zeitpunkt mit definierter Indikation und Zielsetzung mit entsprechender Fachlichkeit. Bei der Operation muss ganz klar sein, welches übergeordnete therapeutische Ziel verfolgt wird. Ist es die maximale Schmerzreduktion, kann ein chirurgisches Konzept diametral anders aussehen, als wenn es um die Verbesserung der Fertilität geht.
Klare Indikationen für eine Operation sind die Ureterendometriose mit Hydronephrose, stenosierende Prozesse am Darm, unklare Dignität eines ovariellen Befundes und Schmerzzustände, die medikamentös nicht kontrollierbar sind.
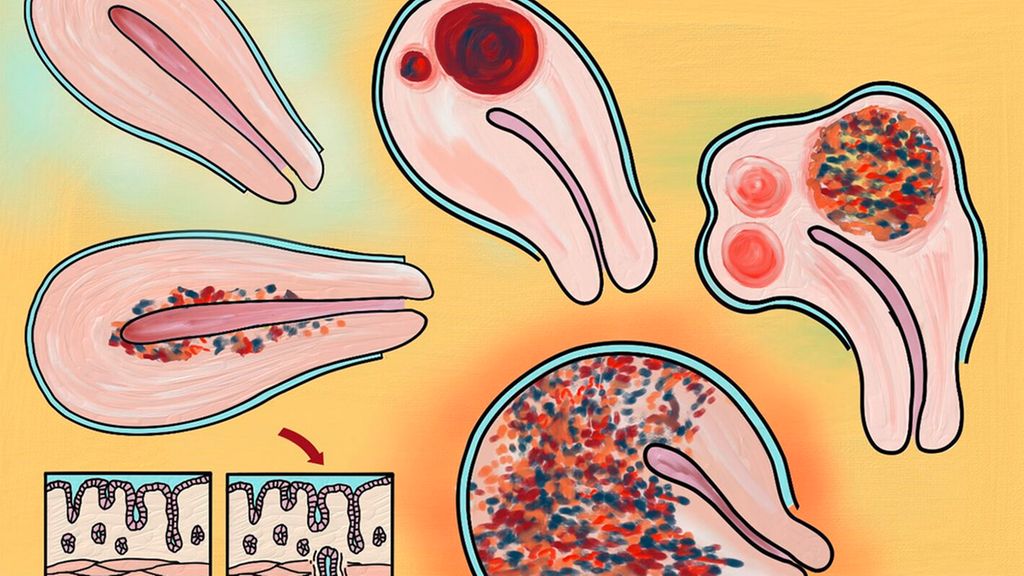
Abb. 5: Endometriome entstehen durch die Invagination von Ovarialkortex, entsprechend gehen bei der Exzision von Endometriomen Kortex und damit Oozyten verloren, die ovarielle Reserve sinkt
Die Entfernung von Endometrioseherden kann vor allem bei niedrigen Endometriosestadien die spontane Schwangerschaftsrate verbessern.17 Geht es um die Umsetzung eines Kinderwunsches, sind fertilitätsmedizinische Massnahmen in der Planung vorauszudenken. Die chirurgische Entfernung von Endometriomen verbessert möglicherweise die spontane Schwangerschaftsrate,18 kann aber die ovarielle Reserve substanziell reduzieren und das Ovar um 10 Jahre altern lassen, weil mit der Resektion der Pseudokapsel des Endometrioms (= invaginiertes Kortexgewebe) die sich darin befindlichen Oozyten mitentfernt werden (Abb. 5).19 Die Lebendgeburtenrate bei In-vitro-Fertilisation wird durch Entfernen von Endometriomen nicht verbessert,20 wird durch eine milde Endometriose nicht reduziert, durch eine ausgeprägte Endometriose hingegen schon.21
Die Exzision tiefer Endometriosen reduziert Schmerzsymptome und verbessert die Lebensqualität.22 Die Chirurgie ist komplex und häufig ist eine interdisziplinäre Chirurgie notwendig. Die Entfernung einer tiefen Endometriose verbessert allenfalls die Fertilität. Bei der chirurgischen Behandlung und derer wissenschaftlichen Aufarbeitung liegt der therapeutische Fokus allerdings auf der Schmerzbehandlung.23
Die Endometriose rezidiviert nach Operationen häufig,24 was nicht nur eine vollständige Exzision, sondern auch eine postoperative medikamentöse Suppressionstherapie mehr als empfehlenswert macht,25 sofern nicht gleich eine Schwangerschaft angestrebt wird.
Literatur:
1 Vercellini P et al.: Oral contraceptives and risk of endometriosis: a systematic review and meta-analysis. Hum Reprod Update 2011; 17: 159-70 2 Ballard KD et al.: Can symptomatology help in the diagnosis of endometriosis? Findings from a national case-control study--Part 1. Bjog 2008; 115: 1382-91 3 AWMF: S2k-Leitlinie Diagnostik und Therapie der Endometriose, Version: 4.0, Stand: 01.09.2020 4 ESHRE Guideline Endometriosis, Issued: 2 February 2022 5 Bendifallah S et al.: Salivary microRNA signature for diagnosis of endometriosis. J Clin Med 2022; 11: 612 6 Eberhard M et al.: Expertenstatement zum Endotest. https://www.sggg.ch/news/detail/expertenstatement-zum-endotest ; zuletzt aufgerufen am 18.8.2023 7 Barbieri RL: Endometriosis and the estrogen threshold theory. Relation to surgical and medical treatment. J Reprod Med 1998; 43: 287-92 8 Römer T: Long-term treatment of endometriosis with dienogest: retrospective analysis of efficacy and safety in clinical practice. Arch Gynecol Obstet 2018; 298: 747-53 9 Strowitzki T et al.: Dienogest is as effective as leuprolide acetate in treating the painful symptoms of endometriosis: a 24-week, randomized, multicentre, open-label trial. Hum Reprod 2010; 25: 633-41 10 Lan S et al.: Analysis of the levonorgestrel-releasing intrauterine system in women with endometriosis. J Int Med Res 2013; 41: 548-58 11 Grandi G et al.: Hormonal contraception in women with endometriosis: a systematic review. Eur J Contracept Reprod Health Care 2019; 24: 61-70 12 Merki-Feld GS et al.: Expertenbrief No 72. Expertenbrief zum Thromboembolierisiko unter hormonaler Kontrazeption. https://www.sggg.ch/fileadmin/user_upload/Dokumente/1_Ueber_uns/1_Verband/2_Arbeitsgemeinschaften/72_Thromboembolierisiko_unter_hormonaler_Kontrazeption_ersetzt_No_35.pdf ; zuletzt aufgerufen am 18.8.2023 13 Muzii L et al.: Continuous versus cyclic oral contraceptives after laparoscopic excision of ovarian endometriomas: a systematic review and metaanalysis. Am J Obstet Gynecol 2016; 214: 203-11 14 Chapron C et al.: Oral contraceptives and endometriosis: the past use of oral contraceptives for treating severe primary dysmenorrhea is associated with endometriosis, especially deep infiltrating endometriosis. Hum Reprod 2011; 26: 2028-35 15 Wu D et al.: Clinical efficacy of add-back therapy in treatment of endometriosis: a meta-analysis. Arch Gynecol Obstet 2014; 290: 513-23 16 Giudice LC et al.: Once daily oral relugolix combination therapy versus placebo in patients with endometriosis-associated pain: two replicate phase 3, randomised, double-blind, studies (SPIRIT 1 and 2). Lancet 2022; 18; 399: 2267-79 17 Hodgson RM et al.: Interventions for endometriosis-related infertility: a systematic review and network meta-analysis. Fertil Steril 2020; 113: 374-82 18 Candiani M et al.: Recurrence rate after „one-step“ CO(2) fiber laser vaporization versus cystectomy for ovarian endometrioma: a 3-year follow-up study. J Minim Invasive Gynecol 2020; 27: 901-8 19 Younis JS et al.: Impact of unilateral versus bilateral ovarian endometriotic cystectomy on ovarian reserve: a systematic review and meta-analysis. Hum Reprod Update 2019; 25: 375-91 20 Hamdan M et al.: The impact of endometrioma on IVF/ICSI outcomes: a systematic review and metaanalysis. Hum Reprod Update 2015; 21: 809-25 21 Hamdan M et al.: Influence of endometriosis on assisted reproductive technology outcomes: a systematic review and meta-analysis. Obstet Gynecol 2015; 125: 79-88 22 Arcoverde FVL et al.: Surgery for endometriosis improves major domains of quality of life: a systematic review and meta-analysis. J Minim Invasive Gynecol 2019; 26: 266-78 23 Bianchi PH et al.: Extensive excision of deep infiltrative endometriosis before in vitro fertilization significantly improves pregnancy rates. J Minim Invasive Gynecol 2009; 16: 174-80 24 Ceccaroni M et al.: Recurrent endometriosis: a battle against an unknown enemy. Eur J Contracept Reprod Health Care 2019; 24(6): 464-74 25 Vercellini P et al.: Post-operative endometriosis recurrence: a plea for prevention based on pathogenetic, epidemiological and clinical evidence. Reprod Biomed Online 2010; 21: 259-65 26 Vercellini P et al.: Medical treatment or surgery for colorectal endometriosis? Results of a shared decision-making approach. Hum Reprod 2018; 33: 202-11
Das könnte Sie auch interessieren:
Antibiotikaresistenz und neue Antibiotika
Resistenzen gegen Antibiotika sind ein zunehmendes Problem und waren 2019 weltweit für rund 1,3 Millionen Todesfälle unmittelbar verantwortlich.1 Wie die Epidemiologie in der Schweiz ...
Herpesvirusinfektionen – ein Überblick
Herpesviren sind weitverbreitet: Mehr als 100 Typen sind bekannt, wovon allerdings nur acht für Menschen infektiös sind. In einem Vortrag im Rahmen des WebUp Allgemeine Innere Medizin ...
«Die Feinde meines Feindes sind meine Freunde»
Wer hätte gedacht, dass wir Viren als unsere Freunde bezeichnen, aber genau das ist bei den Bakteriophagen der Fall. Selbst die heilende Wirkung des Ganges wird mit Bakteriophagen in ...