Systemtherapie des HER2-low fortgeschrittenen Mammakarzinoms
Autor:
Univ.-Prof. Dr.med. Marcus Schmidt
Abteilung für Molekulare Onkologie
Klinik für Geburtshilfe und Frauengesundheit
Universitäres Centrum für Tumorerkrankungen
Universitätsmedizin der Johannes-Gutenberg-Universität
Mainz, Deutschland
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
HER2-low- und HER2-ultralow-Mammakarzinome stellen besondere Herausforderungen dar, da sie sich sowohl in ihrer Prognose als auch im Therapieansprechen von HER2-positiven und HER2-zero- Tumoren unterscheiden. Neue zielgerichtete Therapieoptionen wie Trastuzumab Deruxtecan (T-DXd) bieten vielversprechende Ansätze für diese Patientengruppe. Die Ergebnisse der DESTINY-Breast04- und DESTINY-Breast06-Studien zeigen, dass T-DXd signifikante Vorteile gegenüber Standardtherapien bietet und auch bei HER2-ultralow-Tumoren wirksam ist.1,2 Dieser Artikel gibt einen kurzen Überblick über die Klassifikation, die prädiktive und prognostische Rolle von HER2-low sowie die neuesten Therapieansätze.
Klassifikation von HER2-low
Die Einteilung von HER2 bei Brustkrebs wurde durch neue Erkenntnisse und präzisere Einteilungen differenziert. HER2-low- Tumoren sind durch eine schwache, aber nachweisbare HER2-Expression (1+ oder 2+ ohne HER2-Genamplifikation) gekennzeichnet und wurden traditionell als HER2-negativ bezeichnet.3 HER2-zero-Mammakarzinome ohne immunhistochemische (IHC) Expression von HER2 (IHC0) sind ebenfalls HER2-negativ, während HER2-positive Tumoren eine deutliche HER2-Überexpression (IHC 3+) oder eine Genamplifikation aufweisen. Denkert et al. unterstrichen die Bedeutung dieser Einteilung im Kontext der ASCO/CAP-Leitlinien und zeigten, dass HER2-low eine klinisch bedeutsame Subgruppe innerhalb der HER2-negativen Tumoren darstellt.4 Aktuell wurde im Rahmen der DESTINY-Breast06-Studie die Kategorie HER2-ultralow analysiert, die Tumoren mit schwacher HER2-Expression in <10% der Tumorzellen umfasst.2 64% der Patientinnen mit einem lokalen HER2-IHC0-Score wurden durch einen zentralen Test als HER2-low oder HER2-ultralow eingestuft.5 Es kann daher ratsam sein, HER2-IHC0 erneut zu untersuchen, um eine Eignung für T-DXd zu bestimmen. Da HER2-ultralow derzeit nicht Teil der klinischen Standardpraxis ist, wäre eine erhöhte Aufmerksamkeit für niedrige HER2-Expressionsniveaus wünschenswert.
Prognostische und prädiktive Bedeutung von HER2-low
Eine zentrale Studie zur prädiktiven und prognostischen Rolle von HER2-low führten Denkert et al. durch, wobei sie die klinischen und molekularen Merkmale von HER2-low-Brustkrebs analysierten.4 Diese Studie zeigte, dass HER2-low-Tumoren signifikant häufiger Hormonrezeptor-positiv (HR+) sind als HER2-zero-Tumoren (64,0% vs. 36,7%; p<0,0001). Ausserdem hatten HER2-low-Tumoren eine niedrigere pathologische Komplettremissionsrate (pCR) nach neoadjuvanter Chemotherapie als HER2-zero-Tumoren (29,2% vs. 39,0%; p=0,002). Zusätzlich hatten HER2-low-Tumoren eine bessere krankheitsfreie Überlebensrate (DFS) und Gesamtüberlebensrate (OS) im Vergleich zu HER2-zero-Tumoren. Das OS lag bei HER2-low-Tumoren bei 91,6% im Vergleich zu 85,8% bei HER2-zero-Tumoren (p=0,0016), und das DFS betrug 83,4% vs. 76,1% (p=0,0084). Diese Ergebnisse bestätigen die Bedeutung des HER2-low-Status als eigenständigen prognostischen und prädiktiven Faktor, der bei der Therapieplanung berücksichtigt werden sollte.
Da HER2-low-Tumoren häufig Hormonrezeptor(HR)-positiv sind und daher adjuvant mit endokriner Therapie behandelt werden, ist es naheliegend, dass die bessere Prognose dieser Tumoren mit der endokrinen Behandlung zusammenhängt. Diesem Erklärungsansatz steht die Studie von Almstedt et al. gegenüber.6 Die Autoren untersuchten die Langzeitprognose von HER2-low- und HER2-zero-Tumoren in einer Population von 410 nodal-negativen Brustkrebspatientinnen ohne adjuvante Therapie. Diese Daten sind in diesem Kontext von Bedeutung, da sie zeigen, dass HER2-low-Tumoren eine signifikant bessere Prognose haben als HER2-zero-Tumoren, selbst ohne systemische Nachbehandlung. Die DFS-Rate lag bei HER2-low-Tumoren bei 67,5%, verglichen mit 47,3% bei HER2-zero-Tumoren (p=0,001), und das OS betrug 75,4% vs. 66,8% (p=0,008).
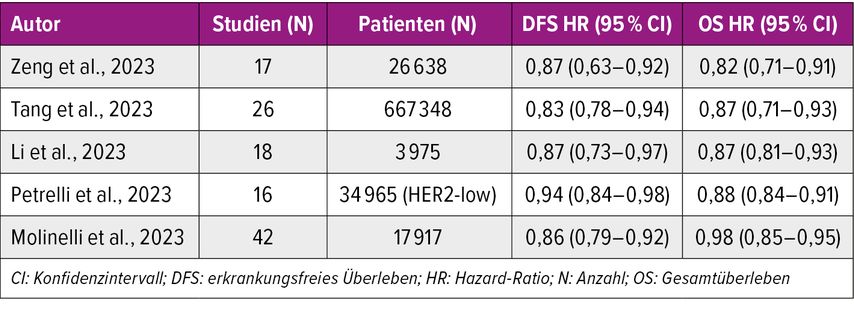
Auch in einer aktuellen Zusammenfassung von systematischen Reviews und Metaanalysen zu HER2-low im Vergleich zu HER2-zero zeigte sich ein verbessertes Überleben bei HER2-low (Tab. 1).7
Tab. 1: Systematische Reviews und Metaanalysen der prognostischen Auswirkungen von HER2-low vs. HER2-zero beim frühen Mammakarzinom7
Die Tabelle verdeutlicht die Unterschiede in der Prognose zwischen HER2-low- und HER2-zero-Tumoren und zeigt, dass HER2-low-Tumoren eine signifikant bessere Prognose aufweisen. Dies könnte für die Therapieplanung relevant sein und unterstreicht die Bedeutung einer genauen Klassifikation des HER2-Status in der klinischen Praxis. Dennoch bleibt die Frage, ob HER2-low tatsächlich eine eigenständige diagnostische Entität darstellt oder ob diese Unterscheidung zukünftig obsolet sein könnte, da erste Studien darauf hindeuten, dass auch HER2-zero-Tumoren möglicherweise von HER2-gerichteten Therapien wie Trastuzumab Deruxtecan profitieren könnten.
Wirkmechanismus von Trastuzumab Deruxtecan (T-DXd)
Trastuzumab Deruxtecan (T-DXd) ist ein Antikörper-Wirkstoff-Konjugat (ADC), das HER2 als Zielstruktur nutzt, um eine hochwirksame Substanz direkt in die Tumorzellen zu transportieren. Der Wirkmechanismus von T-DXd besteht aus mehreren Schritten:8
-
Bindung: Der Antikörperanteil von T-DXd bindet spezifisch an HER2-positive Zellen.
-
Internalisierung und Spaltung: Das ADC wird internalisiert und in den Lysosomen gespalten, was zur Freisetzung des Wirkstoffes, eines Topoisomerase-I-Inhibitors, führt.
-
Zytotoxischer Effekt: Der freigesetzte Wirkstoff induziert eine starke DNA-Schädigung, was zum Zelltod der HER2-positiven Tumorzellen führt.
-
Bystander-Effekt: Durch die Membranpermeabilität des Wirkstoffes kann dieser auch benachbarte HER2-negative Zellen erreichen und schädigen, was besonders bei heterogenen Tumoren von Vorteil ist.
Therapiestudien mit T-DXd beim fortgeschrittenen Mammakarzinom mit geringer HER2-Expression
Die DESTINY-Breast04-Studie untersuchte die Wirksamkeit von T-DXd bei Patientinnen mit metastasiertem HER2-low-Mammakarzinom, die bereits umfangreich vorbehandelt waren.1 Insgesamt wurden 524 Patientinnen in die Studie eingeschlossen und randomisiert entweder mit T-DXd oder einer Standardchemotherapie behandelt. Die Ergebnisse zeigten einen signifikanten Vorteil für die T-DXd-Gruppe hinsichtlich des progressionsfreien Überlebens (PFS) und des Gesamtüberlebens. Das PFS betrug in der T-DXd-Gruppe 9,9 Monate, während es in der Chemotherapie-Gruppe nur 5,1 Monate betrug (HR:0,50; p<0,001). Auch das OS war in der T-DXd-Gruppe länger: 23,4 Monate im Vergleich zu 16,8 Monaten in der Chemotherapie-Gruppe (HR:0,64; p<0,001).
Die prospektive DAISY-Studie untersuchte bei 177 Patientinnen mit metastasiertem Mammakarzinom unter T-DXd die Ansprechrate und das PFS bei verschiedenen HER2-Expressionsniveaus.9 Die Ansprechrate betrug bei HER2-positiven Mammakarzinomen 70,6%, bei HER2-low-Tumoren 37,5% und bei HER2-zero-Tumoren 29,7%, mit einem PFS von 11,1 bzw. 6,7 bzw. 4,2 Monaten. Diese Ergebnisse deuten darauf hin, dass HER2-low- und möglicherweise sogar HER2-zero-Tumoren von T-DXd profitieren können. Der therapeutische Nutzen bei HER2-low- und HER2-zero-Tumoren zeigt die Notwendigkeit einer präzisen Diagnostik und Klassifikation, um Patientinnen für zielgerichtete Therapien besser auswählen zu können.
Die DESTINY-Breast06-Studie untersuchte die Wirksamkeit von T-DXd bei HER2-low- (N=713) und HER2-ultralow- (N=153) Tumoren und konzentrierte sich auf Patientinnen, die bereits mindestens zwei Linien endokriner Therapie erhalten hatten.2 Die Patientinnen wurden randomisiert und entweder mit T-DXd oder einer Standard-Chemotherapie behandelt. Die Ergebnisse zeigten, dass das PFS in der T-DXd-Gruppe bei 13,2 Monaten lag im Vergleich zu 8,1 Monaten in der Chemotherapie-Gruppe (HR:0,62; 95% CI: 0,51–0,74). Auch das OS war in der T-DXd-Gruppe höher (87,6% vs. 81,7%) als in der Chemotherapie-Gruppe. Der Effekt von T-DXd war bei HER2-ultralow vergleichbar.
Fazit
HER2-low- und HER2-ultralow-Tumoren stellen klinisch bedeutsame Subgruppen innerhalb der Brustkrebsklassifikation dar. Die DESTINY-Breast04- und DESTINY-Breast06-Studien haben gezeigt, dass T-DXd eine wirksame und sichere Therapieoption für HER2-low-Tumoren darstellt und dass auch HER2-ultralow-Patientinnen von dieser Therapie profitieren können. Die DAISY-Studie unterstreicht die Möglichkeit, dass DXd auch bei HER2-zero-Tumoren einen Effekt hat, auch wenn dieser geringer als bei HER2-Positivität und bei HER2-low ist. Diese Erkenntnisse betonen die Wichtigkeit einer differenzierten Diagnostik von HER2 und eröffnen neue Perspektiven für die Therapie beim fortgeschrittenen Mammakarzinom.
Literatur:
1 Modi S et al.: Trastuzumab deruxtecan in previously treated HER2-low advanced breast cancer. N Engl J Med 2022; 387: 9-20 2 Bardia A et al.: Trastuzumab deruxtecan after endocrine therapy in metastatic breast cancer. N Engl J Med 2024; doi: 10.1056/NEJMoa2407086. Online ahead of print 3 Denkert C et al.: [New treatment options for metastatic HER2-low breast cancer Consequences for histopathological diagnosis]. Pathologie (Heidelb) 2022; 43(6): 457-66 4 Denkert C et al.: Clinical and molecular characteristics of HER2-low-positive breast cancer: pooled analysis of individual patient data from four prospective, neoadjuvant clinical trials. Lancet Oncol 2021; 22: 1151-61 5 Salgado RF et al.: LBA21 Human epidermal growth factor receptor 2 (HER2)-low and HER2-ultralow status determination in tumors of patients (pts) with hormone receptor–positive (HR+) metastatic breast cancer (mBC) in DESTINY-Breast06 (DB-06). Annals of Oncology 2024; 35 (suppl_2): 1-72 6 Almstedt K et al.: Long-term prognostic significance of HER2-low and HER2-zero in node-negative breast cancer. Eur J Cancer 2022; 173: 10-9 7 Schmidt M et al.: HER2-low and HER2-zero in breast cancer between prognosis, prediction and entity. Oncotarget 2024; 15: 418-20 8 Díaz-Rodríguez E et al.: Novel ADCs and strategies to overcome resistance to anti-HER2 ADCs. Cancers (Basel) 2021; 14(1): 154 9 Mosele F et al.: Trastuzumab deruxtecan in metastatic breast cancer with variable HER2 expression: the phase 2 DAISY trial. Nat Med 2023; 29(8): 2110-20
Das könnte Sie auch interessieren:
Chronischer Pruritus: das heimliche Volksleiden
Eine von fünf Personen der Allgemeinbevölkerung ist in ihrem Leben von chronischem Pruritus (CP) betroffen.1 Der per definitionem für mindestens sechs Wochen bestehende Juckreiz kann zu ...
KI in der Dermatologie
Die Dermatologie zählt zu den Fachgebieten der Medizin, in denen visuelle Befunde eine zentrale Rolle spielen. Die Haut als grösstes Organ des Menschen erlaubt oftmals eine Vorhersage ...
Die menschliche Haut in der modernen Kunst
Dr. Ralph Ubl, Professor für neuere Kunstgeschichte an der Universität Basel, stellte sich der schwierigen Herausforderung, einem Raum voller erwartungsvoller Dermatologen das Organ Haut ...