Update zum Nierenzellkarzinom vom ASCO GU 2025
Autor:
Prim. Priv.-Doz. Dr. Martin Marszalek
Abteilung für Urologie und Andrologie
Klinik Donaustadt, Wien
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Der diesjährige ASCO GU wurde von 14. bis 16.2.2025 in San Francisco abgehalten. Die Veranstaltung hat sich im Laufe vieler Jahre als eine der wichtigsten uroonkologischen Plattformen für die Publikation neuer Studienerkenntnisse und den interaktiven Austausch etabliert. In gewohnt niederschwelligem interaktivem Rahmen wurden auch in diesem Jahr wieder Thematiken zu den wichtigsten uroonkologischen Erkrankungsbildern diskutiert. Einige der interessantesten Präsentationen auf dem Gebiet des Nierenzellkarzinoms sollen im folgenden Überblick beleuchtet werden.
CheckMate 9ER – finale Datenanalyse
Mit einem Follow-up von knapp fünfeinhalb Jahren wurden die finalen Daten der Studie CheckMate 9ER präsentiert. Zur Erinnerung: Diese Studie behandelte Patienten mit metastasiertem Nierenzellkarzinom in der Erstlinie mit einer Kombinationstherapie aus Cabozantinib und Nivolumab verglichen mit Sunitinib. Es zeigte sich in dieser abschließenden Analyse eine langfristige Konsistenz der bereits bekannten Daten: Der Vorteil im progressionsfreien Überleben lag für Patienten im Kombinationsarm bei knapp acht Monaten (HR: 0,58, 16,4 vs. 8,3 Monate). In Bezug auf das Gesamtüberleben zeigte sich ein Vorteil für Patienten im Kombinationsarm mit Cabozantinib und Nivolumab von fast einem Jahr verglichen mit dem damaligen Therapiestandard Sunitinib (HR: 0,79; 46,5 vs. 35,5 Monate). Beachtlich ist die Rate von 13,9% kompletten Remissionen im Kombinationsarm. Das Auftreten unerwünschter Wirkungen blieb auch in der Langzeitanalyse unverändert.
Finale Ergebnisse der COSMIC-313-Studie präsentiert
COSMIC 313 untersuchte die Wirksamkeit von Cabozantinib in Kombination mit Nivolumab und Ipilimumab verglichen mit Nivolumab und Ipilimumab alleine in der Erstlinientherapie des fortgeschrittenen Nierenkarzinoms bei Patienten mit intermediärem oder schlechtem Risikoprofil. In den bisher publizierten Daten konnte ein signifikanter Vorteil im progressionfreien Überleben für die Dreifachkombination gezeigt werden. Daten, welche einen Vorteil im Gesamtüberleben demonstrieren würden, waren bisher ausständig.
In der nunmehr publizierten finalen Analyse der Studie wurden Daten über 855 Patienten publiziert, welche entweder in die Dreifachkombination aus Cabozantinib mit Nivolumab und Ipilimumab (n=428) oder den Kontrollarm mit Placebo, Nivolumab und Ipilimumab (n=427) randomisiert wurden. Der Großteil der Patienten befand sich in der Gruppe mit intermediärem Risiko. Nach einem medianen Follow-up von 45 Monaten konnte der bereits bekannte Vorteil im progressionfreien Überleben für die Dreifachkombination bestätigt werden. Das mediane progressionfreie Überleben lag hier bei 16,6 Monaten in der Dreifachkombination verglichen mit 11,2 Monaten in der. Die Ansprechrate war mit 46% vs. 37% höher in der Gruppe der Dreifachkombination. Den deutlichsten Unterschied im Ansprechen auf die Dreifachkombination gab es im Anteil der Patienten mit progredienter Erkrankung: Nur 8% der Patienten unter der Dreifachkombination zeigten ein Fortschreiten der Erkrankung, verglichen mit 20% unter der Zweifachkombination. Das größte Interesse wurde sicherlich den Ergebnissen in Bezug auf das Gesamtüberleben entgegengebracht, hier zeigte sich jedoch kein signifikanter Vorteil für die Dreifachkombination. Vor diesem Hintergrund muss kritisch betrachtet werden, dass die Dreifachkombination mit 81% versus 62% eine deutlich höhere Rate an Nebenwirkungen – vor allem hepatischen – aufweist. Cosmic 313 zeigte also einen signifikanten Vorteil für die Dreifachkombination aus Cabizantinib, Nivolumab und Ipilimumab verglichen mit der Kombination Nivolumab und Ipilimumab in Bezug auf das progressionfreie Überleben und die Ansprechrate, ein Vorteil im Gesamtüberleben konnte nicht demonstriert werden. Die Nebenwirkungsrate war unter der Dreifachkombination deutlich höher.
Finale Analyse der CALYPSO-Studie bei fortgeschrittenem papillärem Nierenkarzinom und MET-Mutation
Bereits publizierte Phase-II-Daten der CALYPSO-Studie zeigten eine vielversprechende Aktivität von Durvalumab, einem PD-L1-Inhibitor, in Kombination mit Savolitinib, einem MET-Inhibitor, bei Patienten mit fortgeschrittenem papillärem Nierenzellkarzinom mit MET-Mutation. Nach nunmehr 41 Monaten Follow-up war die Ansprechrate 34% in der Intention-to-treat-Population verglichen mit 59% bei Patienten mit MET-Mutation. Das mediane progressionsfreie Überleben war 8,4 Monate verglichen mit 16,7 Monaten bei Patienten mit MET-Mutation. Das mediane Gesamtüberleben war ebenfalls bei Patienten mit MET-Mutation deutlich höher (27,4 vs. 18,3 Monate). Dies entspricht einer Reduktion des Risikos für eine Progression von 64% bzw. einer Reduktion der Gesamtmortalität von 24% in der Gruppe der Patientern mit papillärem Nierenzellkarzinom mit MET-Mutation, welche einen deutlich höheren Benefit von dieser Kombinationstherapie hatten.
Die Rolle zirkulierender Tumorzell-DNA (ctDNA) als prognostischer Parameter wird zurzeit bei unterschiedlichen Tumorentitäten diskutiert. In einer Subanalyse dieser Studie zeigte sich, dass Patienten mit kompletter Remission beziehungsweise partieller Remission eine Reduktion an ctDNA aufwiesen, wohingegen Patienten mit „stable disease“ oder Erkrankungsprogress eine Zunahme an ctDNA aufwiesen. Die Konversion von ctDNA-Positivität zu ctDNA-Negativität unter laufender Therapie („ctDNA clearance“) war mit einem verlängerten progressionfreien Überleben vergesellschaftet. Ein Zusammenhang zwischen Positivität für ctDNA und der Detektion von MET-Alterationen oder PD-L1 Status konnte nicht gezeigt werden. Patienten mit nachweisbarer ctDNA hatten ein deutlich schlechteres Outcome. Das Gesamtüberleben dieser Patienten betrug nur 7,3 Monate verglichen mit 36 Monaten bei Patienten ohne Nachweis von ctDNA. CALYPSO zeigte also einen Vorteil im progressionsfreien Überleben, im Gesamtüberleben so wie auch in der Ansprechrate bei Patienten mit fortgeschrittenem papillärem Nierenzellkarzinom und MET-Mutation unter der Kombinationstherapie aus Durvalumab und Savolitinib. CtDNA könnte zukünftig als prognostischer und gegebenenfalls prädiktiver Marker in Bezug auf Outcome-Parameter wie progressionfreies Überleben und Gesamtüberleben dienen.
Eine weitere, kleine Arbeit zur Rolle der ctDNA als Biomarker bei Patienten mit fortgeschrittenem Nierenkarzinom (Poster 570, Ayanambakkam A et al.) stellte eine retrospektive Analyse bei einer zugegebenermaßen nur geringen Anzahl von 69 Patienten vor. Im longitudinalen Verlauf wurden über den Zeitraum von 2022 bis 2024 insgesamt 229 Serumproben untersucht. Weitere klinische Faktoren, welche in die Analyse eingeschlossen wurden, umfassten den pathologischen Subtyp, das Tumorstadium und -grading sowie die Detektion von sarkomatoiden oder rhabdoiden Features in der Histologie und die Art der systemischen Therapie. Die Analyse der ctDNA wurde in Clearance, Abnahme oder Zunahme der ctDNA stratifiziert. Bei 88% der Patienten lag ein klarzelliges Nierenzellkarzinom vor. 52% der Patienten, welche in diese Studie inkludiert wurden, wiesen ein metastasiertes, 48% ein lokalisiertes Nierenzellkarzinom auf. 76% der Patienten mit lokalisiertem Karzinom erhielten eine adjuvante Therapie mit Pembrolizumab, 11% der Patienten mit metastasiertem Karzinom wiederum waren unter Surveillance. 97% der Patienten mit lokalisiertem Nierenzellkarzinom und negativer ctDNA waren nach einem Follow-up von neun Monaten weiterhin tumorfrei. 61% der Patienten mit metastasiertem Nierenzellkarzinom wiesen zu Therapiebeginn eine ctDNA-Positivität auf, bei 55% dieser Patienten kam es unter laufender Therapie zu einer Clearance der ctDNA (bei zwei Patienten kam es zu einer spontanen Clearance ohne Therapie). Von diesen Patienten blieben 83% nach einem medianen Follow-up von 11,5 Monaten progressionsfrei, zwei Patienten hatten einen Wiederanstieg der ctDNA korrelierend mit einem Erkrankungsprogress. Nach einem medianen Follow-up von 15 Monaten zeigten alle vier Patienten mit radiologisch nachgewiesener Progression einen Anstieg der ctDNA. Die Autoren unterstrichen die Rolle der ctDNA als potenzieller Marker bei Patienten mit metastasiertem Nierenzellkarzinom, nicht nur zur Prognose in Bezug auf das Therapieansprechen, sondern auch zur frühzeitigen Erkennung eines Erkrankungsrelapses nach initialem Ansprechen.
KIM-1: Biomarker bei metastasiertem Nierenzellkarzinom – eine Post-hoc- Analyse von JAVELIN Renal 101
KIM-1 ist ein membranassoziiertes Glykoprotein, das in geschädigten Nierenzellen überexprimiert wird. Studiendaten deuten darauf hin, dass KIM-1 eine spezifische Rolle in der Tumorbiologie beim Nierenzellkarzinom spielt. Eine Post-hoc- Analyse der JAVELIN-Renal-101-Studie (Avelumab und Axitinib vs. Sunitinib bei fortgeschrittenem Nierenzellkarzinom) beschäftigte sich mit der Frage, ob die Baseline-Plasmalevel von KIM-1 und deren Veränderung unter laufender Therapie eine Korrelation mit dem Outcome bei Patienten mit fortgeschrittenem Nierenkarzinom aufwiesen. Hierzu wurde KIM-1 zu Therapiebeginn und unter laufender Therapie gemessen und in hohe, mittlere und niedrige Plasmalevel stratifiziert. In der Gesamtpopulation waren niedrigere KIM-1-Werte zu Therapiebeginn mit einem längeren progressionfreien Überleben (HR: 0,76, 0,58–0,99) und einem längeren Gesamtüberleben (HR: 0,58, 0,38–0,88) verbunden. Die Autoren schlussfolgerten, dass niedrige Plasmalevel von KIM-1 zu Therapiebeginn beziehungsweise eine Abnahme der Plasmalevel unter laufender Therapie mit einer besseren Prognose vergesellschaftet waren (Tab. 1).
Tab. 1: Assoziation des KIM-1-Basiswerts und der Änderung des KIM-1-Wertes unter Behandlung mit dem Outcome in der Studie JAVELIN Renal 101
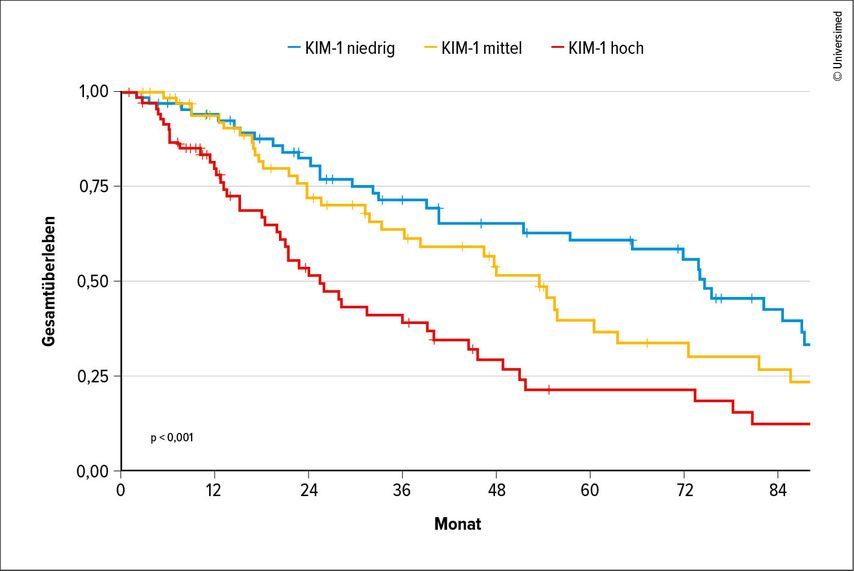
Eine zweite Studie (Poster 582, Steiner C et al) beschäftigte sich ebenso mit einer möglichen Bedeutung von KIM-1 als zirkulierender Tumormarker bei Patienten mit metastasiertem Nierenzellkarzinom. In der Studie wurden ebenso KIM-1-Serumwerte vor Beginn einer systemischen Therapie bei Patienten mit metastasiertem Nierenzellkarzinom bestimmt. Insgesamt wurden 210 Patienten in die Studie eingeschlossen. Patienten mit höheren KIM-1-Werten vor Therapiebeginn hatten ein kürzeres progressionfreies Überleben (p=0,004) und ebenso ein kürzeres Gesamtüberleben (p<0,001). Diese Ergebnisse fanden sich unabhängig vom histologischen Subtyp bei Patienten mit klarzelligem Nierenzellkarzinom ebenso wie bei Patienten mit papillärem Nierenzellkarzinom. Interessanterweise war die prognostische Wertigkeit der Stratifizierung von KIM-1-Serumwerten in Tertilen (hohe, mittlere und niedrige KIM-1-Serumwerte) für das Gesamtüberleben höher als die bekannte IMDC-Risikostratifizierung. Ein Zusammenhang mit anderen nierenschadenassoziierten Molekülen trat nicht zutage, was darauf hinweist, dass KIM-1 vorwiegend aus Tumorgewebe stammt. Die Autoren folgerten, dass KIM-1 mit dem progressionfreien Überleben und dem Gesamtüberleben bei Patienten mit metastasiertem klarzelligem und auch papillärem Nierenzellkarzinom assoziiert war (Abb.1).
KIM-1 wird also zunehmend als prognostischer beziehungsweise prädiktiver Marker in der Behandlung des metastasierten Nierenzellkarzinoms diskutiert und könnte zukünftig eine Rolle in der Prognose des Therapieansprechens und hiermit auch in der Beratung von Patientinnen und Patienten mit fortgeschrittenem Nierenzellkarzinom spielen. Weiters könnte KIM-1 auch in der Überwachung von Patient:innen unter laufender Therapie einen Stellenwert haben, ebenso wie die ctDNA. Damit könnte also endlich Bewegung in die bisher auf dem Stand tretende Landschaft von Biomarkern bei Patient:innen mit metastasiertem Nierenzellkarzinom kommen. Diese nun publizierten Daten heben das Potenzial von ctDNA und auch KIM-1 als Serummarker für eine personalisierte Therapieüberwachung hervor, Validierung und standardisierte Cut-off-Werte sind jedoch für die Integration in klinische Entscheidungsprozesse erforderlich.
Literatur:
beim Verfasser
Das könnte Sie auch interessieren:
AI, EBRT und Co – Zukunft des Stagings beim muskelinvasiven Blasenkarzinom
Im Rahmen des Michael J. Marberger Meetings wurde Zukunftsweisendes zum Einsatz von Artificial Intelligence (AI) beim Blasenkarzinom präsentiert. Es tut sich aber auch einiges abseits ...
Organisiertes Prostatakrebs-Screening inÖsterreich
Das Prostatakarzinom ist die häufigste Krebserkrankung bei Männern in Österreich und eine der Hauptursachen für krebsbedingte Todesfälle weltweit. Die europäischen Leitlinien empfehlen ...
mCRPC – State of the Art, und was kommt 2025?
In den letzten Jahren haben sich neben der Chemotherapie mit Docetaxel und Cabazitaxel und den beiden „new hormonal agents“ (NHA) Enzalutamid sowie Abirateron nun die PARP-Inhibitoren ...