„Entscheidend ist das biologische, nicht das chronologische Alter“
Unser Gesprächspartner:
Priv.-Doz. Dr. Jasmin Bektic, FEBU
Abteilung für Urologie
Medizinische Universität Innsbruck
E-Mail: jasmin.bektic@tirol-kliniken.at
Das Interview führte
Christian Fexa
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Vom Prostatakarzinom sind viele ältere Männer betroffen – ein Teil davon kommt auch mit geriatrischen Problemen oder ist so alt, dass geriatrische Fragestellungen wichtig werden. ÖGU Akuell sprach mit Dozent Jasmin Bektic von der Medizinischen Universität Innsbruck darüber, worauf in diesem Setting besonders zu achten ist.
Was definiert bei der Fragestellung Prostatakarzinom einen geriatrischen Patienten?
Geriatrie kommt aus dem Griechischen und bedeutet Altersheilkunde. Die Gesellschaft für Geriatrie definiert einen geriatrischen Patienten durch die geriatrietypische Multimorbidität und ein höheres Lebensalter – meist 70 Jahre oder älter – oder durch ein Alter von über 80 mit alterstypisch erhöhter Vulnerabilität. Wichtig ist die geriatrietypische Multimorbidität vorrangig vor dem kalendarischen Alter zu sehen – d.h., biologisches Alter geht vor chronologischem Alter.
Das Prostatakarzinom ist, im Unterschied zu anderen Karzinomarten, die von der Malignität her ähnlich sind, ein sehr heterogenes Karzinom. Daher ist die geriatrietypische Multimorbidität beim Prostatakarzinom entscheidend für die Vorgangsweise: Geht man überhaupt in die Diagnostik? Braucht der Patient eine aktive Therapie oder braucht er Beobachtung? Dabei muss man das spezifische Risikopotenzial eines Patienten individuell betrachten und bereits vorliegende Funktionsdefizite berücksichtigen.
Die Population der Patienten, die über 75 Jahre alt sind, wächst schnell. Während die Lebenserwartung eines 75-jährigen Mannes Anfang der 1980er-Jahre 8,5 Jahre war, sind es nun 11,6 Jahre. Der Unterschied von drei Jahren ist viel und auch entscheidend, da die Therapieentscheidung bei einem Prostatakarzinom Sinn hat, wenn der Patient eine Lebenserwartung von über 10 Jahren hat. Man kann also einem Patienten eine Therapie anbieten, obwohl er 75 Jahre alt ist, wenn er eine weitere Lebenserwartung von mehr als 10 Jahren hat – dies ist etwas ganz Typisches für das Prostatakarzinom.
Wie häufig ist das Prostatakarzinom bei geriatrischen Patienten?
Österreichische Daten aus den Jahren 2004 bis 2006 ergaben in der Gruppe der 50–59-Jährigen beim Prostatakarzinom 176 Neuerkrankungen auf 100000 Einwohner; in der Gruppe der 70–79-Jährigen waren es 699. Es ist also ein häufiges Karzinom. In Autopsiestudien bei über 8o-Jährigen wurde sogar sehr häufig ein Prostatakarzinom gefunden. Beim Prostatakarzinom spielt aber die Heterogenität eine wichtige Rolle, denn meist sind diese gefundenen Karzinome wenig maligne. Grob gesagt gibt es ja drei Risikogruppen: jene mit geringem Risiko, jene mit intermediärem Risiko und eine Hochrisikogruppe. Die häufigste ist jene mit geringem Risiko – hier stellt sich die Frage, ob man bei diesen Patienten überhaupt eine weitere Diagnostik macht.
Welche besondere diagnostische Herangehensweise bei geriatrischen Patienten gibt es?
In vielen Leitlinien wird empfohlen, bis zu welchem Alter ein PSA-Test erfolgen sollte – in manchen Leitlinien bis zum 70. Lebensjahr, in manchen bis zum 75. Lebensjahr. Wir in Innsbruck empfehlen ihn bis zum 75. Lebensjahr. Der Grund dafür, dass eine spätere breit eingesetzte PSA-Bestimmung keinen Sinn macht, ist die hohe Prävalenz des Prostatakarzinoms im fortgeschrittenen Lebensalter. Es besteht die Gefahr einer Überdiagnose und eventuellen Übertherapie. Hierin unterscheidet sich das Prostatakarzinom von anderen Karzinomen, bei denen immer solche Bestimmungen unabhängig vom Lebensalter erfolgen.
Wichtig ist es, individuell vorzugehen. Es stellt sich immer die Frage: Was für einen Patienten habe ich vor mir? Ist es ein multimorbider 65-Jähriger, der eine geringere Lebenserwartung hat als ein 80-Jähriger, der noch fit ist? Sehr wichtig ist, dass man über den Patienten alles weiß und man diesen Patienten auch persönlich vor sich hat. Welche Diagnostik Sinn macht, ergibt sich daraus, ob es ein multimorbider Patient ist oder ein Patient mit einer Lebenserwartung von über 10 Jahren.
Es gibt Situationen, in denen man das PSA auch bei morbiden Patienten im fortgeschrittenen Lebensalter bestimmt – wenn z.B. klinische Symptome vorliegen. Etwa bei einem lokal fortgeschrittenen Tumor mit Hämaturie, wenn der Patient nicht Wasser lassen kann, bei Restharnbildung, Hydronephrose oder Hinweis auf Metastasierung – Schwäche, B-Symptomatik, Müdigkeit, Anämie. In diesem Fall geht es in der Diagnostik um die Palliation der Symptomatik.
Inwiefern unterscheiden sich die Tumorcharakteristika bei jüngeren und älteren Patienten?
Eine Studie einer schwedischen Gruppe, aus der Prostate Cancer Database for Sweden, bei Patienten unterschiedlicher Altersgruppen nach dem Gleason Score, hat die Todesursachen untersucht, wenn diese Patienten keine initiale lokale Therapie erhalten. Von den Patienten der Hochrisikogruppe, also Gleason Score 8–10, starben fast alle Patienten, die unter 60 Jahre alt waren, am Prostatakarzinom. Betrachtet man die Gruppe der 75–80-Jährigen bzw. die Gruppe der über 80-Jährigen, dann sterben Patienten der Hochrisikogruppe mit zunehmendem Alter immer häufiger nicht am Prostatakarzinom, sondern an etwas anderem – wie etwa an kardiovaskulären Erkrankungen. Bei Patienten mit niedrigem Risiko kann man überlegen, zu beobachten, ohne eine aktive Therapie zu geben, die möglicherweise Nebenwirkungen hat und die Lebensqualität verschlechtert. Die Studie „Mortality among men with locally advanced prostate cancer managed with noncurative intent“ stellt die Heterogenität – wie alt ist der Patient, wie ist sein biologisches Alter, wie ist seine Lebensqualität – gut dar und auch, was in der Therapieentscheidung überlegt werden muss.
Welche Faktoren spielen in der Therapie bei betagten Patienten eine besondere Rolle?
Gute Tools zur Entscheidungsfindung sind der G8-Screeningbogen oder das Comprehensive Geriatric Assessment, das Patienten in drei Gruppen einteilt: gesund und fit, beeinträchtigt (Englisch: „vulnerable“) oder gebrechlich („frail“). Ein älterer gesunder, fitter Patient sollte die Diagnostik und Therapie bekommen wie jeder andere Patient. Ein älterer beeinträchtigter Patient hat Probleme, die aber möglicherweise mittels Geriatriemedizin so behandelt werden können, dass er wieder in die fitte Gruppe fällt. Dann kann man diesem Patienten eventuell ebenfalls eine Standardtherapie anbieten. Es gibt aber auch die Gruppe gebrechlicher Patienten, bei denen die Situation nicht verbessert werden kann. Bei dieser geht es um die Behandlung der Symptome, weil die aktive Standardtherapie dem Patienten vermutlich keinen Vorteil bringt. Den G8-Screeningbogen verwende ich vor allem bei Patienten mit fortgeschrittenen Prostatakarzinomen.
Wie gehen Sie in der Therapie des lokal begrenzten Prostatakarzinoms vor?
Hier kommen die beiden Faktoren zu tragen, die zuvor öfter Thema waren: die Biologie des diagnostizierten Prostatakarzinoms, d.h. die Risikoeinteilung und die individuelle Gebrechlichkeit. Standardtherapie ist die Beobachtung, die in zwei Gruppen eingeteilt wird: Watchful Waiting und Active Surveillance.
Watchful Waiting ist die reine Beobachtung, z.B. des PSA-Wertes, die rektale Untersuchung und die Kontrolle, wie es dem Patienten geht und ob er Symptome hat oder nicht? Bei Watchful Waiting geht es um die Palliation der Symptome. Bei einem lokal begrenzten Karzinom setzt man dies vor allem bei gebrechlichen Patienten ein.
Active Surveillance bedeutet keine sofortige aktive Therapie, sondern Beobachten, um den Beginn einer aktiven Therapie hinauszuzögern. Beim Patienten wird in regelmäßigen Abständen der PSA-Wert bestimmt und eine Rebiopsie durchgeführt. Dann wird über die weitere Vorgangsweise entschieden. Die beiden Standardoptionen der aktiven Therapie des Prostatakarzinoms sind die Operation oder die Strahlentherapie. Wichtig für die Entscheidung ist das biologische Alter des Patienten. Kann man aufgrund seines biologischen Alters mit einer Lebenserwartung von über 10 Jahren rechnen, und er ist nicht multimorbid, dann kann man die gleiche Therapie anbieten wie einem jungen Patienten. Außerdem spielt auch der Wunsch des Patienten für mich eine wichtige Rolle. Ich erkläre dem Patienten immer, welche Nebenwirkungen welche Therapie haben kann. Wenn sich der Patient trotzdem für eine Therapie entscheidet, weil ihn das Wissen um seine Prostatakrebserkrankung psychisch belastet, würde ich diesem Patienten eine Therapie anbieten, wenn er gesund und fit ist und eine Lebenserwartung von mehr als 10 Jahren hat. Ist das nicht der Fall, würde ich dem Patienten unabhängig von seiner Risikogruppe erklären, was die Therapie bringt und was die Nebenwirkungen sein können. Dann entscheiden wir gemeinsam, was für ihn das Beste ist. Als Beispiel: Mit dem Alter wird der äußere Schließmuskel schwächer, wodurch eine erhöhte Gefahr der Inkontinenz durch die Therapie besteht – erklärt der Patient, dass er das nicht in Kauf nehmen möchte, überlege ich mir eine andere Option. Früher, als ich noch ein junger Assistenzarzt war, galt: bis 70 operieren, ab 70 nicht – dies gibt es heute nicht mehr.
Und was tun bei einem biochemischen Rezidiv?
Kommt es z.B. nach einer Operation zu einem Rezidiv, macht man ein PSMA-PET-CT. Wird in diesem nichts gefunden, aber lokal etwas entdeckt, würde man bestrahlen. Beim geriatrischen Patienten wird die Entscheidung für die weitere Vorgangsweise so getroffen, wie beim lokal begrenzten PCa: beobachten oder gleich Therapie? Die EAU teilt Patienten hierzu in Niedrig- und Hochrisikopatienten ein.
Als Beispiel: Wurde der Patient 1990 operiert und hat er 2022 einen PSA-Wert von 0,2, so ist dieser über die Jahre nur langsam gestiegen, was einem ISUP 3 oder weniger entspricht. Einen solchen geriatrischen Patienten würde ich beobachten.
Ein anderes Beispiel: Ist es ein 60-jähriger Patient, bei dem relativ rasch ein biochemisches Rezidiv aufgetreten ist, aber im PSMA-PET-CT nichts gefunden wird, soll man laut Studien bestrahlen, bevor der PSA-Wert 0,5 ist, weil die Ergebnisse sonst schlechter sind. Ist der Patient dagegen 80 Jahre, hat er einen PSA-Wert von 0,5 und hat er eine hohe PSA-Doubling-Time, dann werde ich ihn vermutlich beobachten.
Man geht bei geriatrischen Patienten also im Großen und Ganzen so vor wie bei nicht geriatrischen, man muss in die Kalkulation aber die aktuelle Situation und Lebenserwartung einrechnen. Das Primäre ist: non nocere. Die Lebensverlängerung ist nicht das Wesentliche. Eine WHO-Definition zur Geriatrie aus dem Jahr 1989 fasst dies prägnant zusammen: Es muss versucht werden, den Jahren Leben zu geben, und nicht dem Leben Jahre.
In der Geriatrie ist es wichtig, die Lebensqualität des Patienten nicht zu zerstören, alle Befunde, nicht nur jene zum Prostatakarzinom, zu berücksichtigen, aber auch das Umfeld, in dem der Patient lebt, seine Psyche, seine Komorbiditäten, die Medikation und Lebenserwartung aufgrund der Komorbiditäten. So kann man ein ganzheitliches Konzept erstellen, das dem Patienten das Höchstmaß an Gesundheit und Wohlbefinden gibt und beim Patienten die geistige und körperliche Vitalität so gut wie möglich erhält.
Wie geht man im Fall eines metastasierten Prostatakarzinoms vor?
Hier ist zu unterscheiden: Ist es ein Low-Volume- oder ein High-Volume-, ein Low-Risk- oder ein High-Risk-Patient? Grundsätzlich geht man im geriatrischen Setting so vor wie im nicht geriatrischen, muss aber nach dem Gesamtzustand des Patienten überlegen, was man in der Therapie macht.
Bei einem metastasierten hormonsensitiven Prostatakarzinom ist heute die Kombinationstherapie die Methode der Wahl und nicht wie früher die Androgendeprivationstherapie als Monotherapie. Bei einem Patienten, der z.B. wegen kardiovaskulärer Erkrankungen viele Medikamente nimmt – und bei dem ich davon ausgehe, dass die Androgendeprivationstherapie bzw. die neue hormonelle Therapie die Situation verschlechtern könnte –, könnte man, wenn es ein Patient ist, der keine Symptome und eine Low-Volume-Erkrankung hat, entscheiden zu beobachten.
Ist es ein Patient mit einer High-Volume-Erkrankung, bei dem ich denke, dass er eine Therapie benötigt, weil sonst seine Lebensqualität aufgrund der ausgeprägten Metastasierung rasch sinken würde, würde man abhängig vom Patienten wahrscheinlich eine Adrgogendeprivationstherapie anbieten – möglicherweise eine Monotherapie, wie man es früher gemacht hat. Man muss berücksichtigen, dass viele dieser Patienten auch schon Symptome haben.
Die neue hormonelle Therapie interagiert mit vielen Medikamenten, etwa bei einer Antikoagulation mit NOAKs – in diesem Fall werden die NOAKs gehemmt. So verliert man die Prophylaxe in Bezug auf seine kardiovaskulären Vorerkrankungen. Bei einem Patienten mit ausgeprägter Osteoporose würde eine Androgendeprivationstherapie die Situation verschlechtern, was bedeutet, dass dieser mit osteoprotektiven Substanzen geschützt werden muss. Geht die Entscheidung in Richtung einer Chemotherapie, ist das G8-Screeningtool ein gutes Hilfsmittel.
Wichtig ist es, diese Patienten durch die Therapie nicht in eine Situation zu bringen, in der die Lebensqualität beeinträchtigt wird und er mehr an der Therapie als an seiner Erkrankung leidet. Notwendig ist also für jeden Patienten ein individuelles Konzept.
Gibt es Spezielles in der Nachsorge?
Die Besonderheit bei geriatrischen Patienten ist die Einteilung in gesunde, fitte Patienten, die leicht beeinträchtigt sind, und Patienten mit schweren Beeinträchtigungen. Dementsprechend kann man die Therapie und auch die Nachsorge organisieren.
Einen gesunden, fitten Patienten würde ich, unabhängig von seinem Alter, kontrollieren.
Bei einem Patienten mit Metastasen und einer Androgendeprivationstherapie wird diese häufig in Abständen von drei Monaten gegeben. Wenn der Patient multimorbid ist, er z.B. weit weg wohnt und der Ambulanzbesuch anstrengend für ihn ist, kann man den Abstand mit einem 6-Monats-Depot verlängern oder eine chirurgische Kastration in Lokalanästhesie anbieten. Bei diesem Patienten wird wahrscheinlich eine Kombinationstherapie nicht möglich sein, weil es sich um einen gebrechlichen Patienten handelt.
Welche Rolle spielen die Psyche bzw. die Wünsche des Patienten?
In Tirol sind viele der Patienten über 75 recht gesund und wünschen sich eine aktive Therapie. Ich bespreche mit den Patienten in jeder Risikosituation immer die Vor- und Nachteile einer Therapie. Natürlich berücksichtige ich seine Wünsche, aber wenn es meiner Meinung nach keinen Vorteil durch die Behandlung eines lokalisierten Karzinoms gibt, dann würde ich sie auch nicht machen.
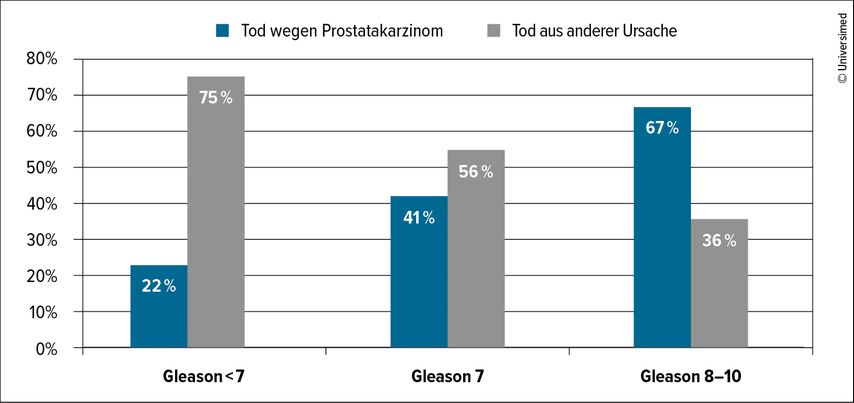
Eine Studie bei 330 Männern im Alter zwischen 70 und 74 Jahren mit Prostatakarzinom hat die Todesursachen – Prostatakarzinom versus eine andere Ursache – unter Active Surveillance oder antiandrogener Therapie untersucht (Abb. 1).
Abb. 1: Todesursachen bei Männern mit Prostatakarzinom und einem Alter von 70–74 Jahren bei Diagnosestellung: Active Surveillance vs. antiandrogene Therapie (nach Bill-Axelson A et al.: Eur Urol 2013: 64: 920-2)
Eingeteilt wurde nach Gleason Score ≤6, 7 und 8 bis 10. Bei einem Gleason Score ≤6 sind 22% am Prostatakarzinom gestorben, 75% an etwas anderem. Bei Gleason Score 7 waren es 41% am Prostatakarzinom und 56% an anderen Ursachen, wobei nicht zwischen Gleason Score 7a und 7b unterschieden wurde, wie man es heute machen würde. Bei Gleason Score 8–10 sind 67% am Prostatakarzinom, 36% an einer anderen Ursache gestorben. Nur in der Gruppe mit einem Gleason Score von 8–10 war das Prostatakarzinom die Haupttodesursache. Diese Tumorbiologie liegt aber nur bei etwa 15% der Prostatakarzinome vor.
Anhand dieser Daten kann man einem z.B. 86-jährigen Patienten mit Gleason Score 6 und einem PSA-Wert unter 10 gut erklären, dass sein Risiko, am Prostatakarzinom zu sterben, extrem niedrig ist – und das ohne medizinische Ausdrücke zu verwenden. Wenn sich ein Vertrauensverhältnis zwischen Patient und Arzt gebildet hat, muss man nicht unbedingt eine aktive Therapie einsetzen, sondern kann auch nur kontrollieren. Für mich steht die Lebensqualität laut dieser WHO-Definition an erster Stelle.
Das könnte Sie auch interessieren:
Aktuelle Entwicklungen und Erkenntnisse beim Urothelkarzinom
Auf dem diesjährigen Genitourinary Cancers Symposium der American Society of Clinical Oncology (ASCO-GU-Kongress) wurden bedeutende Fortschritte in der Diagnose und Behandlung des ...
Aktuelles aus der 7. Version der S3-Leitlinie: wesentliche Leitlinienänderungen
Im Mai 2024 wurde die Prostatakarzinom-S3-Leitlinie unter der Federführung der Deutschen Gesellschaft für Urologie e.V. (DGU) im Rahmen des Leitlinienprogramms Onkologie in ihrer 7. ...
Neues vom ASCO GU zum Prostatakarzinom
Im Rahmen des ASCO GU 2025 in San Francisco wurden eine Vielfalt von neuen praxisrelevanten Studien zum Prostatakarzinom präsentiert. Mit Spannung wurde unter andem auch auf die finalen ...