Ex-vivo-konfokale Laserscanmikroskopie
Autor:
Dr. Mathias Drach
Universitätsklinik für Dermatologie
Medizinische Universität Wien
E-Mail: mathias.drach@meduniwien.ac.at
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Der Chirurgie stehen unterschiedliche Methoden zur Schnellschnittdiagnostik mit unterschiedlichen Vor- und Nachteilen zur Verfügung. Seit einigen Jahren greifen immer mehr Operateur:innen auf die Ex-vivo-Konfokalmikroskopie zurück. Diese Methode überzeugt durch Schnelligkeit, Kosteneffizienz und flexible Einsatzmöglichkeiten, es gibt jedoch bei der Verwendung auch einige Limitationen und Handlungsanweisungen zu beachten.
Moderne (Schnellschnitt-)Diagnostikverfahren lassen sich in drei Gruppen einteilen: die klassische Gefrierschnittmethode,1 die Raman-Technologie2 und die Ex-vivo-Konfokalmikroskopie.3–5
Das Routineverfahren mit der Gefrierschnittmethode findet einen sehr breiten Einsatz im akademischen wie auch im niedergelassenen Bereich in der Pathologie, wo diese Methode den Goldstandard darstellt. Die Raman-Methode ist hochspezialisiert und findet wegen ihres begrenzten Einsatzbereiches nur in ebenfalls hochspezialisierten Abteilungen ihre Anwendung, etwa in der Neurochirurgie.6 Zudem ist der Anschaffungspreis für diese Methode sehr hoch.
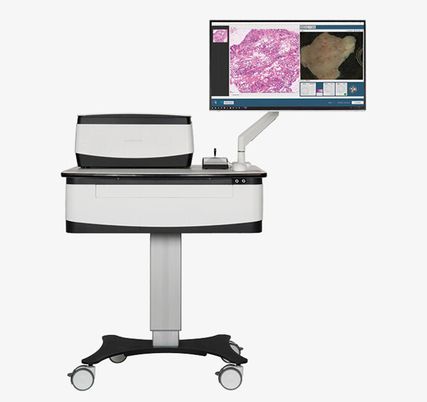
Im Bereich der Dermatochirurgie ist die klassische Gefrierschnittmethode weit verbreitet und speziell im angloamerikanischen Raum im Rahmen der Mohs-Chirurgie stark vertreten. Immer öfter kommt ein alternatives Schnellschnittverfahren zum Einsatz, die sogenannte Ex-vivo-Konfokalmikroskopie. Diese Methode existiert nun seit mehr als 20 Jahren und ist fast ebenso lange in der Routine im Einsatz.4 An unserer Institution arbeiten wir mit dem VivaScope 2500 G4 (Abb. 1) von der Firma Caliber, New York. In Europa ist der Vertrieb durch die VivaScope GmbH, München, gewährleistet. Weltweit sind nach Angaben des Herstellersbereits mehr als 400 Geräte in Verwendung.
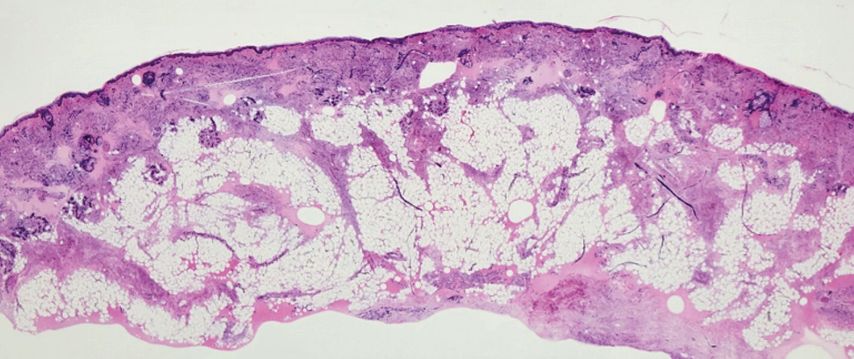
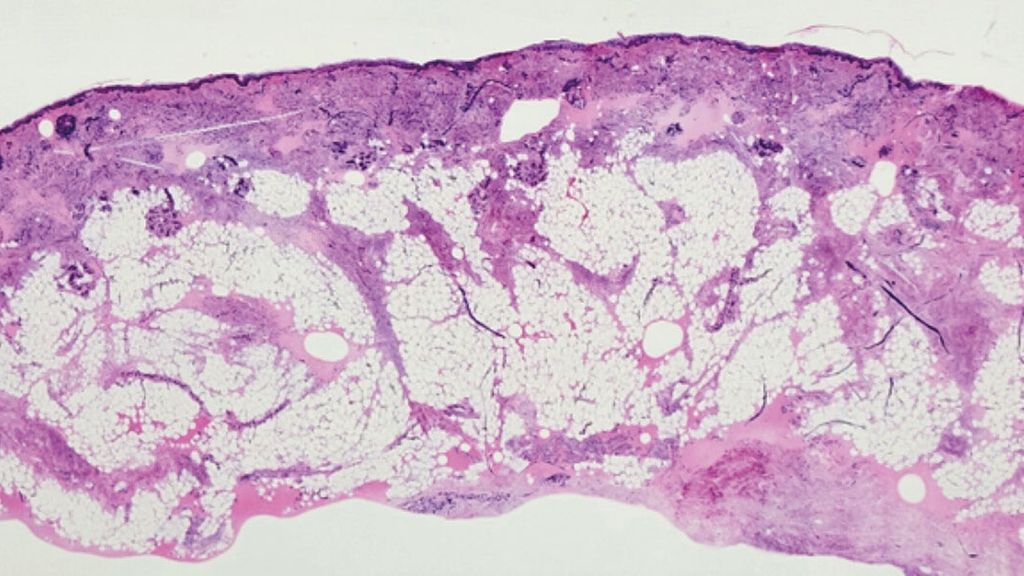
Das Prinzip dieser Methode liegt darin, dass das Ex-vivo-Konfokalmikroskop sowohl im Reflexmodus als auch im Fluoreszenzmodus verwendet werden kann. Letzterer findet an unserer Abteilung Anwendung, hierbei wird das Gewebe nach vorangegangener Vorbehandlung mit Fluoreszenzfarbstoffen mit einem Laser, welcher zwei Wellenlängen emittiert (488nm [blau] und 638nm [rot]), gescannt und das Reflexbild in ein virtuelles HE(Hämatoxylin-Eosin)-Bild umgewandelt (Abb. 2), welches sogleich befundet wird.
Abb. 2: Tumorfreier chirurgischer Resektatrand in der Übersichtsvergrößerung dargestellt mittels Ex-vivo-Konfokalmikroskopie
Da sich das Ex-vivo-Konfokalmikroskop in unmittelbarer räumlicher Nähe zu den Operateuren befindet, können die Resultate unmittelbar mitgeteilt werden.
Methodik
Gewebestücke, die mit der Schnellschnittdiagnostik mittels Ex-vivo-Konfokalmikroskopie beurteilt werden, müssen initial mit 0,9%iger Kochsalzlösung gereinigt werden, damit kein Blut (bzw. so wenig Blut wie möglich) die Untersuchung beeinflusst. Anschließend wird das Gewebe mit 70%igem Alkohol (Abb.3; Nr.1) für wenige Sekunden fixiert und trocken getupft. Im nächsten Schritt erfolgt die Färbung mit den Fluoreszenzfarbstoffen: Das Gewebe wird ca. 50 Sekunden in Acridinorange (Abb.3, Nr.2) gefärbt und trocken getupft. Es folgt die Färbung mit dem zweiten Fluoreszenzfarbstoff Fast Green (Abb.3, Nr.3), ebenfalls für ca. 50 Sekunden. Anschließend wird das Gewebe wieder mit 0,9%iger Kochsalzlösung gewaschen und trocken getupft.
Abb. 3: Schnellschnittarbeitsplatz mit dem VivaScope. 1: 70%iger Alkohol, 2: Acridinorange, 3: Fast Green, 4: Schwämmchen zum Fixieren des Gewebes zwischen Objektträger und Deckglas, 5: Ultraschallgel
Es folgt ein wesentlicher Schritt: Abhängig von der Form des Gewebes müssen nun die zu untersuchenden Flächen vom Operationspräparat abgetrennt werden. Aufgrund der Tatsache, dass an unserer Klinik eine Fadenmarkierung des Operationspräparates meist bei „12 Uhr“ vorgenommen wird, ist zu jedem Zeitpunkt eine Orientierung möglich und erforderlich. Das bedeutet, dass sich die weitere Verarbeitung klar nach der Orientierung richtet und der erste Scanlauf meist die Basis des Resektates erfasst. In weiterer Folge werden die Schnittränder abgetrennt und die Zirkumferenz in zwei Teile geteilt. Im Anschluss erfolgen zwei (Scan-)Läufe, in denen beide Seiten untersucht werden.
Diese Abläufe sind aber nicht immer notwendig, unter bestimmten anatomischen Gegebenheiten, wie z.B. der Ohrhelix, ist es oftmals ausreichend, einen definierten Rand zu untersuchen. Auch sind wir beispielsweise bei größeren Operationspräparaten dazu übergegangen, mehrere Schnittränder gleichzeitig sequenziell abzubilden, was die Untersuchungsgeschwindigkeit erheblich erhöht.
Anschließend wird das Gewebe auf die Objektträger gegeben und mit Schwämmchen (Abb.3, Nr.4) und einem Magnetdeckglas fixiert. Nachdem das Objektiv – zugleich Sender und Empfänger der Laserstrahlen – mit Ultraschallgel (Abb.3, Nr.5) versehen wurde, kann der Scanvorgang begonnen werden. Mögliche Fehlerquellen sind ein Zuviel an Blut, das den Laserstrahl ablenkt, oder Luftblasen, welche den Laser absolut ablenken. Ferner kann ein ungenügend in den Spanngabeln eingespannter Objektträger zu einer Verschiebung des gesamten Bildes führen.
Die Abbildung erfolgt am Bildschirm mit einer Auflösung von maximal 64000 x48000 Pixel. Die Abbildungsqualität ist mit dem eines HE-gefärbten Schnittes vergleichbar und bietet zudem die Möglichkeit, in das Präparat mit einer 550-fachen Vergrößerung zu zoomen.
Gespeichert werden die generierten Daten am lokalen Laufwerk, wo sie auch auf einen fixen Datenträger transferiert werden können, im Idealfall können diese in das krankenhausinterne Netz eingespeist werden.
Goldstandard bleibt, dass das bereits im Schnellschnitt untersuchte Gewebe im Anschluss noch histologisch weiter aufgearbeitet und im Verlauf mit dem Resultat der Ex-vivo-Methode verglichen wird.
Diskussion
Von den drei in der Einleitung erwähnten diagnostischen Verfahren sticht die Ex-vivo-Konfokalmikroskopie durchwegs durch ihre Schnelligkeit heraus; generell ist diese diagnostische Methode etwa doppelt so schnell wie das Schnellschnittverfahren mittels Mohs-Chirurgie.7 Die Geschwindigkeit lässt sich unter anderem auch durch den Wegfall von Fixierschritten erklären.
Ein weiterer Vorteil der Ex-vivo-Konfokalmikroskopie liegt darin, dass dieses Verfahren als „mobiles Labor“ fungieren kann und sehr flexibel örtlich eingesetzt werden kann. Vergleicht man die Kosten der Reagenzien und der verwendeten Materialien, sticht die Methode auch durch ihre Kosteneffizienz hervor. Auch die örtliche Nähe der Diagnostik zum Operationssaal stellt einen wesentlichen Vorteil dar.
Zugleich muss klar hervorgehoben werden, dass die Methode hinsichtlich der Größe der zu beurteilenden Präparate limitiert ist. Die Erfassung von Exzisaten mit einem Durchmesser von >3cm dauert generell länger, wenn beispielsweise für jeden Resektatrand ein extra Scanlauf durchgeführt wird. In unserem Team konnten wir dieses Problem jedoch durch die Implementierung einer sequenziellen Darstellung lösen.
Ferner ist zu beachten, dass die Abbildungsqualität direkt proportional zur Verarbeitungsqualität des Diagnostikers ist: Nur bei optimaler Auflagefläche des Präparates ohne Blutbeimengungen und ohne Luftblasen ist eine ideale Abbildungsqualität gewährleistet. Zudem muss beachtet werden, dass die Festigkeit der zu scannenden Haut von deren ursprünglicher anatomischer Lokalisation abhängig ist: Gesichtshaut ist wesentlich elastischer als die vergleichsweise straffe Haut des oberen Rückens. Die Berücksichtigung der Hautfestigkeit ist unerlässlich für das Einbetten des Gewebestückes auf den Objektträger: Wird vom Objektträger, und konsekutiv mit dem Schwämmchen, zu viel Druck ausgeübt, besteht die Gefahr, dass das Gewebestück verkippt und somit eingeschränkt beurteilbar ist.
Die Stärke der Ex-vivo-Konfokalmikroskopie liegt eindeutig in der Diagnostik von epithelialen Hauttumoren; an unserer akademischen Einrichtung verwenden wir diese Methode nicht in der Diagnostik von melanozytären Läsionen.8 Für die Diagnostik im Formenkreis der entzündlichen Dermatosen haben wir bislang noch keine Erfahrung gesammelt, dies ist jedoch geplant und in der Literatur gut dokumentiert.9
Wer Erfahrung mit der konventionellen (Gefrier-)Schnellschnittmethode hat, weiß, dass in unklaren diagnostischen Situationen weitere Stufenschnitte des bereits aufgefrorenen Gewebes durchgeführt werden können – dies ist mit der Ex-vivo-Konfokalmikroskopie nicht bzw. nur sehr limitiert möglich. Schwierigkeiten können sich mit der Ex-vivo-Konfokalmikroskopie ergeben, wenn beispielsweise an mehreren Stellen gleichzeitig operiert wird – die Möglichkeiten der Verarbeitung und der Diagnostik sind hier begrenzt.
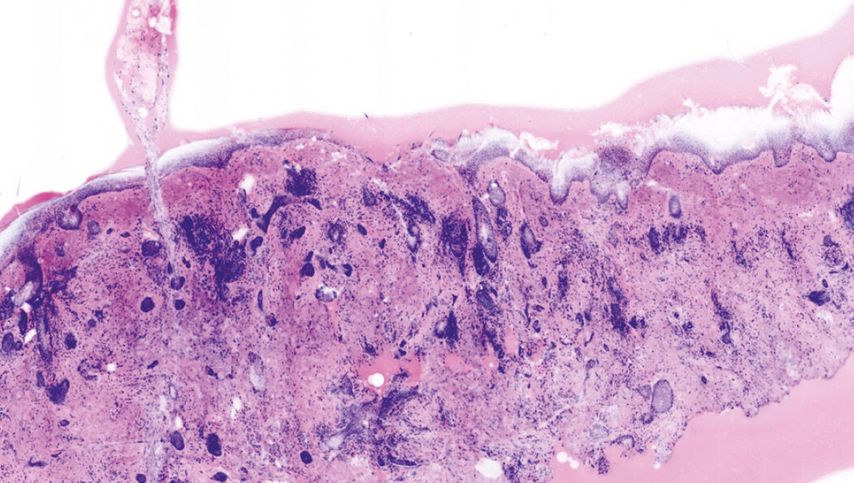
In Hinblick auf die Diagnostik ist das Erkennen der Strukturen denkbar einfach, da wie oben erwähnt die Abbildung stark der eines konventionellen HE-Bildes gleicht. Gute Erfahrungen konnten wir in der Diagnostik knotiger Basalzellkarzinome und von Plattenepithelkarzinomen machen, teilweise schwierig sind infiltrative Basalzellkarzinome zu erkennen (Abb. 4). Hilfreich kann im hier abgebildeten Fall das umgebende Stroma sein, welches einen indirekten Hinweis auf das Vorliegen eines Tumors zeigt.
Abb. 4: Formationen eines infiltrativen Basalzellkarzinoms am chirurgischen Resektatrand
Die Ex-vivo-Konfokalmikroskopie findet neben der Dermatochirurgie Einsatz in einem breiten Feld der Pathologie, etwa in der Urologie, der Gastroenterologie und in der HNO.10,11 Gemäß Literatur schwankt die Spezifität zwischen 91% und 96,5% und die Sensitivität zwischen 73,6% und 92% in der Diagnostik der tumorfreien Schnittränder im Rahmen der Schnittrandkontrolle bei Basalzellkarzinomen.12,13
Literatur:
1 Prickett KA, Ramsey ML: Mohs micrographic surgery. StatPearls [Internet] 2024; verfügbar unter https://www.ncbi.nlm.nih.gov/books/NBK441833/ (zuletzt aufgerufen am 11.12.2024) 2 Nasir-Moin M et al.: Localization of protoporphyrin IX during glioma-resection surgery via paired stimulated Raman histology and fluorescence microscopy. Nat Biomed Eng 2024; 8(6): 672-88 3 Gellrich FF et al.: Ex vivo confocal microscopy speeds up surgical margin control of re-excised skin tumors and greatly shortens in-hospital stay. Cancers (Basel) 2024; 16(18): 3209 4 Bini J et al.: Confocal mosaicing microscopy of human skin ex vivo: spectral analysis for digital staining to simulate histology-like appearance. J Biomed Opt 2011; 16(7): 076008 5 Malvehy J et al.: Ex vivo confocal microscopy: revolution in fast pathology in dermatology. Br J Dermatol 2020; 183(6): 1011-25 6 Hollon TC et al.: Near real-time intraoperative brain tumor diagnosis using stimulated Raman histology and deep neural networks. Nat Med 2020; 26(1): 52-8 7 Leemans G et al.: The introduction of bedside ex vivo confocal microscopy during Mohs surgery of basal cell carcinoma: patient and specialist benefit in an optimized healthcare environment. J Eur Acad Dermatol Venereol 2024; 38(6): e465-6 8 Malvehy J et al.: Ex vivo confocal microscopy: revolution in fast pathology in dermatology. Br J Dermatol 2020; 183(6): 1011-25 9 Hartmann D: Ex-vivo konfokale Laserscanmikroskopie bei melanozytären Läsionen und Autoimmunerkrankungen. Hautarzt 2021; 72(12): 1058-65 10 Titze U et al.: Feasibility study for ex vivo fluorescence confocal microscopy (FCM) on diagnostic prostate biopsies. Quant Imaging Med Surg 2021; 11(4): 1322-32 11 Anker JP et al.: Colonic perforation after piecemeal mucosectomy diagnosed by confocal microscopy. Gastrointest Endosc 2020; 92(4): 971-3 12 Grupp M et al.: Routine application of ex vivo confocal laser scanning microscopy with digital staining for examination of surgical margins in basal cell carcinomas. J Dtsch Dermatol Ges 2021; 19(5): 685-92 13 Ruini C et al.: Ex-vivo fluorescence confocal microscopy with digital staining for characterizing basal cell carcinoma on frozen sections: a comparison with histology. J Biophotonics 2021; 14(8): e202100094
Das könnte Sie auch interessieren:
Long-Acting-Konzepte als Meilenstein in der HIV-Therapie
In den letzten vier Jahrzehnten erfuhr die HIV-Therapie eine enorme Entwicklung und die Optionen für Menschen mit HIV haben sich grundlegend verändert. Aktuell dominiert ein neues ...
Das Mikrobiomvon Wunden und was Probiotika für uns tun können
Unser Darm steht mit einer Vielzahl an Mikroorganismen über unterschiedlichste Funktionsachsen, wie jener zwischen Darm und Haut, mit dem gesamten Organismus in Verbindung. Das Mikrobiom ...
Sexuell übertragbare Infektionen bei Kindern und Jugendlichen
Seit 2019 berichten die World Health Organization (WHO) und die Centersfor Disease Control and Prevention (CDC; USA) regelmäßig über einen dramatischen Anstieg der sexuell übertragbaren ...