Neonatale Erythrodermie: ein potenziell lebensbedrohliches Krankheitsbild
Autorinnen:
Dr. Viktoria Gruber
Priv.-Doz. Dr. Barbara Binder
Universitätsklinik für Dermatologie und Venerologie
Medizinische Universität Graz
E-Mail: viktoria.gruber@medunigraz.at
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Die neonatale Erythrodermie wird definiert als generalisierte Hautrötung oder Dermatitis, welche mindestens 90% der Körperoberfläche betrifft und bereits bei Geburt besteht oder innerhalb der ersten 4 Lebenswochen auftritt. Dieser Artikel beleuchtet einen komplexen Fall einer neonatalen Erythrodermie und bietet Einblicke in mögliche Differenzialdiagnosen und diagnostische Algorithmen.
Keypoints
-
Die neonatale Erythrodermie ist – unabhängig von der Grunderkrankung – potenziell lebensbedrohlich.
-
Betroffene Kinder leiden unter Wärmeverlust, erhöhtem transepidermalem Wasserverlust und haben ein erhöhtes Risiko für transkutane Infektionen.
-
Eine multidisziplinäre Zusammenarbeit (Neonatologie, pädiatrische Dermatologie, Immunologie etc.) und strukturierte frühzeitige Diagnostik sind entscheidend, um die optimale Versorgung betroffener Kinder sicherzustellen.
-
Die langfristige Therapie richtet sich nach der zugrunde liegenden Erkrankung.
Die Bandbreite möglicher Ursachen – von genetischen Erkrankungen, Stoffwechselstörungen bis hin zu Infektionen – kann das behandelnde multidisziplinäre Team vor diagnostische und therapeutische Herausforderung stellen, wie der folgende Fallbericht anschaulich zeigt.
Kasuistik: ein männliches Neugeborenes mit Omenn-Syndrom
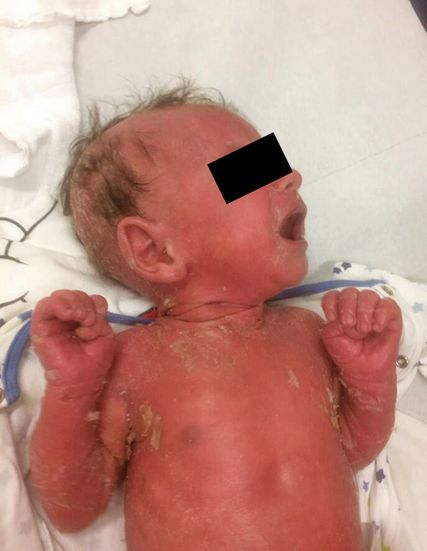
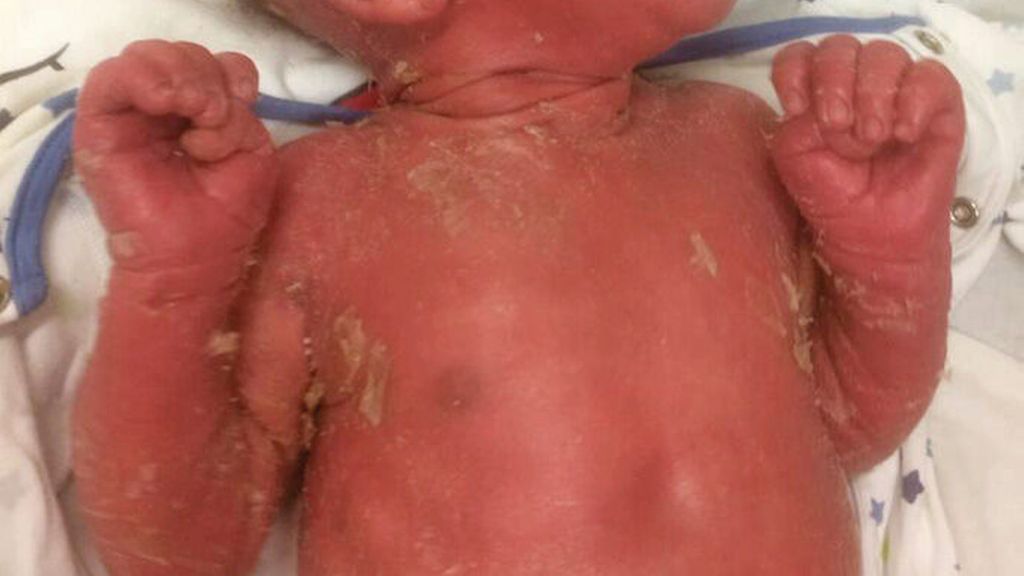
Abb. 1: Erythrodermie mit ichthyosiformer Schuppung bei einem männlichen Neugeborenen mit Omenn-Syndrom
Ein vier Wochen alter Säugling wurde an unserer Universitätshautklinik in Graz aufgrund einer seit Geburt bestehenden Rötung des gesamten Integuments mit begleitender ichthyosiformer Schuppung ohne Blasenbildung vorgestellt (Abb. 1). Die bisherige Behandlung mit topischen Steroiden, rückfettenden Externa und systemischen Antibiotika führte zu keiner Besserung des Hautbildes. Im weiteren klinischen Verlauf entwickelt der Patient zusätzlich eine Gedeihstörung, Durchfälle und schwere rezidivierende systemische Infektionen, weshalb die Verdachtsdiagnose eines primären Immundefekts gestellt wurde.
Die Laboruntersuchungen zeigten eine Hypereosinophilie und erhöhtes Gesamt-IgE. Das Immunscreening ergab negative TREC („T-cell receptor excision circles“) und niedrige KREC („kappa-deleting recombination excision circles“) im peripheren Blut. In der genetischen Untersuchung konnte eine RAG1-Mutation nachgewiesen werden. In Zusammenschau der klinischen Präsentation und der erhobenen Befunde wurde die Diagnose eines Omenn-Syndroms gestellt.
Eine systemische Behandlung mit Cyclosporin A wurde eingeleitet und nachfolgend aufgrund von Nebenwirkungen auf Tacrolimus umgestellt. Nach der HLA-Typisierung erhielt der Patient eine haploidentische hämatopoetische Stammzelltransplantation. Das Hautbild normalisierte sich nachfolgend rasch. Im weiteren klinischen Verlauf entwickelte das Kind jedoch eine akute intestinale und pulmonale Graft-versus-Host-Reaktion sowie eine CMV-Reaktivierung. Aufgrund von respiratorischem Versagen bei Bronchiolitis obliterans und diffuser alveolärer Blutung verstarb das Kind im Alter von 11 Monaten.
Das Omenn-Syndrom stellt eine Sonderform eines schweren kombinierten Immundefekts (SCID) dar.1 Die hämatopoetische Stammzelltransplantation (HSCT) ist derzeit der einzige kurative Therapieansatz.2 Eine immunsuppressive Therapie mit Cyclosporin A kann während der Wartezeit auf eine HSCT zum Einsatz kommen.3 Gentherapeutische Ansätze befinden sich noch in experimentellen Stadien.4,5
Differenzialdiagnosen und diagnostischer Algorithmus
Die Bandbreite möglicher Ursachen der neonatalen Erythrodermie umfassen verschiedene Formen der Ichthyose, Stoffwechselstörungen, Infektionen, Immundefekte, Medikamente und andere Erkrankungen (Tab. 1).
Tab. 1: Übersicht über die wichtigsten Differenzialdiagnosen bei neonataler Erythrodermie (modifiziert nach Cuperus E et al. 2022)6
Eine frühzeitige Diagnostik anhand eines strukturierten Algorithmus in einem multidisziplinären Team ist essenziell, um Patient:innen mit neonataler Erythrodermie optimal zu versorgen. Im Folgenden wird der diagnostische Algorithmus in Anlehnung an Cuperus et al. erläutert.6
Zunächst wird eine ausführliche Anamnese bezüglich Schwangerschaftsverlauf, Familienanamnese (hinsichtlich primärer Immundefekte, Ichthyosen, Atopie und Psoriasis) und Medikamenten erhoben. Häufige medikamentöse Auslöser für eine neonatale Erythrodermie sind Ceftriaxon, Vancomycin und Phenytoin.7 Eine Konsanguinität der Eltern muss berücksichtigt werden, da diese ein erhöhtes Risiko für Ichthyosen, das Netherton-Syndrom, primäre Immundefekte und Stoffwechselerkrankungen birgt.8
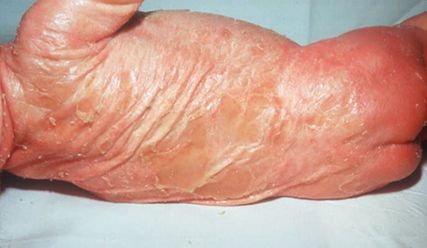
Abb. 2: Neugeborenes mit Kollodiummembran-Ablösung einer universellen pergamentähnlichen Schicht
Die körperliche Untersuchung kann bereits wichtige Hinweise auf die mögliche zugrundeliegende Erkrankung geben. Etwa die Hälfte der Kinder mit neonataler Erythrodermie weisen eine Alopezie auf, welche mit primären Immundefekten oder Stoffwechselerkrankungen assoziiert ist.8 Die Kollodiummembran kann ein begleitendes Symptom bei neonataler Erythrodermie sein und präsentiert sich als pergamentartiger, ölig-glänzender Überzug der Haut (Abb. 2). In der Regel schuppt die Membran meist drei bis vier Wochen nach der Geburt spontan ab.9 Sie tritt überwiegend im Rahmen von Ichthyosen auf, wobei eine generalisierte Kollodiummembran eher mit autosomal-rezessiven kongenitalen Ichthyosen (ARCI) und die partielle Kollodiummembran eher mit syndromischen Ichthyosen einhergeht.10Bei 10% findet sich nach Abschuppung eine normale Haut, hier spricht man vom „self-healing collodion baby“.11 Das Vorliegen einer Schuppung deutet auf Ichthyosen hin. Eine bräunlicheSchuppung ist typisch für die lamelläre Ichthyose (Abb. 3,4), während die Ichthyosis linearis circumflexa, eine girlandenartige doppelte Schuppenleiste, charakteristisch für das Netherton-Syndrom ist.12 Diese tritt allerdings meist erst im Verlauf des Kleinkindalters in Erscheinung.13 Eine fettige gelbliche Schuppung an Kopfhaut und Körperfalten deutet auf eine seborrhoische Dermatitis hin.14 Eine periorifizielle Schuppung findet man häufig beim Holocarboxylase-Mangel, Biotinidase-Mangel oder bei der Acrodermatitis enteropathica (Abb.5).15 Bei Vorliegen einer Collarette-artigen Schuppung mit Pusteln muss an eine kongenitale kutane Candidiasis (CCC) gedacht werden.12 Kommt es zur Blasenbildung, so ist das Vorliegen einer epidermolytischen Ichthyose naheliegend. In diesem Fall verschwinden die Blasen mit der Zeit und werden durch diffuse Hyperkeratosen ersetzt.11
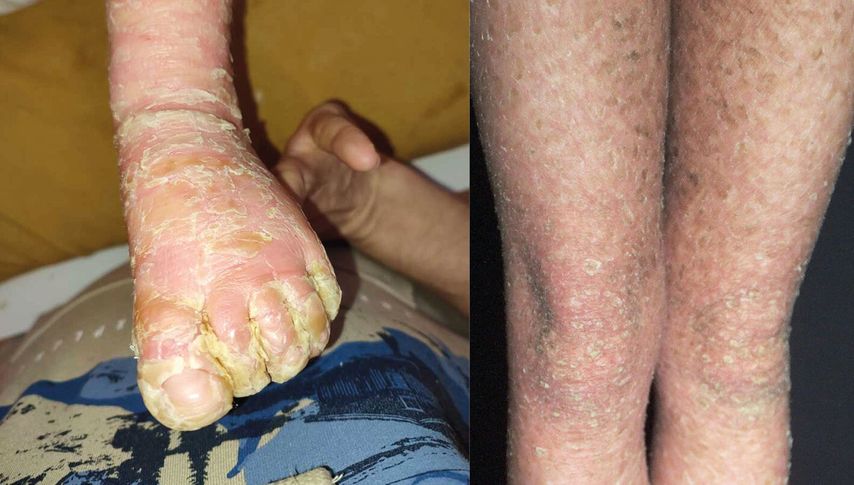
Abb. 3 und 4 (rechts): Hellbräunliche anhaftende Schuppung bei zwei Patientinnen mit lamellärer Ichthyose
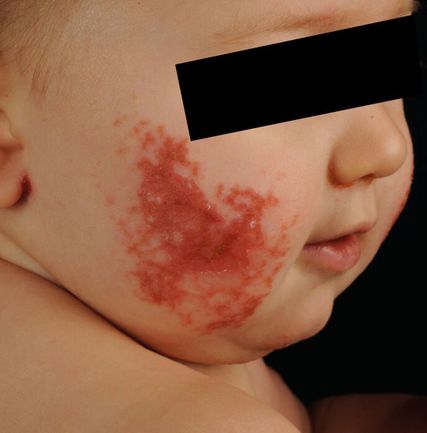
Abb. 5: Periorifizielle netzartige erythematöse Plaques mit Schuppung bei einem Mädchen mit Acrodermatitis enteropathica
Ein weiteres Krankheitsbild, welches mit Blasenbildung einhergeht, ist das „staphylococcal scaled skin syndrome“ (SSSS). Betroffene Kinder leiden zusätzlich unter Fieber und Allgemeinsymptomen. Die Haut präsentiert sich extrem berührungsempfindlich und erinnert durch die großflächige Desquamation an Verbrühungen.16 Bei der diffusen kutanen Mastozytose kommt es ebenfalls zur Blasenbildung nach mechanischer Reibung (positives Darier-Zeichen) und die Haut erscheint diffus induriert („Orangenhaut“).12
Ein Routinelabor (Blutbild, Differenzialblutbild, Serumelektrolyte, Albumin, Harnsäure, Kreatinin, CRP) wird im nächsten Schritt des Algorithmus empfohlen.6 Eine typische Laborkonstellation für das Netherton-Syndrom bildet die Hypernatriämie in Begleitung von Eosinophilie.8 Der TREC-KREC-Screeningtest zum Nachweis primärer Immundefekte wird routinemäßig im Neugeborenen-Screening durchgeführt.17 Bei Verdacht auf eine kutane Mastozytose sollte die Serumtryptase bestimmt werden.18
Erweiterte Untersuchungen
Erweiterte Untersuchungen umfassen eine Hautbiopsie, Trichoskopie, genetische Analysen (z.B. NGS-Panel), zusätzliche Blutuntersuchungen (z.B. Immunglobuline) oder bildgebende Verfahren je nach Indikation in Hinblick auf syndromale oder extrakutane Symptome. Eine Hautbiopsie zur histopathologischen Untersuchung inklusive Immunhistochemie (LEKTI-Färbung) ist besonders hilfreich zur Diagnosesicherung des Netherton-Syndroms.19 Darüber hinaus sollten eine Hautbiopsie und zusätzliche direkte Immunfluoreszenz bei Blasenbildung erfolgen. Die Trichoskopie kann zur Abgrenzung zwischen Netherton-Syndrom („Trichorrhexis invaginata“, Bambushaare), Trichothiodystrophie („Trichorrhexis nodosa“, brüchige glanzlose Haare) und Menkes-Syndrom („Pili torti“, verdrehte Haarschäfte) herangezogen werden.20,21
Genetische Analysen stehen für den Großteil des Spektrums der neonatalen Erythrodermie zur Verfügung und sollten möglichst frühzeitig zum Einsatz kommen.22 Die Bestimmung der Immunglobuline kann ebenfalls diagnostisch wegweisend sein. Unterschiedlich hohe IgE-Level finden sich bei der atopischen Dermatitis (bis 1000IU/ml), dem Chanarin-Dorfman-Syndrom (über 1000IU/ml), dem Netherton-Syndrom (bis 15000IU/ml) und dem Omenn-Syndrom (bis 45000IU/ml).20,23 Erniedrigte IgA-Level deuten auf einen selektiven IgA-Mangel oder ein Netherton-Syndrom hin.24,25 Die IgG-Level können bei primären Immundefekten erniedrigt sein, aber auch im Normbereich (aufgrund maternaler IgG) liegen.24 Bei Verdacht auf eine syndromische Ichthyose kann ein Blutausstrich hilfreich sein. Der Nachweis von Lipidvakuolen in Granulozyten ist hierbei charakteristisch für das Chanarin-Dorfman-Syndrom.12 Bildgebende Verfahren können insbesondere bei primären Immundefekten wegweisend sein. Beim variablen Immundefektsyndrom (CVID) sind typischerweise Bronchiektasen, verdickte Bronchialwände und Atelektasen im Thorax-Röntgen nachweisbar. Zudem kann eine zerebrale Magnetresonanztomografie diffuse leptomeningeale Verdickungen, zerebrale Atrophien und Abszesse aufzeigen. Bei den schweren kombinierten Immundefekten (SCID) und dem DiGeorge-Syndrom finden sich eine schmale obere mediastinale Kontur sowie eine retrosternale Aufhellung im Thorax-Röntgen. Diese Veränderungen sind auf das Fehlen des Thymus zurückzuführen.26 Skelettale Fehlbildungen, wie sie beispielsweise beim Sjögren-Larsson-Syndrom, Conradi-Hünermann-Happle-Syndrom und DiGeorge-Syndrom vorkommen, können röntgenologisch nachgewiesen werden. Eine Echokardiografie sollte bei Verdacht auf DiGeorge-Syndrom, Sjögren-Larsson-Syndrom oder KID-Syndrom durchgeführt werden.6
Extrakutane Symptome zeigen sich häufig bei syndromischen Ichthyosen, primären Immundefekten und Stoffwechselerkrankungen.27 Die Gedeihstörung ist ein charakteristisches Merkmal des Netherton-Syndroms und aller Formen der primären Immundefekte. Im Gegensatz dazu fehlt diese bei der atopischen Dermatitis und kommt nur selten bei Ichthyosen vor.8 Neurologische Auffälligkeiten sind vor allem mit Stoffwechselstörungen vergesellschaftet.12Seltene Ursachen für eine Erythrodermie in der Neugeborenenperiode stellen die atopische Dermatitis, Psoriasis vulgaris und seborrhoische Dermatitis dar. Diese Hauterkrankungen manifestieren sich normalerweise erst ab dem 3. Lebensmonat.22
Literatur:
1 Dvorak CC et al.: The diagnosis of severe combined immunodeficiency (SCID): The Primary Immune Deficiency Treatment Consortium (PIDTC) 2022 Definitions. J Allergy Clin Immunol 2023; 151(2): 539-46 2 Lankester AC et al.: Hematopoietic cell transplantation in severe combined immunodeficiency: The SCETIDE 2006-2014 European cohort. J Allergy Clin Immunol 2022; 149(5): 1744-54.e8 3 Caglayan Sozmen S et al.: Cyclosporin treatment improves skin findings in omenn syndrome. Pediatr Dermatol 2015; 32(2): e54-7 4 Fischer A, Hacein-Bey-Abina S: Gene therapy for severe combined immunodeficiencies and beyond. J Exp Med 2020; 217(2): e20190607 5 Lancester AC et al.: Phase I/II clinical trial stem cell gene therapy in RAG1-deficient SCID (RAG1-SCID) [updated 2024-04-18]. Verfügbar unter https://clinicaltrials.gov/study/NCT04797260 (zuletzt aufgerufen am 12.12.2024) 6 Cuperus E et al.: Proposal for a 6-step approach for differential diagnosis of neonatal erythroderma. J Eur Acad Dermatol Venereol 2022; 36(7): 973-86 7 Yigit S et al.: Drug-induced hypersensitivity syndrome in a premature infant. Pediatr Dermatol 2005; 22: 71-4 8 Pruzskowski Aet al.: Neonatal and infantile erythrodermas. A retrospective study of 51 patients. Arch Dermatol 2000; 136: 875-80 9 Van Gysel GD et al.: Collodion baby: a follow-up study of 17 cases. J Eur Acad Dermatol Venereol 2002; 16(5): 472-5 10 Rubio-Gomez GA et al.: Development of a disease severity score for newborns with collodion membrane. J Am Acad Dermatol 2014; 70: 506-11 11 Oji V et al.: Revised nomenclature and classification of inherited ichthyoses: results of the first ichthyosis consensus conference in Soreze 2009. J Am Acad Dermatol 2010; 63: 60741 12 Fraitag S, Bodemer C: Neonatal erythroderma. Curr Opin Pediatr 2010; 22: 438-44 13 Ott H, Grothaus J: Das rote, schuppende Baby: ein kinderdermatologischer Notfall: Klinik und Differenzialdiagnosen neonataler Erythrodermie. Hautarzt 2017; 68(10): 796-802 14 Dhar S et al.: Neonatal erythroderma: diagnostic and therapeutic challenges. Indian J Dermatol 2012; 57: 475-8 15 Sarkar R, Garg VK. Erythroderma in children. Indian J Dermatol Venereol Leprol 2010; 76: 341-7 16 Leung AKC et al.: Staphylococcal-scalded skin syndrome: evaluation, diagnosis, and management. World J Pediatr 2018; 14: 116-20 17 El-Sayed Z, Radwan N: Newborn screening for primary immunodeficiencies: the gaps, challenges, and outlook for developing countries. Front Immunol2020; 10: 2987 18 Koga H et al.: Neonatal onset diffuse cutaneous mastocytosis: a case report and review of the literature. Pediatr Dermatol 2011; 28(5): 542-6 19 Leclerc-Mercier S et al.: Early skin biopsy is helpful for the diagnosis and management of neonatal and infantile erythrodermas. J Cutan Pathol 2010; 37: 249-55 20 Sun JD, Linden KG: Netherton syndrome: a case report and review of the literature. Int J Dermatol 2006; 45(6): 693-7 21 Galve J et al.: Neonatal erythroderma as a first manifestation of Menkes disease. Pediatrics 2012; 130: e239-42 22 Ott H: Guidance for assessment of erythroderma in neonates and infants for the pediatric immunologist. Pediatr Allergy Immunol 2019; 30: 259-68 23 Van Gysel D et al.: Clinico-immunological heterogeneity in Comèl-Netherton syndrome. Dermatology 2001; 202: 99-107 24 Hannula-Jouppi K et al.: Intrafamily and interfamilial phenotype variation and immature immunity in patients with Netherton syndrome and Finnish SPINK5 founder mutation. JAMA Dermatol 2016; 152: 435-42 25 Wu EY et al.: Clinical and imaging considerations in primary immunodeficiency disorders: an update. Pediatr Radiol 2016; 46: 1630-44 26 Yin EZ et al.: Primary immunodeficiency disorders in pediatric patients: clinical features and imaging findings. Am J Roentgenol 2001; 176: 1541-52 27 Yoneda K: Inherited ichthyosis: syndromic forms. J Dermatol 2016; 43(3): 252-63
Das könnte Sie auch interessieren:
Long-Acting-Konzepte als Meilenstein in der HIV-Therapie
In den letzten vier Jahrzehnten erfuhr die HIV-Therapie eine enorme Entwicklung und die Optionen für Menschen mit HIV haben sich grundlegend verändert. Aktuell dominiert ein neues ...
Das Mikrobiomvon Wunden und was Probiotika für uns tun können
Unser Darm steht mit einer Vielzahl an Mikroorganismen über unterschiedlichste Funktionsachsen, wie jener zwischen Darm und Haut, mit dem gesamten Organismus in Verbindung. Das Mikrobiom ...
Sexuell übertragbare Infektionen bei Kindern und Jugendlichen
Seit 2019 berichten die World Health Organization (WHO) und die Centersfor Disease Control and Prevention (CDC; USA) regelmäßig über einen dramatischen Anstieg der sexuell übertragbaren ...