©
Getty Images/iStockphoto
Die ISG-Arthropathie – ein unterdiagnostiziertes Problem
Leading Opinions
Autor:
cand. med. Andrej Cousin
Autor:
Prof. Dr. med. Clément Werner
etzelclinic, Pfäffikon
E-Mail:
werner@etzelclinic.ch
30
Min. Lesezeit
23.11.2017
Weiterempfehlen
<p class="article-intro">Die ISG-Arthropathie gehört zu den am häufigsten übersehenen Krankheiten. Als Folge treten tieflumbale Rückenschmerzen auf, die mit bekannten Tests nicht exakt reproduziert werden können. Daraus resultiert für betroffene Patienten, dass sie von diversen medizinischen Fachrichtungen gesehen und nicht selten auf die psychiatrische Schiene abgeschoben werden. Die Beschreibung eines genauen klinischen Provokationstests und guter Therapiemöglichkeiten fehlte bisher im Armamentarium der Spezialisten des Bewegungsapparates.</p>
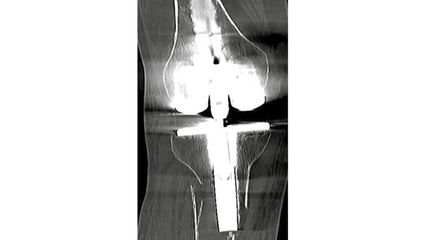
<p class="article-content"><div id="keypoints"> <h2>Keypoints</h2> <ul> <li>Das unterdiagnostizierte ISGLeiden muss bei der Differenzialdiagnostik tieflumbaler Rückenschmerzen miteinbezogen werden.</li> <li>Ein äusserst zuverlässiger und sinnvoller klinischer Test ist der PSIS-Distraktionstest, der schnell zur richtigen Diagnose führen kann.</li> <li>Die konservative Therapie kann die meisten ISG-Leiden lindern, nur in Ausnahmefällen ist eine chirurgische Intervention indiziert.</li> </ul> </div> <h2>No Man’s Land</h2> <p>Mit einer Inzidenz von 70 % ist der tieflumbale Rückenschmerz («low back pain», LBP) insbesondere bei älteren Personen ein sehr häufiges Krankheitsbild.<sup>1</sup> In einem Drittel der Fälle ist die Ursache des LBP das iliosakrale Gelenk (ISG).<sup>2–5</sup> Aufgrund des breiten Beschwerdebildes und der Komplexität der Anatomie bleibt das eigentliche Problem im ISG oft unerkannt.<sup>6, 7</sup> Nach dem Auftreten der Rückenschmerzen folgt für die Betroffenen meistens eine «Fachrichtungs-Odyssee», bei der sie von einer Vielzahl von Spezialisten untersucht werden, bis sie zuletzt psychiatrisch behandelt werden. Somit kommt es neben der medizinischen Problematik auch zum wirtschaftlichen Problem.<sup>1</sup> Das Schwierige dabei ist, die Zugehörigkeit der ISG-Arthropathien in der Medizin zu finden. Die Zuständigkeit des Wirbelsäulenspezialisten endet nämlich am Sakrum. Die Gynäkologen sind bis zur Schwangerschaft und währenddessen für ISG-Patienten zuständig, wodurch der häufige postpartale ISG-Schmerz auch oft undiagnostiziert bleibt. Das dem ISG proximalste Gelenk, mit dem sich Orthopäden beschäftigen, ist die Articulatio coxae. Eine ISGBlockade wäre durch den Chiropraktiker zu behandeln, jedoch verschwinden die Schmerzen der ISG-Arthropathie nach einer Mobilisation nicht. Der Rheumatologe beschäftigt sich mit dem Morbus Bechterew, nicht aber mit der ISG-Arthropathie. Als letzte Instanz werden die Patienten oft in die Obhut der Psychiater gegeben, wo versucht wird, das somatische Problem zu lösen (Abb. 1).</p> <p><img src="/custom/img/files/files_datafiles_data_Zeitungen_2017_Leading Opinions_Ortho_1704_Weblinks_lo_ortho_1704__s34_abb1.jpg" alt="" width="1051" height="1282" /></p> <h2>Innervation des ISG</h2> <p>Das Iliosakralgelenk ist die Verbindung zwischen der gemeinsamen Gelenkfläche der Segmente S1–S3 und dem Os ilium des Beckens. (Die sakralen Segmente verwachsen physiologischerweise zwischen dem 10. und 20. Lebensjahr.) Das ISG bietet eine hohe Stabilität, die unter anderem der unregelmässigen Gelenksfläche und dem starken Bandapparat zu verdanken ist. Seine Motilität ist dementsprechend sehr eingeschränkt.<sup>8</sup> Die Innervation des Gelenks erfolgt durch den Plexus lumbalis und kommt teilweise aus sakralen Segmenten. Die rein nozizeptive Versorgung des Gelenks erfolgt durch die Rami dorsales der Nervenwurzeln S1–S4.<sup>9–11</sup> Sogenannte Ansae, Nervenäste aus benachbarten Ligamenten und Facettengelenken, tragen auch zur Schmerzwahrnehmung am ISG bei.<sup>12, 13</sup> Die komplexe neurogene Versorgung erlaubt ein sehr vielfältiges Schmerzmuster, welches eine Kongruenz zu anderen Krankheitsbildern, wie zum Beispiel der Sakroiliitis oder der ISG-Blockade, aufweist.</p> <h2>Befund und klinische Tests</h2> <p>Anamnestisch kann der Unterschied zwischen entzündlichen und mechanischen Rückenschmerzen anhand der Rudwaleit’schen Kriterien (Tab. 1) identifiziert werden.<sup>14, 15</sup> Die Einteilung des typischen Schmerzmusters fehlt in der Literatur häufig. Patienten berichten über paravertebrale Schmerzen am lumbosakralen Übergang und am lateralen Bein, das Knie bleibt jedoch schmerzfrei (Abb. 2).<sup>16</sup> Da der nozizeptive Reiz bei ISG-Arthropathien meistens unilateral ist, sind beim betroffenen Patienten unruhiges Sitzen und häufiger Positionswechsel ein typisches Erscheinungsbild.<br /> Bei 44 % der Patienten haben die ISG-Beschwerden eine mechanische Ursache.17 Dies wird bei Menschen mit einer behandelten Beckenringfraktur deutlich. Über 30 % klagen über eine schmerzhafte posttraumatische ISG-Symptomatik.<br /> Momentan werden diverse klinische Provokationstests zur Diagnose eingesetzt. So versuchte man bisher anhand der Beckenkompression, der Beckendistraktion, des Gaenslen- Zeichens, des Thigh-Thrust- Tests und anhand des Faber- Zeichens eine ISG-Arthropathie zu diagnostizieren.<sup>5, 16, 18–20</sup> Jedoch sind diese Tests in diesem Fall nur von geringer klinischer Relevanz.<sup>5, 16, 18, 21–23</sup> Der Fehler liegt darin, anzunehmen, dass die oben genannten Tests nur die Schmerzreize im iliosakralen Gelenk reproduzieren, wobei die Kraftausübung auf das Hüftgelenk und die Spina iliaca anterior superior vernachlässigt wird.<sup>24, 25</sup> Der Verlust der klinischen Gültigkeit in der Untersuchung des ISG mithilfe des Mennell-Tests konnte in einem Vergleich von 11 Studien nachgewiesen werden.<sup>22</sup> Zudem besteht ein Zusammenhang zwischen ISG-generierten Schmerzen und Reizempfinden an der Spina iliaca posterior superior (PSIS).<br /> Der PSIS-Distraktionstest ist eine zuverlässige und schnelle Methode zur Diagnostik der ISG-Arthropathie. Er basiert darauf, dass der Untersucher punktuellen Druck auf die PSIS mit einem von medial nach lateral gerichteten Zug kombiniert (Abb. 3). Der Untersuchte kann dabei entweder stehen oder auf dem Bauch liegen. Berichtet der Untersuchte von einem stärkeren Reiz mit demselben Schmerzmuster, wird der Test als positiv bewertet.<sup>26</sup> Durch Testung an Patienten mit einer interventionell bestätigten ISG-Arthropathie konnte für den PSIS-Distraktionstest eine Testgenauigkeit von 94 % , eine Sensitivität von 100 % und eine Spezifität von 89 % nachgewiesen werden.<sup>26, 27</sup> Andere Provokationstests haben zwar eine sehr hohe Spezifität, aber eine äusserst niedrige Sensitivität (Faber-Test: 34 % ).<sup>26</sup><br /> Da alle Patienten mit ISG-Beschwerden erkannt werden, eignet sich der PSIS-Distraktionstest hervorragend als Screening-Untersuchung. Somit könnte das bisher gebräuchliche invasive Screening dadurch ersetzt werden. Fällt der Test bei einem Patienten vor dem 40. Lebensjahr positiv aus, so ist die Bestimmung folgender anamnestischer und labortechnischer Faktoren sinnvoll, um eine axiale Spondylarthritis (axSpA) auszuschliessen:</p> <ul> <li>Positive Familienanamnese</li> <li>Bilateraler Schmerz >3 Monate</li> <li>CRP</li> <li>Blutsenkungsgeschwindigkeit</li> <li>HLA-B27-Gen</li> </ul> <h2><img src="/custom/img/files/files_datafiles_data_Zeitungen_2017_Leading Opinions_Ortho_1704_Weblinks_lo_ortho_1704__s33_tab1.jpg" alt="" width="1417" height="456" /></h2> <p><img src="/custom/img/files/files_datafiles_data_Zeitungen_2017_Leading Opinions_Ortho_1704_Weblinks_lo_ortho_1704__s34_abb2.jpg" alt="" width="2150" height="1236" /></p> <p><img src="/custom/img/files/files_datafiles_data_Zeitungen_2017_Leading Opinions_Ortho_1704_Weblinks_lo_ortho_1704__s35_abb3.jpg" alt="" width="684" height="523" /></p> <h2>Bildgebende Diagnostik</h2> <p>Das Röntgen kann dazu genutzt werden, diverse Differenzialdiagnosen (z.B. Spondylarthritiden, Coxarthrosen und Frakturen) auszuschliessen.<sup>7, 16</sup> Aufgrund einer geringen Sensitivität führt ein unauffälliges Röntgen jedoch nicht zum Ausschluss einer ISG-Arthropathie.<sup>16</sup> Bei älteren Patienten mit dem in Abbildung 2 beschriebenen Schmerzmuster wird sehr stark empfohlen, von der Schnittbilddiagnostik Gebrauch zu machen. So können mit der Computertomografie osteoporotische Frakturen im posterioren Beckenring ausgeschlossen werden. Die CT kann aber auch eine Dysplasie verbildlichen, welche auf das ISG als Schmerzverursacher hinweist. Dabei sollte man besonders auf die Sakralisation, also die Segmentationsstörung der Verbindung zwischen L5 und S1, angezeigt durch eine verbleibende Bandscheibe, und auf das Bertolotti-Syndrom<sup>28</sup> achten. Röntgen und CT geben vor allem strukturelle Dysmorphien wieder, die neben der Sakralisation und dem Bertolotti- Syndrom noch «mamillary bodies», steil abfallende Alae<sup>29</sup>, das «Tongue in groove»- Zeichen, Osteophyten, eine Ankylosierung und Luft im iliosakralen Gelenk beinhalten. Insbesondere die Luft (hauptsächlich Stickstoff) im ISG ist pathognomonisch für eine ISG-Instabilität und wird im Rahmen einer Arthropathie immer gesehen. Aber auch die anderen Veränderungen deuten auf das im ISG lokalisierte Leiden hin. Neben der CT kann das MRI zum Ausschluss einer aktiven Sakroiliitis genutzt werden. Mit der STIR-Sequenz («short tau inversion recovery») können allgemein entzündliche Veränderungen besonders gut dargestellt werden.<sup>30–34</sup> Es konnte gezeigt werden, dass die Anwendung von Kontrastmitteln in diesem Fall keinen Nutzen hat.<sup>31</sup> Das MRI ist sowohl für die Diagnosestellung als auch für den Ausschluss ungenügend.<br /> Trotz der Identifizierung aller gesunden Patienten als richtig positiv (Spezifität 100 % ) kann die Szintigrafie wegen der Sensitivität von 13 % als radiologisches Hilfsmittel in der Bildgebung des iliosakralen Gelenks nicht genutzt werden.<sup>33, 35</sup> Die SPECT («single photon emission computed tomography») findet aufgrund ihrer hohen Sensitivität und Spezifität immer öfters Anwendung für die Diagnostik der iliosakralen Arthropathie.<sup>34, 36</sup></p> <h2>Infiltrationstechnik</h2> <p>Eine gesicherte ISG-Arthropathie wird wie folgt definiert: Das radiologisch auffällige oder unauffällige Gelenk löst Schmerzen aus, welche anhand einer lokalen intraartikulären Anästhesie um 70–90 % vermindert werden.<sup>12, 18, 21–23</sup> Somit gilt die Infiltration als Goldstandard für die Diagnostik.<sup>5, 16, 18–20, 23</sup> Die fehlerfreie Injektion des Anästhetikums in das Gelenk gelingt allerdings nur bei 22 % der klinischen Verfahren.<sup>8, 37</sup> Um die Treffsicherheit zu erhöhen, sollte man die Infiltration immer mithilfe von bildgebenden Methoden, bestenfalls mit dem Röntgen, durchführen. Aufgrund der komplexen anatomischen Zusammensetzung des ISG und seiner angrenzenden Strukturen kann dies trotz radiologischer Bestätigung zu rein extraartikulären Injektionen und so zu falsch negativen Ergebnissen führen.<br /> Bei der Durchführung sollte versucht werden, die Gelenkkapsel im synovialen dorsokaudalen Teil des Gelenks, dem sogenannten «Auge», zu treffen. Zum einen liegt dieser Abschnitt sehr oberflächlich und ist somit besser zugänglich; zum anderen beginnt eine Sakroiliitis häufig dort. Sobald dort die anästhetische Wirkung eingetreten ist, setzt man nach kranial fort und versucht, erst die Nerven um S3, dann um S2 zu betäuben. Sobald auch dort die Wirkung eingetreten ist, wird die Nadel intraartikulär eingeführt. Zuletzt sollen die Facettengelenke angezielt werden. Die alleinige intraartikuläre Infiltration genügt dabei oft nicht. Bei der Infiltration kann die Zuhilfenahme einer CT die Dauer des Eingriffs verkürzen.<sup>38</sup> Nach der Infiltration lässt man den Patienten nochmals den Schmerz beschreiben:</p> <ul> <li>Reduziert sich der Schmerz um weniger als 50 % , so muss nach einer anderen Schmerzursache gesucht werden.</li> <li>Reduziert sich der Schmerz um 50– 75 % , ist das Ergebnis für eine Aussage zu ungenau. Die Infiltration sollte wiederholt werden, bis die Schmerzlinderung diese Grenzen über- oder unterschreitet.</li> <li>Reduziert sich der Schmerz um mehr als 75 % , so ist eine iliosakrale Arthropathie wahrscheinlich und es sollte mit der konservativen Therapie begonnen werden.<sup>39</sup></li> </ul> <h2>Therapie</h2> <p>Die konservative Therapie beim akuten Schmerz beschränkt sich fast ausschliesslich auf die Applikation von NSAR und die Kühlung.<sup>8, 27</sup> In weiteren Schritten kann man eine Wärmetherapie anwenden oder bei vorliegender unterschiedlicher Länge der Beine versuchen diese zum Beispiel mit orthopädisch korrigierten Schuhen auszugleichen. Die Stabilisierung des ISG durch Aufbau der assoziierten Muskulatur (M. iliopsoas, M. biceps femoris, M. gluteus maximus) soll ebenfalls eine therapeutische Massnahme in der Akutphase sein.<sup>8, 16</sup> Besonders aus der Wirbelsäule stammende vertikale Scherkräfte auf das Iliosakralgelenk sollen vermieden werden. Demnach sollten Aktivitäten unterlassen werden, bei denen man auf einem Bein steht. Dazu gehören unter anderem Laufen, Kegeln, Skaten und Treppensteigen.<sup>40</sup></p> <p>Eine anatomische Ursache des ISG-Problems stellt die Kombination aus der Verkürzung des M. iliopsoas und der Schwächung des M. gluteus maximus sowie der ischiocruralen Muskulatur dar. Als Folge rotiert der Beckenring nach frontal.<sup>16, 40</sup> Ein angepasster Beckengürtel hat sich als gute Methode bewährt, die frontale Kippung um 30 % zu minimieren, um so eine achtbare Linderung der Schmerzen zu erzielen.<sup>8, 16, 40</sup> Auch Dehnen und Mobilisation haben eine schmerzminimierende Wirkung. Letztere sollten nicht während der Schwangerschaft durchgeführt werden.<br /> Voraussetzungen für eine chirurgische Intervention sind das Ausschöpfen der Möglichkeiten der konservativen Methoden bei chronischen Schmerzpatienten und ein klinisches Ansprechen auf die intraartikuläre Infiltration mit zeitlicher Begrenzung. Sind diese Bedingungen gegeben, kann versucht werden, eine minimal invasive iliosakrale Fusion, mit oder ohne zusätzliche Denervation unter endoskopischer Kontrolle, durchzuführen. Bei der Denervation wird mithilfe der Radiofrequenzablation versucht, die um das ISG liegenden Nervenbahnen zu zertrennen. Dabei wird der dorsale Anteil des Lig. sacrum bis zum S2/S3 durchtrennt. Anschliessend werden die Nervenwurzeln L5 und L4 und zuletzt die Iliumsäste der Nn. clunei durchgeschnitten. Wegen der Durchtrennung des Kapsel-Band-Apparates birgt das Verfahren das Risiko der Destabilisierung des Iliosakralgelenkes.<sup>39</sup><br /> Das iFuse-Implantatsystem™ als stabilisierende Fusionstechnik stellt die Alternative zur Ablation dar. Erst- und Zweijahreskontrollen zeigen aussichtsreiche Ergebnisse (Abb. 4).<sup>41</sup> Das Outcome der Langzeitstudien fehlt jedoch noch bei beiden Verfahren.<sup>27, 42, 43</sup></p> <p><img src="/custom/img/files/files_datafiles_data_Zeitungen_2017_Leading Opinions_Ortho_1704_Weblinks_lo_ortho_1704__s35_abb4.jpg" alt="" width="2150" height="793" /></p> <h2>Eigener Algorithmus</h2> <p>Berichtet der Patient von tieflumbalen Rückenschmerzen sowie Becken-, Hüftund Leistenschmerzen, (pseudo-)radikulären Schmerzen oder Sitzbeschwerden, soll zunächst nach der Ursache gesucht werden. So erhöhen zum Beispiel eine vaginale Geburt und ein Trauma zusammen mit dem typischen Schmerzmuster die Wahrscheinlichkeit einer ISG-Arthropathie. Wenn der Bericht des Patienten und die anamnestische Befragung positiv sind, kann der PSIS-Distraktionstest als klinische Untersuchung genutzt werden. Fällt der Provokationstest positiv aus, indem Schmerzen mit dem typischen Schmerzmuster (Abb. 2) reproduziert werden, so kann eine intraartikuläre ISG-Infiltration durchgeführt werden.</p> <p><img src="/custom/img/files/files_datafiles_data_Zeitungen_2017_Leading Opinions_Ortho_1704_Weblinks_lo_ortho_1704__s36_abb5.jpg" alt="" width="2150" height="1404" /></p></p>
<p class="article-footer">
<a class="literatur" data-toggle="collapse" href="#collapseLiteratur" aria-expanded="false" aria-controls="collapseLiteratur" >Literatur</a>
<div class="collapse" id="collapseLiteratur">
<p><strong>1</strong> Andersson GB: Lancet 1999; 354(9178): 581-5 <strong>2</strong> Daum WJ: Am J Orthop 1995; 24(6): 475-8 <strong>3</strong> Dontigny RL: Phys Ther 1990; 70(4): 250-65 <strong>4</strong> Sembrano JN, Polly DW: Spine 2009; 34(1): E27-32 <strong>5</strong> Schwarzer AC et al.: Spine 1995; 20(1): 31-7 <strong>6</strong> Slipman CW et al.: Arch Phys Med Rehabil 2000; 81(3): 334-8 <strong>7</strong> McGrath M: J Osteopath Med 2004; 7: 16-24 <strong>8</strong> Forst SL et al.: Pain Physician 2006; 9(1): 61-7 <strong>9</strong> Vleeming A et al.: J Anat 2012; 221(6): 537-67 <strong>10</strong> Grob KR et al.: Z Rheumatol 1995; 54(2): 117-22 <strong>11</strong> Patel N et al.: Pain Med 2012; 13(3): 383-98 <strong>12</strong> Szadek KM et al.: Clin Anat 2010; 23(2): 192-8 <strong>13</strong> Vilensky JA et al.: Spine 2002; 27(11): 1202-7 <strong>14</strong> Haikh SA: J Can Chiropr Assoc 2007; 51(4): 249-60 <strong>15</strong> Rudwaleit M et al.: Arthritis Rheum 2006; 54(2): 569-78 <strong>16</strong> Foley BS, Buschbacher RM: Am J Phys Med Rehabil 2006; 85(12): 997-1006 <strong>17</strong> Chou LH et al.: Pain Med 2004; 5(1): 26-32 <strong>18</strong> Slipman CW et al.: Arch Phys Med Rehabil 1998; 79(3): 288-92 <strong>19</strong> Broadhurst NA, Bond MJ: J Spinal Disord 1998; 11(4): 341-5 <strong>20</strong> Stone JA, Bartynski WS: Tech Vasc Interv Radiol 2009; 12(1): 22-32 <strong>21</strong> Szadek KM et al.: J Pain 2009; 10(4): 354-68 <strong>22</strong> van der Wurff P et al.: Man Ther 2000; 5(2): 89-96 <strong>23</strong> Dreyfuss P et al.: Spine 1996; 21(22): 2594-602 <strong>24</strong> Fortin JD, Falco FJ: Am J Orthop 1997; 26(7): 477-80 <strong>25</strong> Murakami E et al.: J Orthop Sci 2008; 13(6): 492-7 <strong>26</strong> Werner CM et al.: BMC Surg 2013; 13: 52 <strong>27</strong> Laux CJ et al.: Praxis 2015; 104(1): 33-9 <strong>28</strong> Manhoman S et al.: Malays Fam Physician 2015; 10(2): 55-8 <strong>29</strong> Laux CJ et al.: in press <strong>30</strong> Jans L et al.: Eur J Radiol 2014; 83(1): 179-84 <strong>31</strong> de Hooge M et al.: Rheumatology 2013; 52(7): 1220-4 <strong>32</strong> Rudwaleit M et al.: Ann Rheum Dis 2009; 68(10): 1520-7 <strong>33</strong> Tuite MJ: Semin Musculoskelet Radiol 2008; 12(1): 72-82 <strong>34</strong> Kotsenas AL: Radiol Clin North Am 2012; 50(4): 705-30 <strong>35</strong> Slipman CW et al.: Spine 1996; 21(19): 2251-4 <strong>36</strong> Scheyerer MJ et al.: Eur J Nucl Med Mol Imaging 2014; 41(Suppl 1): S59-66 <strong>37</strong> Rosenberg JM et al.: Clin J Pain 2000; 16(1): 18-21 <strong>38</strong> Bollow M et al.: J Comput Assist Tomogr 1996; 20(4): 512-21 <strong>39</strong> Laux CJ et al.: Praxis 2015; 104(1): 33-9 <strong>40</strong> Prather H: Clin J Sport Med 2003; 13(4): 252-5 <strong>41</strong> Polly DW et al.: Int J Spine Surg 2016; 10: 28 <strong>42</strong> Spiker WR et al.: Evid Based Spine Care J 2012; 3(4): 41-53 <strong>43</strong> Ashman B et al.: Evid Based Spine Care J 2010; 1(3): 35-44</p>
</div>
</p>
Das könnte Sie auch interessieren:
«Auch Patienten mit Demenz profitieren von einer chirurgischen Stabilisierung»
Patienten mit Hüftfraktur und einer leichten, mittelschweren oder schweren Demenz haben ein geringeres Risiko zu sterben, wenn sie operiert werden – vor allem wenn es sich um Kopf-Hals- ...
Management periprothetischer Frakturen am Kniegelenk
Mit steigenden Versorgungszahlen der Knieendoprothetik und dem höheren Lebensalter entsprechend der Alterspyramide nimmt auch die Zahl der periprothetischen Frakturen zu und stellt die ...
Patellofemorale Instabilität
In diesem Übersichtsartikel möchten wir ein Update über die aktuelle Diagnostik und die konservativen wie auch operativen Behandlungsmöglichkeiten der patellofemoralen Instabilität geben.