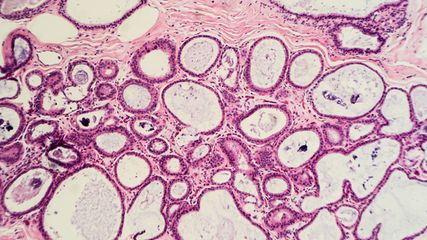
Stellenwert der Zytologie und Histologie in der Pathologie des Harntraktes
Autorin:
OÄ Dr. med. Tatjana Vlajnic
Institut für Medizinische Genetik und Pathologie
Universitätsspital Basel
E-Mail: Tatjana.Vlajnic@usb.ch
Zytologie und Histologie kommen in der Abklärung des Harntraktes bei unterschiedlichen Fragestellungen und Konstellationen zum Einsatz. Die Kenntnis der zugrundeliegenden pathologischen Veränderungen erlaubt, den Stellenwert der beiden Methoden besser zu verstehen, sie differenziert einzusetzen und die Resultate kritisch zu interpretieren.
Keypoints
-
Grundsätzlich sind Histologie und Zytologie bei der Abklärung des Harntraktes als gleichwertig beziehungsweise als sich teils ergänzende Methoden zu sehen.
-
Die Zytologie besitzt eine hohe Sensitivität in der Diagnose von HGUC und hat eine klassische Indikation in der Tumornachsorge von Patienten mit bekanntem HGUC.
-
Der Vorteil der Histologie liegt in der Abklärung des «low grade» nicht invasiven papillären Urothelkarzinoms sowie in der Beurteilung der Invasionstiefe bei soliden Urothelkarzinomen.
-
Eine FISH-Untersuchung (UroVysionTM-Test) kann zusätzlich zur Klärung unklarer zytologischer Befunde hinzugezogen werden.
Die Zytologie ist seit Jahrzehnten ein zentraler Bestandteil in der Abklärung von Erkrankungen der Harnwege sowie in der Nachsorge von Patienten mit urothelialen Neoplasien. Dabei eignen sich sowohl Spontanurin als auch im Rahmen einer Endoskopie gewonnene Spülflüssigkeit als zytologisches Untersuchungsmaterial. Letztere ist häufig zellreicher und weist weniger degenerative Zellveränderungen auf, wodurch sich die Aussagekraft der Untersuchung erhöht.
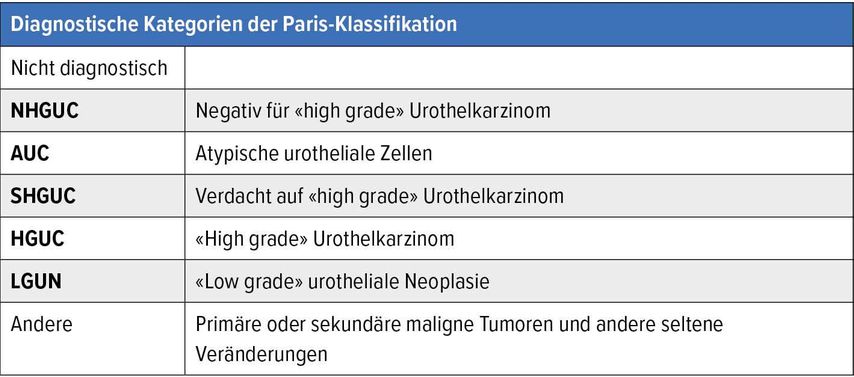
Vor einigen Jahren wurde die Paris-Klassifikation («The Paris System», TPS) im diagnostischen Alltag eingeführt, mit dem Ziel, ein international standardisiertes Befundungssystem für die Urinzytologie zu etablieren. Für die diagnostischen Kategorien der Paris-Klassifikation wurden genau definierte und reproduzierbare morphologische Kriterien festgelegt in Hinsicht auf einen möglichst hohen positiven prädiktiven Wert für die Diagnose des potenziell lebensbedrohlichen «highgrade» Urothelkarzinoms (HGUC).1,2 Zudem haben sich dadurch auch eine Reduktion und eine bessere Eingrenzung der bisher uneinheitlich genutzten Diagnose von «Atypien» ergeben, was die Aussagekraft der Urinzytologie verbessert hat (Tab. 1). Das Prinzip dieser Einteilung basiert auf der hohen Sensitivität der Zytologie für den Nachweis von HGUC, da sich hier die Zellveränderungen am deutlichsten zeigen und die Abweichungen von der Norm am stärksten ausgeprägt sind.
Unter der Voraussetzung einer gewissen diagnostischen Erfahrung in der Zytologie lässt sich die Mehrheit der zytologischen Befunde mit der sogenannten «Fünf-Sekunden-Regel» diagnostizieren: Eindeutig negative Befunde oder eindeutig maligne Befunde lassen sich auf den ersten Blick als solche erkennen.
Im Folgenden wird die Rolle der Zytologie und Histologie in Abhängigkeit von den vorhandenen Läsionen dargestellt.
Abklärung flacher Läsionen
In der Abklärung von flachen, zystoskopisch unklaren Läsionen der Harnblase, die als Rötungen oder Unregelmässigkeiten der Harnblasenschleimhaut imponieren, ist die Zytologie die diagnostisch zielführende Untersuchung. Differenzialdiagnostisch kann es sich dabei um entzündlich reaktive Veränderungen handeln oder ein urotheliales Carcinoma in situ (CIS), wobei diese Unterscheidung endoskopisch nicht immer sicher möglich ist. Zytologisch oder histologisch ist dies jedoch in der Regel keine diagnostische Herausforderung. Ein klarer Vorteil der Zytologie gegenüber der Histologie besteht im extremen Fall einer «denudierenden Zystitis». Dahinter verbirgt sich meist ein CIS, in welchem die Zellen aufgrund des verminderten Zusammenhaltes abschilfern und anschliessend nur in der Spülflüssigkeit nachweisbar sind, die «denudierten» Schleimhautbiopsien sind hingegen diagnostisch nicht weiterführend. Manchmal wird auch ein sehr umschriebenes oder sich diskontinuierlich ausbreitendes CIS in einer kleinen Biopsie nicht erfasst, hier ist ebenfalls die Zytologie der Histologie überlegen.
Die Zytologie spielt ausserdem eine wichtige Rolle in der Nachsorge von Patienten mit bekanntem HGUC. Zytologische Kontrollen unter oder nach stattgehabter intravesikaler «Bacillus-Calmette-Guérin»(BCG)-Behandlung dienen dazu, das Ansprechen auf die Therapie zu evaluieren und ein mögliches Rezidiv frühzeitig zu entdecken.
Flache Läsionen des oberen Harntraktes (OHT) sollten ebenfalls präferenziell mittels Zytologie abgeklärt werden: Einerseits sind flache Läsionen des OHT aufgrund von anatomischen Gegebenheiten schwierig zu biopsieren, andererseits wird mittels Spülzytologie praktisch der gesamte Harntrakt untersucht, sodass auch Zellen eines umschriebenen Prozesses mit hoher Wahrscheinlichkeit erfasst werden können.
Abklärung solider Tumoren
Bei soliden Tumoren, in den meisten Fällen wenig differenzierte Urothelkarzinome, ist die Eindringtiefe für die Bestimmung der pT-Kategorie entscheidend für die Therapieplanung und den weiteren klinischen Verlauf. Naturgemäss sind der Nachweis eines invasiven Wachstums und die Beurteilung der Invasionstiefe an zytologischen Präparaten nicht möglich. Somit ist zur Unterscheidung von muskelinvasiven und nicht muskelinvasiven Urothelkarzinomen die histologische Untersuchung klinisch relevant und der Zytologie überlegen.
Bei klinischem Nachweis eines soliden Tumors in der Harnblase muss differenzialdiagnostisch nebst einer nicht epithelialen Neoplasie auch an die seltene Möglichkeit einer Metastase gedacht werden. Zu erwähnen sind hier insbesondere Primärtumoren aus Organen mit topografischer Nähe zur Harnblase, wie Prostata- oder Rektumkarzinome, aber auch andere metastasierte Tumoren wie z.B. Mamma- und Ovarialkarzinome oder Melanome. Während histologisch architektonische Besonderheiten wie z.B. glanduläres Wachstum bei Adenokarzinomen hilfreich für die Diagnose sind, sind die zytologischen Merkmale, welche auf eine Metastase deuten, oftmals subtil und leicht zu übersehen. So können bei wenig differenzierten Prostatakarzinomen die typischen prominenten Nukleolen fehlen und lediglich angedeutet azinäre Formationen hinweisend sein. Bei Nachweis von zytoplasmatischem Schleim ist differenzialdiagnostisch an die Metastase eines Adenokarzinoms zu denken, da primäre Adenokarzinome der Harnblase äusserst selten sind. Die weitere Eingrenzung der Differenzialdiagnosen erfolgt mittels Immunzytochemie. Letztendlich ist hier auch die Kenntnis bzw. Mitteilung der klinischen Vorgeschichte von grosser Bedeutung für die richtige Diagnosestellung.
Abklärung papillärer Tumoren
Nicht invasive papilläre Urothelkarzinome sind mit Abstand die häufigsten Tumoren der Harnblase. Es handelt sich zumeist um «lowgrade» nichtinvasive papilläre Urothelkarzinome, die zwar häufig rezidivieren, jedoch eine günstige Prognose aufweisen, da sie, im Gegensatz zu «highgrade»Tumoren, selten zu invasiven Karzinomen fortschreiten.
Endoskopisch werden papilläre Tumoren abgetragen und stellen dann histologisch kein nennenswertes diagnostisches Problem dar. Bei «high grade» papillären Tumoren mit ausgeprägten Kernatypien gelingt die Diagnose auch zytologisch zuverlässig. Die Unterscheidung eines «low grade» papillären Tumors vom Normalbefund ist demgegenüber zytologisch schwieriger, da die nukleären Veränderungen sehr diskret sein können. Deshalb ist es möglich, dass ein zystoskopisch eindeutig pathologischer Befund eines papillären Tumors zytologisch als «negativer Befund» (NHGUC) erscheint. Unter Umständen kann eine «low grade» papilläre Neoplasie (LGUN) zytologisch vermutet werden, wenn z.B. das Zellbild monoton erscheint, die Urothelien diskrete Kernatypien (ohne Hyperchromasie!) aufweisen und eine erhöhte Kern-Plasma-Relation besteht. In der Vergangenheit war der Stellenwert der Zytologie in der Abklärung von «low grade» urothelialen Tumoren deshalb umstritten. Aufgrund der nun sehr strengen, standardisierten und einfach reproduzierbaren Definitionen der Paris-Klassifikation hat sich allerdings auch hier der Stellenwert verbessert: LGUN können nur bei zusätzlichem Nachweis von Papillen diagnostiziert werden.
Eine Besonderheit stellen papilläre Tumoren des oberen Harntraktes dar, welche als schwieriges Gebiet in der Zytologie gelten. Hier sind die Kernatypien auch bei grossen und endoskopisch eindeutig erkennbaren Tumoren eher diskret, was in einer vermeintlich negativen Zytologie resultiert.
Die «G2»-Problematik bei papillären Tumoren
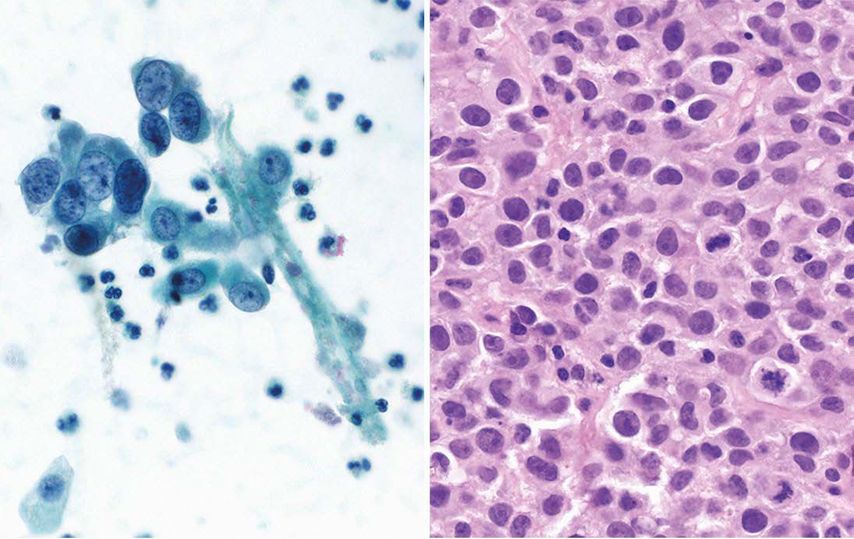
In der aktuellen WHO-Klassifikation der Urothelkarzinome wurde die seit Jahrzehnten bestehende dreistufige Einteilung der Differenzierungsgrade der nichtinvasiven papillären Urothelkarzinome durch ein zweistufiges System ersetzt, welches nun zwischen den Kategorien «lowgrade» und «highgrade» unterscheidet. Dadurch werden die weitere Diagnostik und Therapie standardisiert und stark vereinfacht. Biologisch gesehen besteht zwischen diesen beiden Gruppen jedoch ein Kontinuum. Im Grauzonenbereich der intermediären Atypien kann somit sowohl in der Histologie als auch in der Zytologie die Unterscheidung zwischen «lowgrade» und «highgrade» schwierig sein. Zytologisch kann unter Umständen nur die Verdachtsdiagnose eines HGUC geäussert werden (Abb. 1). In histologischen Präparaten kann z.B. die vermehrte Anzahl von Mitosen als Entscheidungshilfe dienen, um den Tumor eher in die Kategorie «highgrade» einzustufen. In diesem Zusammenhang ist auch das Phänomen von «hypochromatischen» HGUC zu erwähnen, welches nur in zytologischen Proben, jedoch nicht in entsprechenden Biopsien beobachtet wurde.3 Diese Besonderheit muss diagnostisch berücksichtigt werden, da sie in gewissem Widerspruch zur Paris-Klassifikation steht, in der definitionsgemäss die Kern-Hyperchromasie als Hauptkriterium für die Diagnose eines HGUC gilt.
Abb. 1: Zytologischer Befund (links): Verdacht auf «highgrade»Urothelkarzinom (SHGUC). Korrespondierender histologischer Befund (rechts) entspricht eindeutig einem wenig differenzierten («highgrade») Urothelkarzinom
Der Wolf im Schafspelz
Eine diagnostische Herausforderung sowohl zytologisch als auch histologisch stellt die sogenannte «nested variant» des Urothelkarzinoms dar. Hierbei handelt es sich um einen besonderen Subtyp, welcher zwar selten ist, jedoch einen aggressiven Verlauf zeigt. Dieser Tumor wächst in kleinen Nestern aus paradoxerweise wenig atypischen Zellen. Die Tumorzellen können derart bland aussehen, dass eine Diagnose auch an zytologischen Präparaten sehr schwierig oder gar unmöglich ist. An oberflächlichen Biopsien der Harnblase kann dieser Tumor leicht übersehen werden. Differenzialdiagnostisch stellt die Abgrenzung zu einer Cystitits cystica oder zu von Brunn’schen Nestern, welche die wichtigsten Differenzialdiagnosen darstellen, die grösste Herausforderung dar. Falls allerdings tiefere Wandschichten in der transurethralen Resektion (TUR) erfasst sind, gelingt die Diagnose anhand der Infiltration der muskulären Harnblasenwand relativ einfach.
FISH als molekulare Zusatzmethode
Die am besten validierte molekulare Zusatzmethode für die Abklärung unklarer zytologischer Befunde ist der UroVysionTM-Test.4, 5 Es handelt sich hier um eine Fluoreszenz-in-situ-Hybridisierung(FISH)-Untersuchung zum Nachweis chromosomaler Aberrationen als Ausdruck eines neoplastischen Prozesses. Die Paris-Kategorien bieten dabei eine wichtige Grundlage für eine gezielte Indikationsstellung. In einer kürzlich publizierten Arbeit konnten wir den Stellenwert der UroVysionTM-FISH vor dem Hintergrund der Paris-Klassifikation untersuchen.6Gemäss unserer Erfahrung lässt sich die FISH-Untersuchung vor allem bei den TPS-Kategorien AUC und SHGUC (vgl. Tab. 1) sinnvoll in den diagnostischen Algorithmus implementieren, wodurch in den meisten Fällen eine zuverlässige Unterscheidung zwischen reaktiven Veränderungen und einer urothelialen Neoplasie möglich ist.
Literatur:
1 Rosenthal DL et al.: The Paris system for reporting urinary cytology. 1. Auflage. Berlin: Springer Verlag, 2016 2 Barkan GA et al.: The Paris system for reporting urinary cytology: the quest to develop a standardized terminology. Acta Cytol 2016; 60(3): 185-97 3 Pierconti F et al.: Hypochromatic large urothelial cells in urine cytology are indicative of high grade urothelial carcinoma. APMIS 2018; 126(9): 705-9 4 Halling KC et al.: A comparison of cytology and fluorescence in situ hybridization for the detection of urothelial carcinoma. J Urol 2000; 164(5): 1768-75 5 Bubendorf L: Multiprobe fluorescence in situ hybridization (UroVysion) for the detection of urothelial carcinoma - FISHing for the right catch. Acta Cytol 2011; 55(2): 113-9 6 Vlajnic T et al.: The Paris system for reporting urinary cytology in daily practice with emphasis on ancillary testing by multiprobe FISH. J Clin Pathol 2020; 73(2): 90-5
Das könnte Sie auch interessieren:
Die Pathologie des Magenkarzinoms
Weltweit ist das Magenkarzinom der am fünfthäufigsten diagnostizierte maligne Tumor, mit einer verhältnismäßig hohen Sterblichkeit, bedingt vor allem durch das weit fortgeschrittene ...
Das Grading des Urothelkarzinoms
Das Grading des Urothelkarzinoms (UK) ist immer wieder ein Thema, das Pathologen und Urologen beschäftigt. Das Bestimmen eines Grades erlaubt die Differenzierung eines UK zu bewerten und ...
The impact of inherited mutations in oncohaematology
Acquired mutations detection by the use of next-generation sequencing (NGS) is largely used in oncohaematology. Germline mutations have also shown to play a major role in this context ...