<p class="article-intro">Die Verwendung von Leichennerven zur Rekonstruktion peripherer Nerven Seit einigen Jahren besteht die Möglichkeit, schwere Verletzungen peripherer Nerven vor allem der oberen Extremitäten mit speziell aufgearbeiteten Totspendenerven zu therapieren. Dieser neue Zugangsweg verspricht eine nebenwirkungsärmere Behandlung bei hochgradigen Nervenverletzungen im Vergleich zur standardmäßig angewandten Nerventransplantation mit Eigenspendenerv.</p>
<hr />
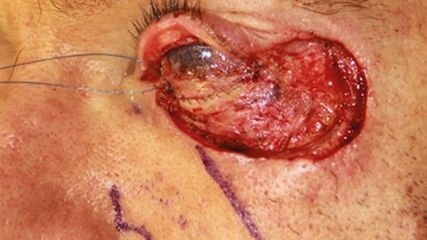
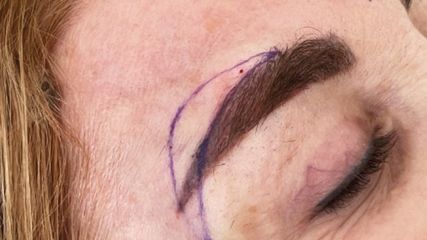
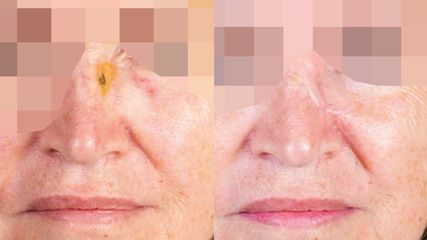
<p class="article-content"><h2>Nervenrekonstruktion peripherer Nerven</h2> <p>Schwere Nervenverletzungen ziehen Defizite in motorischer und sensibler Funktion der Extremitäten nach sich. Oft führen solche Traumata zu tiefgreifenden Einschränkungen im Leben der Patienten. Ist die Kontinuität des betroffenen Nervs nicht mehr gegeben, muss sie durch operative Maßnahmen wiederhergestellt werden. Ziel ist eine spannungsfreie Koaptierung der beiden Nervenstümpfe. Erscheint eine direkte Approximierung der Nervenenden aufgrund des Ausmaßes, der Kontaminierung der Verletzung oder der Retraktion des Nervs nicht möglich, so muss der Defekt interpositioniert werden. Allseits als Goldstandard anerkannt ist die Überbrückung von Nervendefekten mit autologen Nerventransplantaten.<sup>1</sup> Das heißt, das für die Wiederherstellung benötigte Nervenstück wird vom Patienten selbst gewonnen. Die Nachteile dieses Vorgehens, wie Sensibilitätsstörungen an der Hebestelle, zusätzliche Narben und prolongierte Operationszeit, führten dazu, neue Herangehensweisen und Alternativen für die sogenannten Autografts zu erforschen. Mittlerweile gibt es eine Vielfalt von biologischen und synthetischen Nervenüberbrückungen, sogenannte Konduite und allogene, von Organspendern gewonnene Nerventransplantate. Ohne spezielle Behandlung der Spendernerven verursachen die Nerventransplantate Abstoßungsreaktionen, die auch trotz immunsuppressiver Therapie auftreten können.<sup>2</sup> Entwicklungen in der medizinischen Technologie ermöglichen die Dezellularisierung der Nerventransplantate, wobei die Hüllstrukturen der Nerven bestehen bleiben, aber die Immunogenität herabgesetzt wird und die Patienten somit keine immunsuppressive Therapie brauchen.<sup>3</sup> In den letzten Jahren kristallisierten sich humane azelluläre Allografts als die am vielversprechendste Alternative zu Autografts heraus.<sup>4</sup> Verglichen mit traditionellen Methoden, ermöglicht die Nervenrekonstruktion mit azellulären Allografts die Vermeidung von Hebemorbiditäten und eine kürzere OP-Zeit.</p> <h2>Allografts als Alternative für Autografts</h2> <p>Die Vorteile einer Nervenwiederherstellung mit autologen Nerven sind gut erforscht. Sie unterstützen die Nervenregeneration mit den notwendigen Komponenten inklusive intakter Nervenarchitektur und Mediatoren, die es den Axonen ermöglichen, zielgerichtet auszusprossen, was zu einer Reinnervation der deinnervierten Organe führt. Sensibilitätsstörungen, Schmerzen, Neurome im Bereich der Hebestelle, zusätzliche Narben, limitierte Verfügbarkeit und verlängerte OP-Dauer gaben den Anstoß zur Erforschung von Alternativen. Denaturierte Nervenallografts könnten eine Lösung für diese unerwünschten Morbiditäten darstellen. Von Totspendern gewonnene Nerven werden durch spezielle enzymatische, chemische Prozesse und durch radioaktive Bestrahlung aufgearbeitet, um die Immunogenität aufzuheben und so eine Transplantatabstoßung zu verhindern. Trotz dieser Vorbehandlung behält das Transplantat die für die Nervenregeneration notwendigen Bestandteile in Makro- und Mikrostruktur. Ein intaktes Epi- und Perineurium als makrostrukturelle Hüllstrukturen ermöglichen dem Chirurgen, das Allograft in gleicher Art und Weise wie das Autograft in den Defekt zu interponieren. Mikrostrukturelle Komponenten wie das erhaltene Endoneurium geben den aussprossenden Axonen eine Leitstruktur, um gerichtet auswachsen und so das Endorgan erreichen zu können.<sup>5</sup> In Studien und auch im klinischen Alltag erweist sich die Nerventransplantation mit Allografts als sehr vielversprechend. In über 87 % der behandelten oberen Extremitäten kommt es zu einer bedeutenden funktionellen Regeneration der betroffenen Gliedmaße.<sup>6</sup> Außerdem zeigte sich in Tierversuchen eine zu Autografts ähnliche Revaskularisierung und mikro- und makrostrukturelle Integration der Transplantate.<sup>7</sup> Ein großer Vorteil bei der Verwendung von vorbehandelten Spendernerven ist eine große Verfügbarkeit der Allografts in verschiedenen Kalibern und Längen. Ein adäquates Interponat kann für den jeweils betroffenen Nerv, vom Digitalnerv bis zum Hauptstamm des Nervus medianus, ulnaris oder radialis, verwendet werden. Bei Rekonstruktion eines Nervenhauptstammes ist bei Verwendung von autologen Transplantaten die Interposition von mehreren Stücken, sogenannten Kabeln, notwendig, um den gesamten Durchmesser des geschädigten Nervs wiederherstellen zu können. Nur dieser Zugang ermöglicht die Regeneration aller durchtrennten Nervenaxone. Bei Anwendung eines Allografts werden dem betroffenen Patienten ein weiterer Eingriff zur Hebung eines autologen Transplantates und die damit verbundenen Risiken für Komplikationen erspart. Dadurch kann die Operationszeit deutlich gesenkt werden.</p> <h2>Klinischer Einsatz von Allografts</h2> <p>Patienten mit ausgeprägten Nervenläsionen und damit verbundenen funktionellen Einschränkungen der betroffenen Extremität müssen genau abgeklärt werden. Nach anamnestischer Erhebung des Verletzungshergangs, klinischer Untersuchung und Diagnostik inklusive elektrophysiologischer Untersuchungen mittels EMG und NLG sowie bildgebender Maßnahmen kann die OP-Indikation gestellt werden. Ist die Überbrückung längerer Nervendefekte unvermeidlich, so ist es möglich, neben der bisher standardmäßig durchgeführten autologen Nerventransplantation die Läsion mittels eines aufgearbeiteten Leichennervs zu rekonstruieren. Präoperativ wird das Ausmaß des Nervendefekts durch erhobene diagnostische Befunde eingeschätzt und adäquate allogene Nerventransplantate werden bereitgestellt. Bei der OP werden standardmäßig die betroffenen Nervenenden neurolysiert und so weit rückgekürzt, bis unverletztes Nervengewebe vorliegt und die Faszikelgruppen identifiziert werden können. Der allogene Spendernerv wird nach Vorgaben des Herstellers mit Kochsalzlösung aufbereitet, unter Mikroskopsicht in den Defekt eingepasst und mit feinen Nähten koaptiert (Abb. 1–4). Die so eingebrachten nervalen Hüllstrukturen ermöglichen es dem Nerv, seine Axone wieder zu ihren Endorganen gerichtet auswachsen zu lassen. Dieser Prozess dauert je nach Höhe des Nervendefektes an der verletzten Extremität Monate bis Jahre. In dieser Phase ist es wichtig, regelmäßige Verlaufskontrollen klinischer und elektrophysiologischer Funktionen sowie intensive ergotherapeutische Maßnahmen durchzuführen. Nur so kann eine möglichst zufriedenstellende Wiedergewinnung der verlorenen Funktion gewährleistet werden. Aus eigener Erfahrung können bei Patienten mit präoperativ kompletter Anästhesie im Versorgungsgebiet des N. medianus, nach erfolgreicher Nervenrekonstruktion mit Allograft, annähernd normale Zwei-Punkt-Diskriminationswerte von 4mm im Bereich der Fingerbeeren erzielt werden. Dieser Umstand ermöglicht es den behandelten Patienten, ihren alltäglichen manuellen Tätigkeiten wieder nachgehen zu können.</p> <p><img src="/custom/img/files/files_datafiles_data_Zeitungen_2017_Jatros_Derma_1703_Weblinks_s54.jpg" alt="" width="1417" height="1386" /></p> <h2>Konklusion</h2> <p>In der Behandlung von ausgeprägten Nervenverletzungen mit der Notwendigkeit von Nerventransplantaten etabliert sich in den letzten Jahren die Verwendung von azellulären Leichennerven als vielversprechende Alternative zur bisher standardmäßig durchgeführten Rekonstruktion mit Eigennerven. Vorteile liegen in der äußerst großen Verfügbarkeit der allogenen Transplantate in verschiedenen Größen, der guten chirurgischen Handhabung und der Vermeidung der Entnahme eines eigenen Spendernervs mit assoziierten Hebemorbiditäten und Verlängerung der OP-Dauer. Diese neue Herangehensweise, um Nervendefekte zu überbrücken, ermöglicht eine gute Regeneration von funktionellen Nervenläsionen. Abzuwarten sind Langzeit­ergebnisse, die Anwendung dieser Technik in größeren Fallzahlen und Zentren, um die sehr vielversprechenden Ergebnisse auch zu bestätigen.</p></p>
<p class="article-footer">
<a class="literatur" data-toggle="collapse" href="#collapseLiteratur" aria-expanded="false" aria-controls="collapseLiteratur" >Literatur</a>
<div class="collapse" id="collapseLiteratur">
<p><strong>1</strong> Dellon AL, Mackinnon SE: Basic scientific and clinical applications of peripheral nerve regeneration. Surg Annu 1988; 20: 59-100 <strong>2</strong> Mackinnon SE, Hudson AR: Clinical application of peripheral nerve transplantation. Plast Reconstr Surg 1992; 90: 695-9 <strong>3</strong> Hudson TW et al.: Optimized acellular nerve graft is immunologically tolerated and supports regeneration. Tissue Eng 2004; 10: 1641-51 <strong>4</strong> Yang LM et al.: Human peripheral nerve-derived scaffold for tissue-engineered nerve grafts: histology and biocompatibility analysis. J Biomed Mater Res B Appl Biomater 2011; 96B: 25-33 <strong>5</strong> Avance nerve graft – instructions for use, available online at <a href="http://www.axogeninc.com">www.axogeninc.com</a> <strong>6</strong> Brooks et al.: Processed nerve allografts for peripheral nerve reconstruction: A multicenter study of utilization and out­comes in sensory, mixed, and motor nerve reconstructions. Microsurgery 2012; 32: 1-14 <strong>7</strong> Whitlock EL et al.: Processed allografts and type I collagen conduits for repair of peripheral nerve gaps. Muscle Nerve 2009; 39: 787-99</p>
</div>
</p>